Incretinas: Guía Definitiva de Hormonas Clave en Metabolismo
Resumen Clínico Rápido
🔬 Clasificación
Hormonas Pépticas Gastrointestinales
⚙️ Función Principal
Regulación Glucémica Postprandial
📋 Impacto Clave
Control de Glucosa, Peso y Saciedad
Descifrando las Incretinas: Los Mensajeros Ocultos de Nuestro Metabolismo
En el intrincado universo de la fisiología humana, existen moléculas que actúan como directores silenciosos de orquesta, coordinando respuestas vitales con una precisión asombrosa. Entre estas, las incretinas emergen como protagonistas esenciales, un grupo de hormonas gastrointestinales que han revolucionado nuestra comprensión del control glucémico y la homeostasis energética. Lejos de ser meros auxiliares, estas sustancias pépticas son fundamentales para la regulación postprandial de la glucosa, el apetito y, en última instancia, el peso corporal y la salud metabólica general. Su descubrimiento y el desentrañamiento de sus complejos mecanismos de acción no solo han abierto nuevas vías para el tratamiento de la diabetes tipo 2 y la obesidad, sino que también nos ofrecen una ventana a la sofisticada interconexión entre nuestro sistema digestivo, el páncreas y el cerebro.
Esta guía enciclopédica del Glosario Ketocis se adentrará en la esencia de las incretinas, explorando su origen, su fascinante fisiología molecular, su papel crucial en la respuesta a los nutrientes y las implicaciones de su disfunción. Desde su producción en el intestino hasta su influencia en la secreción de insulina y glucagón, y su impacto en la saciedad y la neuroprotección, desvelaremos por qué estas hormonas son mucho más que simples reguladores de la glucosa. Preparémonos para un viaje profundo al corazón de la ciencia metabólica, donde la comprensión de las incretinas no es solo una cuestión de conocimiento, sino una herramienta poderosa para la optimización de la salud.
Resumen Clínico
- Las incretinas son hormonas gastrointestinales (GLP-1 y GIP) liberadas en respuesta a la ingesta de nutrientes.
- Estimulan la secreción de insulina de manera glucosa-dependiente y suprimen la liberación de glucagón, contribuyendo al control de la glucemia postprandial.
- Además de su efecto pancreático, influyen en la saciedad, el vaciamiento gástrico y ofrecen beneficios cardiovasculares y neuroprotectores.
Las incretinas solo importan en diabéticos.
Su rol es fundamental en la fisiología glucémica normal y su disfunción contribuye a diversas patologías metabólicas, no solo la diabetes. Son clave para la saciedad y el metabolismo general en individuos sanos.
Origen y Descubrimiento de las Incretinas: Una Historia de Revelación Metabólica
La idea de que el intestino pudiera influir en la secreción de insulina del páncreas no es nueva. Ya en 1902, los fisiólogos británicos William Bayliss y Ernest Starling acuñaron el término ‘secretina’ para describir una sustancia liberada por el intestino que estimulaba la secreción pancreática. Sin embargo, no fue hasta la década de 1960 cuando se empezó a sospechar que existían factores intestinales capaces de potenciar la respuesta de la insulina a la glucosa oral, un fenómeno conocido como el ‘efecto incretina’. Se observó que la respuesta de la insulina era significativamente mayor cuando la glucosa se administraba por vía oral en comparación con la vía intravenosa, incluso cuando los niveles de glucosa en sangre eran idénticos.
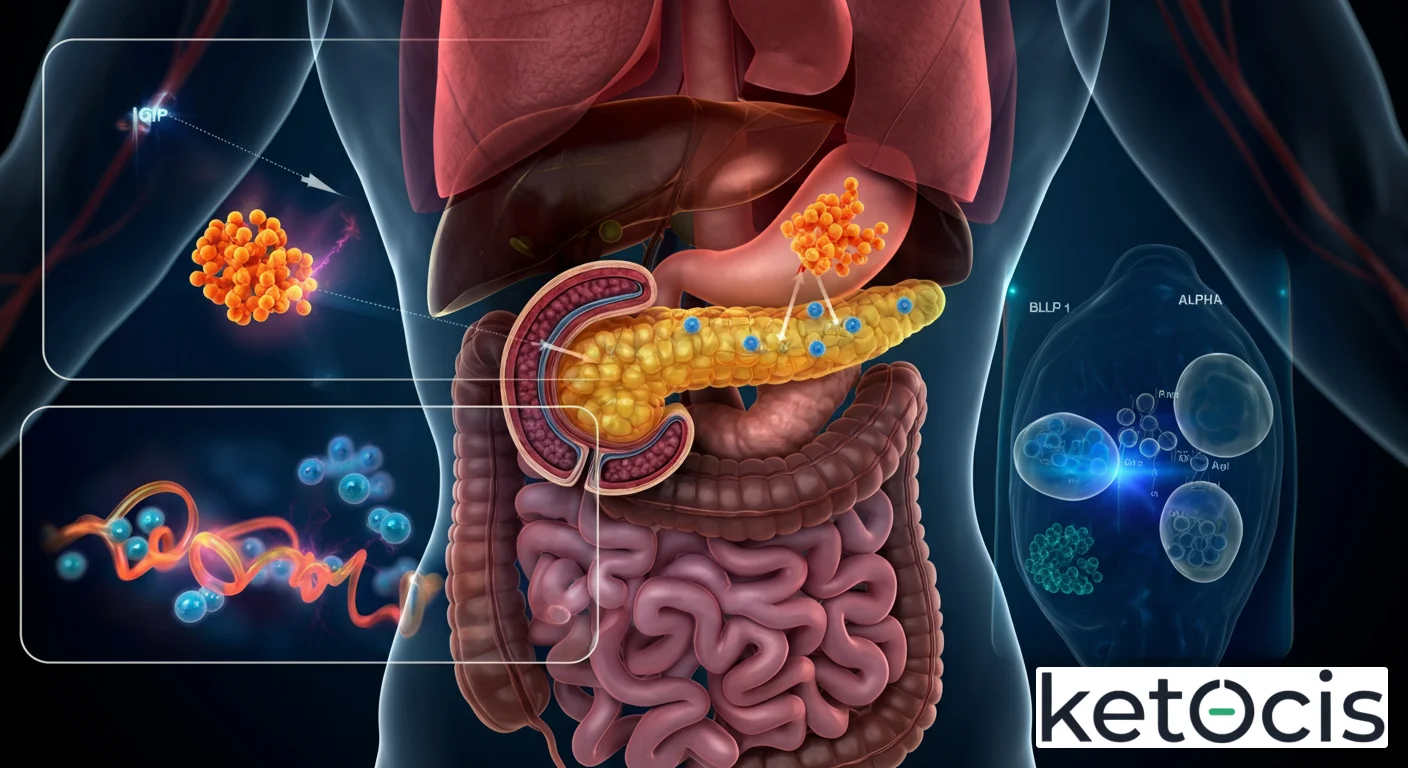
Este efecto diferencial apuntaba a la existencia de factores liberados por el intestino al contacto con los nutrientes. A principios de los años 70, se identificaron dos péptidos principales responsables de este fenómeno: el Péptido Inhibitorio Gástrico (GIP), inicialmente conocido como Péptido Liberador de Insulina dependiente de Glucosa (GLI), y el Péptido Similar al Glucagón-1 (GLP-1). Ambos péptidos son producidos por células enteroendocrinas especializadas en la mucosa intestinal, en respuesta a la presencia de alimentos.
Las Células Secretoras: K y L
El GIP es secretado principalmente por las células K, que se encuentran predominantemente en el duodeno y el yeyuno proximal del intestino delgado. Estas células son activadas por la presencia de glucosa y grasas. Por otro lado, el GLP-1 es producido por las células L, ubicadas de forma más distal en el intestino delgado (íleon) y en el colon, y su liberación es estimulada por una gama más amplia de nutrientes, incluyendo carbohidratos, grasas y proteínas. La estratégica distribución de estas células asegura una respuesta incretina coordinada a medida que los alimentos transitan por el tracto digestivo, optimizando la preparación del cuerpo para la absorción y utilización de los nutrientes.
Mecanismo de Acción: La Orquesta Metabólica Dirigida por las Incretinas
El principal y más conocido mecanismo de acción de las incretinas es su capacidad para potenciar la secreción de insulina de las células beta pancreáticas de manera dependiente de la glucosa. Esto significa que las incretinas solo estimulan la liberación de insulina cuando los niveles de glucosa en sangre están elevados, lo que minimiza el riesgo de hipoglucemia. Sin embargo, su influencia se extiende mucho más allá del páncreas, orquestando una serie de respuestas metabólicas cruciales.
Estimulación de la Secreción de Insulina Glucosa-Dependiente
Cuando los nutrientes llegan al intestino, las células K y L liberan GIP y GLP-1, respectivamente. Estas hormonas viajan a través del torrente sanguíneo hasta el páncreas, donde se unen a receptores específicos en la superficie de las células beta de los islotes de Langerhans. La unión de GLP-1 y GIP a sus receptores activa una cascada de señalización intracelular que culmina en un aumento de la liberación de insulina. Este efecto es crucial para mantener la homeostasis de la glucosa después de una comida, permitiendo que el cuerpo almacene energía de manera eficiente.
Supresión de la Secreción de Glucagón
Además de estimular la insulina, el GLP-1 ejerce un efecto supresor sobre la secreción de glucagón, otra hormona pancreática producida por las células alfa. El glucagón tiene un efecto opuesto a la insulina, elevando los niveles de glucosa en sangre al promover la gluconeogénesis y la glucogenólisis hepática. Al suprimir el glucagón postprandial, el GLP-1 ayuda a prevenir picos excesivos de glucosa, contribuyendo aún más al control glucémico.
Retraso del Vaciamiento Gástrico y Saciedad
Las incretinas, especialmente el GLP-1, también actúan sobre el tracto gastrointestinal superior, ralentizando el vaciamiento del estómago. Este retraso tiene varios beneficios: prolonga la sensación de saciedad, reduce la velocidad a la que la glucosa entra en el torrente sanguíneo desde el intestino y disminuye el apetito, lo que puede contribuir a la pérdida de peso. Esta acción es una de las razones por las que los análogos de GLP-1 son tan efectivos en el manejo de la obesidad.
Efectos a Nivel Central: Saciedad y Neuroprotección
Los receptores de GLP-1 se encuentran en varias regiones del cerebro, incluyendo el hipotálamo, que es clave en la regulación del apetito y la ingesta de alimentos. Al activar estos receptores, el GLP-1 promueve la saciedad y reduce la ingesta calórica. Investigaciones emergentes también sugieren un papel neuroprotector para el GLP-1, con estudios que exploran su potencial en enfermedades neurodegenerativas como el Alzheimer y el Parkinson, donde se ha observado una mejora en la función cognitiva y una reducción de la neuroinflamación.
Efectos Cardiovasculares y Renales
Cada vez hay más evidencia que apunta a que las incretinas, en particular el GLP-1, ejercen efectos beneficiosos directos sobre el sistema cardiovascular y los riñones. Los agonistas del receptor de GLP-1 han demostrado reducir el riesgo de eventos cardiovasculares adversos mayores en pacientes con diabetes tipo 2, así como mejorar ciertos parámetros de la función renal. Estos efectos se atribuyen a su capacidad para reducir la presión arterial, mejorar la función endotelial y disminuir la inflamación.
Proliferación y Protección de Células Beta
Un aspecto fascinante del GLP-1 es su capacidad para promover la proliferación y la supervivencia de las células beta pancreáticas. En modelos preclínicos, se ha observado que el GLP-1 puede aumentar la masa de células beta y protegerlas del daño oxidativo y la apoptosis. Este efecto podría ser crucial para preservar la función pancreática a largo plazo en condiciones como la diabetes tipo 2, donde la pérdida de células beta es un factor patogénico clave.
Principales Incretinas: GLP-1 y GIP, Similitudes y Diferencias
Aunque ambos son péptidos incretínicos con acciones superpuestas, el GLP-1 y el GIP poseen características distintivas que los hacen únicos en su contribución a la homeostasis metabólica. Su comprensión es vital para apreciar la complejidad de la regulación de la glucosa.
Péptido Similar al Glucagón-1 (GLP-1)
El GLP-1 es una hormona de 30 o 31 aminoácidos derivada del proglucagón, un precursor que también da origen al glucagón. Se libera en respuesta a la presencia de nutrientes en el íleon y el colon, actuando a través de su receptor específico, el receptor de GLP-1 (GLP-1R). Sus efectos son potentes y multifacéticos: estimulación de la secreción de insulina glucosa-dependiente, supresión del glucagón, retraso del vaciamiento gástrico, promoción de la saciedad central, efectos protectores sobre las células beta y beneficios cardiovasculares y renales. Es el más estudiado y el que ha dado lugar a la mayoría de los tratamientos basados en incretinas.
Péptido Inhibitorio Gástrico (GIP)
El GIP es un péptido de 42 aminoácidos, secretado principalmente por las células K del duodeno y el yeyuno proximal. Su liberación es particularmente sensible a la glucosa y a los triglicéridos de cadena larga. Inicialmente se le denominó ‘inhibitorio gástrico’ porque se pensaba que su principal función era inhibir la secreción de ácido gástrico y la motilidad. Aunque tiene este efecto, su rol más prominente es la estimulación de la secreción de insulina de las células beta a través del receptor de GIP (GIPR). A diferencia del GLP-1, el GIP no suprime el glucagón de forma tan consistente y sus efectos sobre el vaciamiento gástrico y la saciedad son menos pronunciados. En estados de resistencia a la insulina, la respuesta del GIP puede verse alterada o reducida.
La Diferencia en la Acción
Mientras que el GLP-1 mantiene su efecto insulinotrópico incluso en la diabetes tipo 2, la respuesta a GIP puede estar disminuida en esta condición. Esto llevó a que, durante un tiempo, se centrara la atención terapéutica casi exclusivamente en el GLP-1. Sin embargo, estudios recientes con agonistas duales de GLP-1 y GIP han reavivado el interés en el GIP, sugiriendo que la co-activación de ambos receptores podría ofrecer beneficios metabólicos superiores, especialmente en la pérdida de peso y el control glucémico, al aprovechar sinergias entre ambas vías.
Regulación y Degradación: El Papel de la DPP-4
La naturaleza potente pero efímera de las incretinas en el cuerpo es una característica clave para su función fisiológica. Una vez liberadas, tanto el GLP-1 como el GIP son rápidamente inactivados por una enzima ubicua llamada Dipeptidil Peptidasa-4 (DPP-4). Esta enzima, presente en la superficie de muchas células y también en forma soluble en la circulación, escinde dos aminoácidos del extremo N-terminal de las incretinas, generando metabolitos que son biológicamente inactivos o tienen una actividad muy reducida. La vida media del GLP-1 intacto en la circulación es de solo unos minutos, lo que garantiza que su acción sea transitoria y finamente controlada.
La rápida degradación por DPP-4 subraya la importancia de esta enzima como un punto de control fisiológico crucial. Sin embargo, esta misma característica ha sido explotada terapéuticamente. Los inhibidores de la DPP-4 son una clase de fármacos que bloquean la acción de esta enzima, prolongando la vida media de las incretinas endógenas y permitiendo que ejerzan sus efectos insulinotrópicos y glucagón-supresores durante más tiempo. Estos fármacos, como la sitagliptina o la vildagliptina, son ampliamente utilizados en el tratamiento de la diabetes tipo 2.
Biohacking Metabólico: El Poder de la Fibra y Proteína
Para optimizar la liberación endógena de incretinas como el GLP-1, incorpora fibra soluble y proteína de alta calidad en cada comida. La fibra, especialmente la presente en vegetales y legumbres, retrasa el vaciamiento gástrico y permite que los nutrientes lleguen más lentamente a las células L distales, prolongando la liberación de GLP-1. La proteína, por su parte, es un potente secretagogo de GLP-1. Un desayuno rico en proteínas, por ejemplo, puede preparar tu metabolismo para un mejor control glucémico y mayor saciedad durante el día, ¡un simple cambio con grandes beneficios!
Análogos de Incretinas y su Aplicación Clínica: Revolucionando el Tratamiento
La comprensión de la rápida degradación de las incretinas por la DPP-4 impulsó el desarrollo de fármacos que pudieran superar esta limitación y proporcionar una acción incretínica sostenida. Esto llevó a la creación de dos clases principales de medicamentos: los ya mencionados inhibidores de la DPP-4 y los agonistas del receptor de GLP-1 (AR-GLP-1), que han transformado el panorama del tratamiento de la diabetes tipo 2 y la obesidad.
Agonistas del Receptor de GLP-1 (AR-GLP-1)
Los AR-GLP-1 son péptidos diseñados para imitar la acción del GLP-1 endógeno, pero con una mayor resistencia a la degradación por la DPP-4, lo que les confiere una vida media mucho más larga. Algunos ejemplos incluyen liraglutida, semaglutida y dulaglutida. Estos fármacos se administran por inyección (aunque ya existen formulaciones orales de semaglutida) y han demostrado ser extremadamente efectivos en:
- Control glucémico: Reducen significativamente la hemoglobina glicosilada (HbA1c) al potenciar la secreción de insulina y suprimir el glucagón.
- Pérdida de peso: Gracias a sus efectos sobre la saciedad y el retraso del vaciamiento gástrico, muchos AR-GLP-1 inducen una pérdida de peso clínicamente significativa.
- Beneficios cardiovasculares y renales: Estudios a gran escala han demostrado que estos fármacos reducen el riesgo de eventos cardiovasculares mayores y ralentizan la progresión de la enfermedad renal crónica en pacientes con diabetes tipo 2.
Agonistas Duales de GLP-1 y GIP
Un avance más reciente ha sido el desarrollo de agonistas que activan tanto los receptores de GLP-1 como los de GIP. El ejemplo más notable es la tirzepatida. Este enfoque dual ha demostrado ser aún más potente en la reducción de la glucosa y, sobre todo, en la pérdida de peso, superando incluso a los AR-GLP-1 de acción única en algunos ensayos clínicos. La hipótesis es que la activación sinérgica de ambas vías incretínicas proporciona un control metabólico más completo y eficaz.
Incretinas y el Metabolismo en Cetosis/Ayuno: Adaptación y Eficiencia
Aunque las incretinas son clásicamente asociadas con la respuesta postprandial a los carbohidratos, su papel en contextos de bajo consumo de carbohidratos, como la dieta cetogénica, o durante periodos de ayuno intermitente, es igualmente relevante y, a menudo, subestimado. En estos estados metabólicos, el cuerpo se adapta para depender menos de la glucosa exógena y más de las grasas y los cuerpos cetónicos como fuente de energía.
Durante el ayuno, los niveles basales de incretinas se mantienen bajos, reflejando la ausencia de estímulos nutricionales en el intestino. Sin embargo, cuando se produce la reintroducción de alimentos tras un periodo de ayuno, la respuesta incretina puede ser particularmente aguda, lo que facilita una gestión eficiente de los nutrientes. En una dieta cetogénica, aunque la ingesta de carbohidratos es mínima, la presencia de grasas y proteínas sigue estimulando la liberación de GLP-1 y GIP. El GLP-1, en particular, sigue ejerciendo su efecto sobre la saciedad, lo cual es beneficioso para mantener la adherencia a la dieta al reducir el apetito y los antojos.
Además, la capacidad del GLP-1 para suprimir el glucagón es crucial incluso en cetosis. Aunque el glucagón es necesario para la cetogénesis, su supresión postprandial ayuda a evitar una gluconeogénesis hepática excesiva que podría elevar la glucosa en sangre y dificultar el mantenimiento de la cetosis. Las incretinas, por tanto, actúan como reguladores finos, asegurando que el cuerpo se adapte a los cambios en la disponibilidad de nutrientes de manera óptima, incluso en un estado metabólico alterado como la cetosis.
Mitos y Conceptos Erróneos sobre las Incretinas
A pesar de la creciente evidencia, persisten ciertos malentendidos sobre las incretinas que es importante aclarar para una comprensión precisa de su fisiología y terapéutica.
Mito Popular: «Las incretinas solo importan en diabéticos.»
Este es un error común. Aunque las incretinas son pilares en el tratamiento de la diabetes tipo 2, su función es fundamental en la fisiología de cualquier individuo, diabético o no. El efecto incretina es un mecanismo natural y esencial para el control de la glucosa postprandial en personas sanas. La disfunción en la producción o acción de las incretinas puede contribuir al desarrollo de la resistencia a la insulina y la diabetes, pero su presencia y actividad son vitales para la homeostasis metabólica normal. Son hormonas clave para la saciedad y el metabolismo general en individuos sanos, ayudando a prevenir picos de glucosa y a regular el apetito.
Alerta Metabólica: Riesgo de «Rebote de Peso» al Suspender Agonistas de GLP-1
Aunque los agonistas del receptor de GLP-1 son altamente efectivos para la pérdida de peso, es crucial entender que suspender abruptamente estos tratamientos puede llevar a un «rebote de peso» significativo. Esto se debe a que el medicamento suprime el apetito y ralentiza el vaciamiento gástrico; al detenerlo, estos efectos desaparecen, lo que puede resultar en un aumento del apetito y una mayor ingesta calórica. La interrupción debe ser manejada bajo supervisión médica, a menudo acompañada de cambios sostenibles en el estilo de vida para mitigar este riesgo y mantener los beneficios obtenidos.
Optimización de la Función Incretina: Estrategias de Biohacking
Más allá de las intervenciones farmacológicas, existen estrategias de estilo de vida que pueden potenciar la liberación y la acción de las incretinas endógenas, contribuyendo a una mejor salud metabólica y un control de peso más eficiente.
- Dieta Rica en Fibra: La fibra dietética, especialmente la soluble, no solo alimenta la microbiota intestinal, sino que también ralentiza la digestión y el tránsito de los alimentos, permitiendo una liberación más sostenida y prolongada de GLP-1 desde las células L distales. Incluye abundantes vegetales, frutas, legumbres y cereales integrales.
- Ingesta Adecuada de Proteínas: Las proteínas son potentes estimuladores de la liberación de GLP-1 y GIP. Incorporar fuentes de proteína de alta calidad (carne magra, pescado, huevos, lácteos, legumbres) en cada comida puede mejorar la respuesta incretina y aumentar la saciedad.
- Grasas Saludables: Aunque las grasas pueden ralentizar el vaciamiento gástrico, las grasas saludables (aguacate, aceite de oliva, frutos secos) también estimulan la liberación de GIP y GLP-1, contribuyendo a la saciedad y a una respuesta incretina equilibrada.
- Ejercicio Físico Regular: La actividad física, especialmente el ejercicio de intensidad moderada a alta, ha demostrado mejorar la sensibilidad a las incretinas y aumentar su liberación. El ejercicio aeróbico y el entrenamiento de fuerza contribuyen a una mejor homeostasis glucémica general.
- Optimización del Sueño: La privación crónica del sueño altera el equilibrio hormonal, incluyendo las hormonas que regulan el apetito y el metabolismo. Un sueño de calidad puede mejorar la sensibilidad a la insulina y la función incretina.
- Reducción del Estrés Crónico: El estrés eleva el cortisol, lo que puede impactar negativamente la sensibilidad a la insulina y la función metabólica. Técnicas de manejo del estrés como la meditación o el yoga pueden indirectamente apoyar una mejor función incretina.
- Alimentos Fermentados y Probióticos: Una microbiota intestinal saludable se asocia con una mejor producción de ácidos grasos de cadena corta, que pueden influir positivamente en la liberación de GLP-1. Incluir alimentos fermentados como el kéfir, el chucrut o el kimchi puede ser beneficioso.
Conclusión: Las Incretinas como Pilares de la Salud Metabólica
Las incretinas, particularmente el GLP-1 y el GIP, son mucho más que simples curiosidades bioquímicas; son hormonas fundamentales que orquestan una compleja red de respuestas metabólicas vitales para nuestra salud. Desde su descubrimiento, han pasado de ser meros factores intestinales a convertirse en dianas terapéuticas de vanguardia, revolucionando el manejo de la diabetes tipo 2 y la obesidad. Su capacidad para modular la secreción de insulina y glucagón, influir en la saciedad, proteger el páncreas y ofrecer beneficios cardiovasculares y neuroprotectores, las posiciona como protagonistas indiscutibles en la ciencia metabólica.
Comprender su fisiología, las estrategias para optimizar su función endógena y las innovaciones farmacológicas que las emulan, nos proporciona herramientas poderosas para abordar los desafíos de las enfermedades metabólicas modernas. En el viaje hacia una salud óptima, especialmente en el contexto de enfoques como el de Ketocis, el conocimiento sobre las incretinas no solo es fascinante, sino esencial. Nos recuerdan la intrincada sabiduría de nuestro cuerpo y el potencial que reside en comprender y apoyar sus mecanismos innatos para vivir una vida más saludable y plena.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.