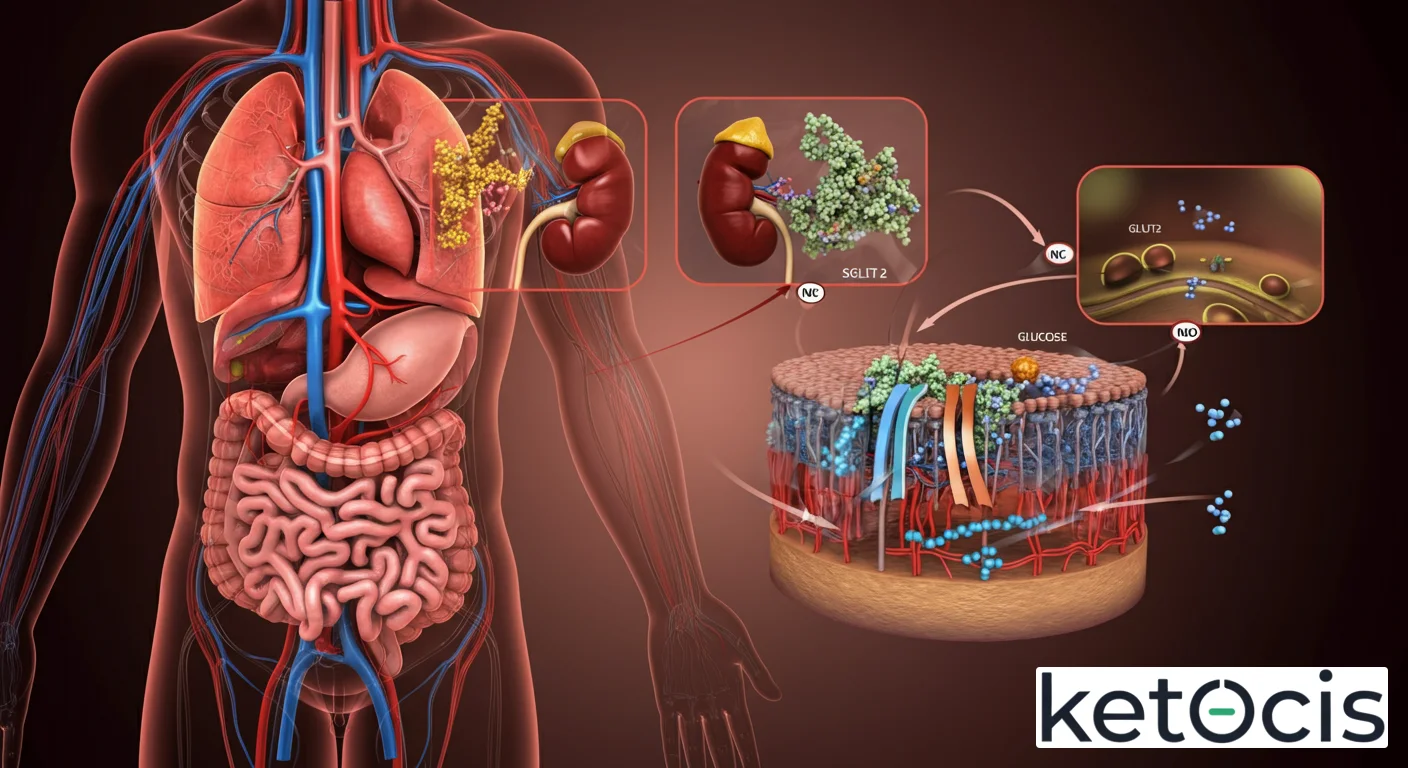
SGLT2: Transportador Renal de Glucosa y Farmacología Innovadora
Resumen Clínico Rápido
🔬 Clasificación
Cotransportador de sodio-glucosa
⚙️ Función
Reabsorción de glucosa en riñón
📋 Impacto
Control glucémico, cardiovascular, renal
¿Qué es el Transportador de Glucosa SGLT2? Una Guía Definitiva para el Glosario Ketocis
En el vasto y complejo universo de la fisiología humana, la gestión de la glucosa sanguínea representa una de las tareas más críticas y finamente orquestadas. Cada célula depende de ella como fuente de energía, pero un exceso o defecto puede desencadenar cascadas patológicas. En el epicentro de esta regulación, particularmente en el ámbito renal, reside una proteína fascinante y de profunda relevancia clínica: el cotransportador de sodio-glucosa tipo 2, más conocido como SGLT2.
Este transportador, ubicado estratégicamente en los túbulos renales, desempeña un papel primordial en la reabsorción de glucosa filtrada, asegurando que este valioso combustible no se pierda innecesariamente en la orina. Su función es tan vital que su disfunción o modulación farmacológica tiene implicaciones monumentales para enfermedades metabólicas como la diabetes mellitus tipo 2 y, sorprendentemente, para la salud cardiovascular y renal en general. En esta guía enciclopédica, desentrañaremos la estructura, función, implicaciones patológicas y el revolucionario impacto terapéutico del SGLT2, ofreciendo una perspectiva integral para el glosario Ketocis.
Resumen Clínico: Puntos Clave del SGLT2
- El SGLT2 es el principal cotransportador de sodio-glucosa en el túbulo contorneado proximal del riñón, responsable de reabsorber el 90% de la glucosa filtrada.
- Su función es esencial para mantener la glucemia, evitando la pérdida de energía a través de la orina en condiciones fisiológicas.
- En la diabetes tipo 2, la actividad del SGLT2 puede aumentar, contribuyendo a la hiperglucemia al recapturar excesivamente la glucosa.
- Los inhibidores de SGLT2 (gliflozinas) son una clase de fármacos que bloquean este transportador, induciendo glucosuria y ofreciendo beneficios cardiovasculares y renales más allá del control glucémico.
- La modulación del SGLT2 tiene implicaciones en estados de ayuno y cetosis, afectando el balance energético y la excreción de glucosa.
Origen y Localización del SGLT2: Un Guardián Renal de la Glucosa
El SGLT2 es una proteína de membrana integral codificada por el gen SLC5A2. Su expresión es predominantemente renal, localizándose de manera crucial en el segmento S1 y S2 del túbulo contorneado proximal de la nefrona. Esta ubicación no es aleatoria; es la primera sección del túbulo renal que la orina filtrada atraviesa después del glomérulo, lo que permite una reabsorción eficiente y temprana de la glucosa antes de que pueda avanzar por la nefrona y potencialmente perderse.
Desde una perspectiva evolutiva, la existencia de transportadores de glucosa de alta capacidad como el SGLT2 es un testimonio de la importancia de conservar la energía. En entornos donde la disponibilidad de alimentos era incierta, la pérdida de glucosa a través de la orina habría sido un lujo metabólico inaceptable. El SGLT2, junto con su contraparte de menor capacidad pero mayor afinidad, el SGLT1 (presente también en el intestino y en el segmento S3 del túbulo renal), asegura que casi el 100% de la glucosa filtrada por los riñones sea devuelta a la circulación sanguínea, siempre y cuando los niveles de glucosa no excedan la capacidad máxima de transporte renal, conocida como umbral renal de glucosa.
Que los SGLT2i 'curan' la diabetes o permiten comer carbohidratos sin control.
Los SGLT2i gestionan la glucemia y ofrecen protección orgánica, pero no eliminan la necesidad de un estilo de vida saludable ni revierten la patología subyacente de la diabetes. Su efecto es de manejo y protección, no de cura.
Fisiología Molecular y Mecanismo de Acción: El Baile del Sodio y la Glucosa
El SGLT2 es un miembro de la familia de cotransportadores de sodio-glucosa (SGLT), que se caracteriza por su capacidad para transportar glucosa en contra de su gradiente de concentración, utilizando la energía derivada del gradiente electroquímico del sodio. Este es un ejemplo clásico de transporte activo secundario.
El mecanismo es el siguiente: las bombas de sodio-potasio (Na+/K+-ATPasa) en la membrana basolateral de las células tubulares renales bombean activamente el sodio fuera de la célula hacia el intersticio, creando un gradiente de concentración de sodio bajo dentro de la célula y alto en la luz tubular. El SGLT2 aprovecha este gradiente. Cuando el sodio se une al SGLT2 en la superficie apical (lumen tubular), induce un cambio conformacional que aumenta la afinidad del transportador por la glucosa. Una vez que la glucosa se une, el transportador sufre otro cambio conformacional, liberando tanto el sodio como la glucosa dentro de la célula tubular.
Es importante destacar que el SGLT2 cotransporta una molécula de sodio por cada molécula de glucosa (relación 1:1), lo que lo distingue del SGLT1, que tiene una estequiometría de 2 sodios por 1 glucosa y una mayor afinidad por la glucosa, aunque una menor capacidad de transporte global. Una vez dentro de la célula, la glucosa es transportada al intersticio y luego a la sangre a través de transportadores de glucosa facilitada (GLUT), principalmente GLUT2, ubicados en la membrana basolateral.
Este sistema de transporte de dos pasos (SGLT en la membrana apical y GLUT en la basolateral) es increíblemente eficiente, permitiendo que el riñón reabsorba aproximadamente 180 gramos de glucosa al día en un individuo sano, virtualmente toda la glucosa filtrada.
SGLT2 en la Homeostasis de la Glucosa y Patologías: Un Actor Clave en la Diabetes
En condiciones fisiológicas, el SGLT2 es un héroe silencioso que previene la glucosuria, es decir, la presencia de glucosa en la orina. Sin embargo, en estados patológicos como la diabetes mellitus tipo 2, su papel se vuelve perjudicial. En pacientes diabéticos, caracterizados por niveles crónicamente elevados de glucosa en sangre (hiperglucemia), el SGLT2 puede experimentar una sobreexpresión y/o un aumento de su actividad.
Este aumento compensatorio en la reabsorción de glucosa por el SGLT2 agrava la hiperglucemia, ya que el riñón, en lugar de excretar el exceso de glucosa, lo devuelve a la circulación. Esto crea un círculo vicioso que contribuye a mantener los niveles elevados de glucosa, exacerbando la resistencia a la insulina y el daño a los tejidos. La comprensión de este mecanismo ha sido fundamental para el desarrollo de una nueva y revolucionaria clase de fármacos.
Inhibidores de SGLT2: Una Revolución Farmacológica con Beneficios Multiorgánicos
La identificación del SGLT2 como un contribuyente clave a la hiperglucemia en la diabetes tipo 2 abrió una nueva avenida terapéutica. Los inhibidores de SGLT2, comúnmente conocidos como gliflozinas (como empagliflozina, dapagliflozina y canagliflozina), son fármacos que bloquean selectivamente la función de este transportador.
Al inhibir el SGLT2, estos medicamentos reducen drásticamente la reabsorción renal de glucosa, provocando una excreción significativa de glucosa en la orina (glucosuria). Esto tiene varios efectos beneficiosos:
- Control Glucémico: La eliminación de glucosa por la orina reduce directamente los niveles de glucosa en sangre.
- Pérdida de Peso: La glucosa excretada representa una pérdida calórica (aproximadamente 200-300 kcal/día), lo que contribuye a una modesta pero sostenida pérdida de peso.
- Reducción de la Presión Arterial: La glucosuria induce una diuresis osmótica y natriuresis (excreción de sodio), lo que lleva a una reducción de la volemia y, en consecuencia, de la presión arterial.
- Beneficios Cardiovasculares: Más allá del control glucémico, los estudios clínicos han demostrado que las gliflozinas reducen significativamente el riesgo de eventos cardiovasculares adversos mayores (MACE), hospitalizaciones por insuficiencia cardíaca y mortalidad cardiovascular en pacientes con diabetes tipo 2 y enfermedad cardiovascular establecida o factores de riesgo.
- Beneficios Renales: Las gliflozinas también han demostrado ralentizar la progresión de la enfermedad renal crónica (ERC) en pacientes con y sin diabetes, ofreciendo un efecto nefroprotector.
Estos beneficios multiorgánicos han posicionado a los inhibidores de SGLT2 como pilares fundamentales en el tratamiento de la diabetes tipo 2, la insuficiencia cardíaca y la enfermedad renal crónica, redefiniendo las estrategias terapéuticas.
Biohacking Metabólico: SGLT2 y la Eficiencia Cetogénica
En un estado de cetosis o ayuno prolongado, el cuerpo optimiza la conservación de glucosa. Curiosamente, la actividad del SGLT2 tiende a disminuir en respuesta a la reducción de la carga de glucosa filtrada y a la adaptación metabólica general. Esto significa que, en un contexto de dieta cetogénica o ayuno intermitente, el riñón naturalmente retiene menos glucosa de la que filtraría en una dieta rica en carbohidratos, contribuyendo a la eficiencia metabólica. Algunos estudios sugieren que la presencia de cuerpos cetónicos puede, en ciertas condiciones, influir indirectamente en la regulación de la expresión de transportadores renales, aunque el mecanismo exacto y la relevancia clínica en individuos sanos requieren mayor investigación. Comprender esta dinámica subraya cómo las adaptaciones renales son parte integral de nuestra capacidad para prosperar en diferentes estados metabólicos.
SGLT2 y el Metabolismo Cetogénico/Ayuno: Una Adaptación Renal
La relación entre el SGLT2 y los estados metabólicos como la cetosis o el ayuno es intrigante. Durante el ayuno prolongado o una dieta cetogénica estricta, la ingesta de carbohidratos es mínima, lo que resulta en niveles bajos de glucosa en sangre y una producción endógena de glucosa (gluconeogénesis) que, aunque activa, es limitada.
En estas condiciones, la cantidad de glucosa que llega al riñón para ser filtrada es significativamente menor. Por lo tanto, la carga de trabajo del SGLT2 disminuye. Si bien la expresión o la actividad intrínseca del SGLT2 no se apaga, su relevancia funcional en la reabsorción de glucosa se reduce proporcionalmente a la menor disponibilidad de sustrato. Esto contribuye a la conservación de la poca glucosa disponible y a la optimización del uso de cuerpos cetónicos como fuente de energía.
Además, es importante considerar que el riñón no solo reabsorbe glucosa, sino también cuerpos cetónicos. Aunque los transportadores específicos para cuerpos cetónicos son diferentes (monocarboxilato transportadores, MCTs), el ambiente metabólico general influenciado por la actividad del SGLT2 y los niveles de glucosa puede tener efectos indirectos. Por ejemplo, la natriuresis inducida por los inhibidores de SGLT2 puede influir en el balance de líquidos y electrolitos, lo cual es de particular interés en individuos en cetosis que ya pueden experimentar cambios en el balance hídrico y electrolítico.
Implicaciones y Consideraciones Clínicas: Navegando los Riesgos
A pesar de sus notables beneficios, el uso de inhibidores de SGLT2 no está exento de consideraciones. Los efectos adversos más comunes incluyen infecciones del tracto urinario y micóticas genitales, debido a la presencia de glucosa en la orina que favorece el crecimiento bacteriano y fúngico. También puede ocurrir deshidratación o hipotensión, especialmente en pacientes ancianos o que toman diuréticos, debido a la diuresis osmótica.
Una preocupación particular, especialmente relevante para el público interesado en el metabolismo cetogénico, es el riesgo de cetoacidosis diabética euglucémica (CADe). Aunque rara, esta condición se caracteriza por una cetoacidosis significativa (niveles elevados de cuerpos cetónicos y acidosis metabólica) con niveles de glucosa en sangre que no están marcadamente elevados (a menudo por debajo de 250 mg/dL), lo que puede dificultar su diagnóstico. Esto ocurre más frecuentemente en pacientes con diabetes tipo 1 que usan SGLT2i off-label, o en pacientes con diabetes tipo 2 en situaciones de estrés metabólico (enfermedad aguda, cirugía, restricción calórica severa, o consumo excesivo de alcohol) o en dietas muy bajas en carbohidratos, donde la producción de cuerpos cetónicos ya es elevada y la falta de glucosa en orina enmascara la cetoacidosis.
Alerta Metabólica: Cetoacidosis Euglucémica y SGLT2i
La cetoacidosis diabética euglucémica (CADe) es un riesgo serio, aunque infrecuente, asociado al uso de inhibidores de SGLT2 (gliflozinas). Se caracteriza por una cetoacidosis metabólica severa con niveles de glucosa en sangre solo moderadamente elevados o incluso normales, lo que puede retrasar el diagnóstico. Este riesgo es mayor en pacientes con diabetes tipo 1, así como en aquellos con diabetes tipo 2 bajo estrés fisiológico (cirugía, enfermedad grave, ayuno prolongado) o que siguen dietas muy bajas en carbohidratos o cetogénicas. La combinación de una reducción en la secreción de insulina (o deficiencia), aumento de hormonas contrarreguladoras y el bloqueo de la reabsorción de glucosa por SGLT2i puede desviar el metabolismo hacia una producción excesiva de cuerpos cetónicos. Es crucial que los pacientes que tomen gliflozinas y consideren dietas cetogénicas o ayunos prolongados consulten a su médico para evaluar el riesgo y recibir orientación adecuada.
La investigación continúa explorando nuevas aplicaciones y comprendiendo mejor los mecanismos subyacentes de los SGLT2. Desde su papel en la protección contra el daño miocárdico y renal hasta su potencial impacto en otras enfermedades metabólicas, el SGLT2 sigue siendo un foco de intenso estudio.
Conclusión: El SGLT2, un Pilar de la Salud Metabólica
El transportador de glucosa SGLT2, inicialmente reconocido por su papel en la reabsorción renal de glucosa, ha emergido como una diana terapéutica de inmensa importancia. Su modulación farmacológica a través de los inhibidores de SGLT2 ha transformado el panorama del tratamiento de la diabetes tipo 2, la insuficiencia cardíaca y la enfermedad renal crónica, ofreciendo beneficios que van mucho más allá del simple control glucémico.
Comprender el SGLT2 no es solo entender una proteína renal, sino desentrañar una pieza fundamental del rompecabezas de la homeostasis energética y la salud metabólica. Su estudio nos recuerda la intrincada sabiduría del cuerpo humano y cómo, al comprender sus mecanismos más profundos, podemos desarrollar estrategias para optimizar la salud y combatir algunas de las enfermedades más prevalentes de nuestro tiempo.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.