Receptor P2X7: Guía Definitiva y Rol en Inflamación y Cetosis
Resumen Clínico Rápido
🔬 Clasificación
Canal iónico ligando-dependiente (P2X)
⚙️ Función Principal
Sensor de ATP extracelular, mediador de inflamación
📋 Activador Clave
ATP extracelular
¿Qué es el Receptor Purinérgico P2X7? La Puerta de la Inflamación Celular
En el vasto y complejo universo de la señalización celular, existen moléculas que actúan como guardianes y mensajeros, traduciendo señales externas en respuestas biológicas cruciales. Entre ellas, el receptor purinérgico P2X7 emerge como una entidad de profundo interés biomédico, un canal iónico activado por ATP extracelular que desempeña un papel central en la modulación de la inflamación, la inmunidad y una miríada de procesos fisiológicos y patológicos. Su estudio ha desvelado una intrincada red de interacciones que lo posicionan como una diana terapéutica prometedora para diversas afecciones, desde enfermedades autoinmunes hasta trastornos neurodegenerativos y el cáncer.
Este receptor, miembro de la familia de receptores P2X, es una proteína transmembrana que se expresa predominantemente en células del sistema inmune, como macrófagos, monocitos y microglía, pero también en otras estirpes celulares como osteoclastos, queratinocitos y células endoteliales. Su activación por altas concentraciones de adenosín trifosfato (ATP) en el espacio extracelular no solo regula el flujo de iones, sino que también inicia una cascada de eventos que pueden llevar a la liberación de potentes mediadores proinflamatorios, la apoptosis celular y la remodelación tisular. Comprender la fisiología molecular del P2X7 es fundamental para desentrañar los mecanismos subyacentes de muchas enfermedades y desarrollar estrategias de intervención innovadoras.
Resumen Clínico: Puntos Clave del Receptor P2X7
-
Punto clave 1: El receptor P2X7 es un canal iónico activado por ATP extracelular, crucial para la señalización de peligro y la respuesta inflamatoria.
-
Punto clave 2: Su activación induce la liberación de citocinas proinflamatorias como IL-1β e IL-18, y está implicado en la activación del inflamasoma NLRP3.
-
Punto clave 3: Se expresa ampliamente en células inmunes y no inmunes, siendo una diana terapéutica potencial en enfermedades autoinmunes, neurodegenerativas, cáncer y trastornos metabólicos.
Estructura y Clasificación del Receptor P2X7
Los receptores purinérgicos son un grupo diverso de proteínas que responden a nucleótidos y nucleósidos purínicos, como el ATP, ADP, UTP y adenosina. Se dividen en dos familias principales: los receptores P1 (para adenosina) y los receptores P2 (para ATP y otros nucleótidos). Los receptores P2, a su vez, se subdividen en receptores P2Y (acoplados a proteínas G) y receptores P2X (canales iónicos ligando-dependientes). El P2X7 es uno de los siete miembros de la familia P2X, caracterizado por su estructura trimérica y su capacidad única para formar poros de gran tamaño.
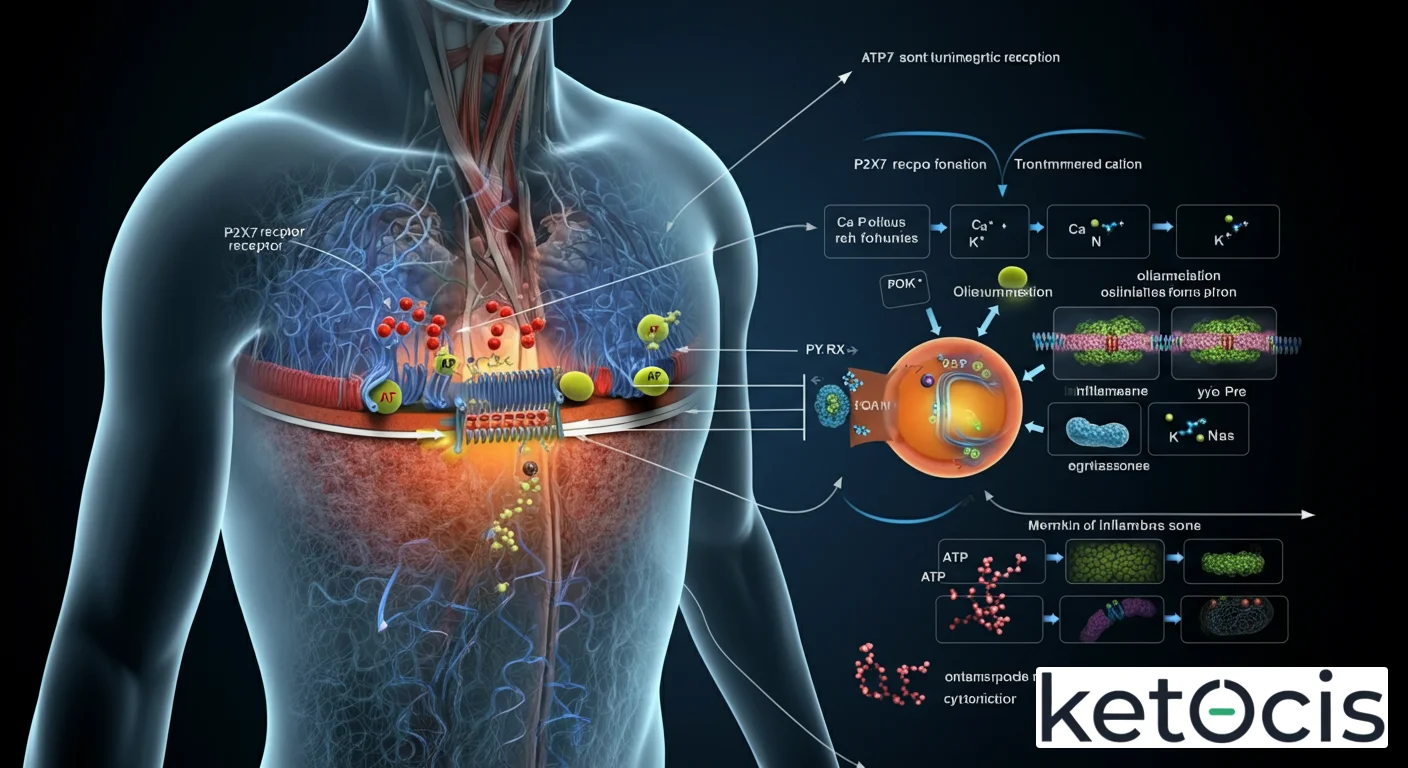
Cada subunidad del receptor P2X7 consta de dos dominios transmembrana, un bucle extracelular grande que contiene los sitios de unión al ATP, y dominios intracelulares N- y C-terminales. La cola C-terminal intracelular del P2X7 es notablemente más larga que la de otros receptores P2X, y es fundamental para sus funciones distintivas, incluida la interacción con proteínas adaptadoras y la modulación de la señalización intracelular. La oligomerización de tres subunidades forma un canal central permeable a cationes monovalentes como iones sodio (Na+) y potasio (K+), y, bajo estimulación prolongada o intensa, a iones divalentes como el calcio (Ca2+) y moléculas de hasta 900 Da.
El P2X7 solo tiene un papel proinflamatorio.
Aunque predominantemente proinflamatorio, el P2X7 puede tener roles duales dependiendo del contexto celular y tisular, incluso mediando la muerte celular antitumoral o siendo neuroprotector en ciertas condiciones.
Mecanismo de Acción: La Danza del ATP y el Poro
El mecanismo de acción del receptor P2X7 es fascinante y multifacético, iniciándose con la detección de ATP extracelular, una señal de ‘peligro’ o daño celular. En condiciones fisiológicas normales, la concentración de ATP extracelular es baja. Sin embargo, en situaciones de estrés, lesión tisular, infección o inflamación, las células dañadas o activadas liberan ATP al espacio extracelular, donde actúa como un potente DAMP (patrón molecular asociado a daño). Es este ATP extracelular el ligando primario que activa el P2X7.
Cuando el ATP se une a los sitios específicos en el bucle extracelular del P2X7, induce un cambio conformacional en el receptor. Inicialmente, este cambio abre un canal pequeño que permite el flujo rápido de iones Na+ y Ca2+ hacia el interior de la célula y la salida de iones K+ al exterior. Este movimiento iónico provoca una despolarización de la membrana y un aumento transitorio de Ca2+ intracelular, lo que activa diversas vías de señalización. Sin embargo, la característica más distintiva del P2X7 es su capacidad, bajo estimulación prolongada o con altas concentraciones de ATP, para transicionar a un estado de poro de mayor tamaño. Este poro de gran conductancia permite el paso bidireccional de moléculas de hasta 900 Da, como los colorantes fluorescentes (por ejemplo, bromuro de etidio) e incluso péptidos pequeños.
La formación de este poro tiene profundas consecuencias celulares. La entrada masiva de Ca2+ y la salida de K+ son eventos cruciales para la activación de complejos multiproteicos conocidos como inflamasomas, particularmente el inflamasoma NLRP3. La activación de NLRP3 conduce a la escisión de la procaspasa-1 en caspasa-1 activa, la cual, a su vez, procesa las pro-citocinas proinflamatorias interleucina-1 beta (IL-1β) e interleucina-18 (IL-18) en sus formas maduras y biológicamente activas, que son luego liberadas al exterior celular. Además, la activación del P2X7 puede inducir la liberación de microvesículas, la autofagia, la fagocitosis y, en algunos contextos, la muerte celular programada (piropoptosis o apoptosis).
Roles Fisiológicos Multifacéticos
El receptor P2X7 no es un actor solitario; su ubicuidad y capacidad para modular respuestas celulares lo convierten en un componente clave en múltiples sistemas fisiológicos. Su papel es particularmente prominente en la interfaz entre la inmunidad y la inflamación.
El Guardián del Sistema Inmune
En el sistema inmune, el P2X7 es un sensor crítico de peligro. Se expresa abundantemente en macrófagos, monocitos, células dendríticas, linfocitos y microglía. En estas células, su activación por ATP extracelular es un evento central en la iniciación y propagación de la respuesta inflamatoria. Más allá de la liberación de IL-1β e IL-18, el P2X7 contribuye a la maduración de las células dendríticas, la diferenciación de linfocitos T y B, y la eliminación de patógenos intracelulares. Una disfunción en la regulación de P2X7 puede llevar a una inflamación crónica o a una respuesta inmune deficiente, lo que subraya su importancia en la homeostasis inmune.
Modulador del Sistema Nervioso
En el sistema nervioso central (SNC) y periférico, el P2X7 se encuentra en neuronas, astrocitos, oligodendrocitos y, especialmente, en la microglía, las células inmunes residentes del cerebro. Aquí, su activación juega un papel dual. Por un lado, puede contribuir a la neuroinflamación y la muerte neuronal en condiciones patológicas como la isquemia, la enfermedad de Alzheimer, la enfermedad de Parkinson y el dolor neuropático. Por otro lado, en ciertos contextos, su modulación puede ser neuroprotectora o participar en la plasticidad sináptica. La complejidad de su función en el SNC lo convierte en una diana desafiante pero prometedora para el tratamiento de trastornos neurológicos.
Regulador del Metabolismo Óseo
El P2X7 también tiene un rol significativo en el tejido óseo, donde se expresa en osteoclastos y osteoblastos. En los osteoclastos, células responsables de la resorción ósea, la activación del P2X7 promueve su diferenciación, fusión y actividad resorptiva. Esto sugiere que el P2X7 podría estar implicado en enfermedades óseas como la osteoporosis, donde un desequilibrio entre la formación y la resorción ósea conduce a la fragilidad ósea. La modulación de P2X7 podría ofrecer una nueva vía para el tratamiento de estas afecciones.
Implicaciones en la Oncología
En el ámbito del cáncer, el P2X7 presenta un papel paradójico. En algunos tipos de cáncer, su activación puede inducir la muerte de células tumorales, sugiriendo un rol antitumoral. Sin embargo, en otros contextos, su expresión o activación promueve la proliferación, migración e invasión de células cancerosas, y facilita la supervivencia tumoral al modular el microambiente inmune. Esta dualidad hace que el P2X7 sea una diana compleja en la oncología, requiriendo una comprensión detallada de su contexto específico en cada tipo de tumor.
Biohacking del P2X7 y la Salud Celular: La Dieta como Modulador
¿Sabías que tu alimentación podría influir en la actividad de tu receptor P2X7? Investigaciones emergentes sugieren que ciertos componentes dietéticos, como los polifenoles presentes en frutas, verduras y té verde, poseen propiedades antiinflamatorias que podrían actuar indirectamente modulando las vías de señalización asociadas al P2X7. Al reducir el estrés oxidativo y la liberación de DAMPs, una dieta rica en antioxidantes podría atenuar la activación excesiva del P2X7, contribuyendo a una menor inflamación sistémica y favoreciendo la salud celular. Considera una ingesta abundante de alimentos vegetales ricos en quercetina, resveratrol o curcumina para optimizar la respuesta inflamatoria de tu organismo.
P2X7 en el Contexto de la Cetosis y el Ayuno
Para el Glosario Ketocis, es imperativo explorar la interconexión entre el receptor P2X7 y los estados metabólicos como la cetosis y el ayuno. Ambos estados son conocidos por inducir cambios significativos en el metabolismo energético y la respuesta inflamatoria, lo que abre la puerta a una posible modulación del P2X7.
Modulación de la Inflamación Metabólica
La cetosis nutricional, caracterizada por la producción de cuerpos cetónicos como el beta-hidroxibutirato (BHB), ha demostrado tener efectos antiinflamatorios potentes. Curiosamente, el BHB ha sido identificado como un inhibidor endógeno del inflamasoma NLRP3, la misma vía que se activa aguas abajo del P2X7. Al suprimir directamente la activación de NLRP3, el BHB podría indirectamente atenuar las consecuencias proinflamatorias de una activación excesiva del P2X7, incluso si el receptor mismo sigue siendo activado por el ATP. Esto sugiere un mecanismo por el cual la cetosis podría mitigar la inflamación crónica asociada a la activación del P2X7 en enfermedades metabólicas.
El ayuno intermitente y prolongado también reduce la inflamación sistémica y promueve la autofagia, un proceso de limpieza celular que puede eliminar componentes celulares dañados que, de otra manera, liberarían ATP y activarían el P2X7. Al reducir la carga de daño celular y la disponibilidad de ATP extracelular, el ayuno podría indirectamente desensibilizar o reducir la activación basal del P2X7, contribuyendo a un estado de menor inflamación y mayor resiliencia celular. La autofagia, inducida por el ayuno, es clave para mantener la integridad celular y prevenir la liberación de DAMPs.
Interacción con Cuerpos Cetónicos
Más allá de la supresión del inflamasoma NLRP3, algunos estudios sugieren que los cuerpos cetónicos podrían tener efectos más directos sobre la función del P2X7. Aunque la investigación es aún incipiente, es plausible que los cambios en el estado redox celular o la disponibilidad de sustratos energéticos durante la cetosis puedan alterar la expresión o la sensibilidad del P2X7. La hipótesis es que un entorno metabólico favorable, como el que se observa en la cetosis, podría modular la respuesta proinflamatoria del P2X7, convirtiéndolo en un objetivo indirecto pero significativo de las intervenciones dietéticas.
Potencial Terapéutico
Entender cómo la cetosis y el ayuno influyen en el P2X7 abre nuevas vías para el biohacking y la optimización de la salud. Si la dieta cetogénica o el ayuno pueden modular la actividad del P2X7 y sus vías de señalización asociadas, esto podría tener implicaciones profundas para el tratamiento y la prevención de enfermedades inflamatorias crónicas, neurodegenerativas y metabólicas, donde el P2X7 juega un papel central. La modulación de la inflamación purinérgica a través de estrategias dietéticas es un campo de investigación emergente con un gran potencial.
Antagonistas y Estrategias Terapéuticas
Dada la implicación del P2X7 en numerosas patologías, el desarrollo de moduladores farmacológicos ha sido un área activa de investigación. Los antagonistas del P2X7 son moléculas diseñadas para bloquear la unión del ATP al receptor o para inhibir su función de canal, atenuando así las respuestas proinflamatorias y citotóxicas.
Se han desarrollado varios antagonistas del P2X7, algunos de los cuales han avanzado a ensayos clínicos. Ejemplos incluyen el A740003, el AZD9056 y el GSK1482160, que han mostrado promesas en modelos preclínicos de dolor crónico, artritis reumatoide y enfermedad de Crohn. Sin embargo, la complejidad de la señalización del P2X7 y su papel dual en diferentes tejidos y enfermedades ha presentado desafíos en el desarrollo de fármacos, incluyendo la necesidad de selectividad y la evitación de efectos secundarios no deseados.
Variantes Genéticas y Farmacogenómica
Además de los enfoques farmacológicos, las variaciones genéticas en el gen P2RX7 pueden influir significativamente en la función del receptor. Polimorfismos de un solo nucleótido (SNPs) en el gen P2RX7 se han asociado con una mayor o menor actividad del receptor y con la susceptibilidad a diversas enfermedades, incluyendo la tuberculosis, la enfermedad de Crohn, la depresión y la osteoporosis. La farmacogenómica, el estudio de cómo los genes de una persona afectan su respuesta a los medicamentos, es crucial para personalizar las terapias dirigidas al P2X7, asegurando que los tratamientos sean lo más efectivos y seguros posible para cada individuo.
¡Alerta Metabólica! El Peligro de la Inflamación Crónica y el P2X7
Es un error común subestimar el impacto de la inflamación crónica de bajo grado en la salud general. La activación sostenida del receptor P2X7, a menudo por niveles elevados de ATP extracelular derivados del daño celular o estrés metabólico (como el que se observa en dietas ricas en ultraprocesados y azúcares), puede perpetuar un ciclo inflamatorio dañino. Este estado de inflamación crónica no solo agota los recursos del cuerpo, sino que también es un factor subyacente clave en el desarrollo y progresión de enfermedades como la resistencia a la insulina, la diabetes tipo 2, enfermedades cardiovasculares y neurodegeneración. Ignorar las señales de inflamación o no adoptar un estilo de vida antiinflamatorio puede llevar a consecuencias metabólicas graves y a largo plazo.
Impacto Clínico y Enfermedades Asociadas
La relevancia clínica del P2X7 se extiende a un amplio espectro de enfermedades, lo que lo convierte en un objetivo terapéutico de gran interés.
Enfermedades Autoinmunes e Inflamatorias
La sobreactivación del P2X7 es un factor clave en enfermedades inflamatorias crónicas como la artritis reumatoide, la enfermedad inflamatoria intestinal (enfermedad de Crohn y colitis ulcerosa) y la psoriasis. En estas condiciones, la activación del P2X7 contribuye a la producción excesiva de citocinas proinflamatorias y al daño tisular. La inhibición del P2X7 ha demostrado ser eficaz en modelos animales de estas enfermedades, lo que sugiere un potencial terapéutico significativo.
Trastornos Neurodegenerativos y Dolor Crónico
En el SNC, el P2X7 está implicado en la patogénesis de enfermedades como el Alzheimer, el Parkinson y la esclerosis múltiple, donde la neuroinflamación mediada por la microglía juega un papel central. La modulación de P2X7 podría ofrecer estrategias para reducir la inflamación y proteger las neuronas. Además, el P2X7 contribuye a la sensibilización de las vías del dolor, siendo un objetivo prometedor para el tratamiento del dolor neuropático crónico y el dolor inflamatorio.
Síndrome Metabólico y Diabetes
La inflamación crónica de bajo grado es una característica central del síndrome metabólico y la diabetes tipo 2. El P2X7, al mediar la liberación de IL-1β, contribuye a la disfunción de las células beta pancreáticas y a la resistencia a la insulina en tejidos periféricos. La inhibición del P2X7 podría mejorar la sensibilidad a la insulina y proteger las células pancreáticas, ofreciendo una nueva vía para el manejo de estas enfermedades metabólicas.
Cáncer
Como se mencionó anteriormente, el papel del P2X7 en el cáncer es complejo y bidireccional. En algunos tumores, la activación de P2X7 puede promover la muerte celular, mientras que en otros, su expresión elevada se asocia con la progresión tumoral y la metástasis. La comprensión de estos mecanismos es fundamental para desarrollar terapias dirigidas al P2X7 en el contexto oncológico, quizás utilizando su activación para inducir la muerte de células cancerosas o su inhibición para frenar la metástasis.
Conclusión y Perspectivas Futuras
El receptor purinérgico P2X7 es mucho más que un simple canal iónico; es un sensor molecular crucial en la intersección de la inflamación, la inmunidad y el metabolismo. Su capacidad para traducir señales de peligro extracelulares en poderosas respuestas celulares lo convierte en un actor central en la homeostasis y la patogénesis de una amplia gama de enfermedades.
La investigación continua sobre el P2X7 no solo profundiza nuestra comprensión de los mecanismos moleculares subyacentes a la enfermedad, sino que también abre nuevas avenidas para el desarrollo de terapias innovadoras. La modulación farmacológica, la comprensión de sus variantes genéticas y la exploración de cómo factores del estilo de vida, como la dieta cetogénica y el ayuno, pueden influir en su actividad, representan frentes prometedores en la búsqueda de tratamientos más efectivos y personalizados. El P2X7, sin duda, seguirá siendo un punto focal en la investigación biomédica, ofreciendo una ventana hacia nuevas estrategias para combatir algunas de las enfermedades más desafiantes de nuestro tiempo.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.