Vía de Señalización Notch: Guía Definitiva de Fisiología y Rol en Salud
Resumen Clínico Rápido
🔬 Clasificación
Vía de comunicación célula-célula
⚙️ Función Principal
Determinación de destino celular
📋 Impacto Clínico
Desarrollo, homeostasis, cáncer
¿Qué es la Vía de Señalización Notch? Una Guía Definitiva para el Glosario Ketocis
En el intrincado universo de la biología celular, donde miles de millones de células interactúan y se coordinan para formar organismos complejos, existen mecanismos de comunicación tan fundamentales que su descubrimiento y comprensión han transformado nuestra visión de la vida misma. Entre estos, la vía de señalización Notch emerge como un paradigma de interacción célula-célula directa, un sistema maestro que orquesta decisiones cruciales sobre el destino de cada célula. Desde la mosca de la fruta hasta el ser humano, esta vía evolutivamente conservada es indispensable para el desarrollo embrionario, el mantenimiento de tejidos adultos y la homeostasis, regulando procesos tan diversos como la neurogénesis, la angiogénesis y la diferenciación de células madre. Su desregulación, por otro lado, se asocia con una plétora de patologías, incluyendo diversos tipos de cáncer y trastornos del desarrollo. Comprender Notch no es solo adentrarse en la mecánica molecular, sino desentrañar uno de los pilares que sustentan la arquitectura y función de la vida pluricelular.
Resumen Clínico
- La vía Notch es un sistema de comunicación célula-célula directa esencial para la toma de decisiones sobre el destino celular.
- Regula procesos biológicos fundamentales como el desarrollo embrionario, la homeostasis tisular y la diferenciación de células madre.
- Su desregulación está implicada en diversas enfermedades, incluyendo el cáncer y trastornos del desarrollo, lo que la convierte en una diana terapéutica potencial.
Propósito Evolutivo y Ubicuidad de Notch
La historia de la vía Notch es tan antigua como la multicelularidad misma. Identificada por primera vez en la mosca de la fruta, Drosophila melanogaster, por su papel en el desarrollo de las alas (de ahí su nombre, ‘Notch’ que significa muesca o hendidura), se ha demostrado que esta vía es increíblemente conservada a lo largo de la evolución. Desde nematodos hasta mamíferos, los componentes clave de Notch y su mecanismo de acción han permanecido notablemente similares, lo que subraya su importancia fundamental en la biología. Su propósito evolutivo radica en proporcionar un mecanismo robusto y eficiente para que las células coordinen sus decisiones de desarrollo y diferenciación con sus vecinas inmediatas. En esencia, Notch actúa como un ‘teléfono’ celular que permite a una célula influir directamente en el comportamiento de la célula adyacente, un proceso crítico para la formación de patrones, la determinación del destino celular y la inhibición lateral. Esta inhibición lateral es un concepto clave donde una célula que adopta un destino particular inhibe a sus vecinas para que no adopten el mismo destino, asegurando la diversidad celular y la correcta estructuración de los tejidos.
La activación de Notch siempre es beneficiosa para la regeneración tisular.
Si bien Notch es crucial para el mantenimiento de células madre y la regeneración, su activación desregulada puede promover la proliferación de células madre cancerosas y el desarrollo tumoral, actuando como oncogén en muchos contextos.
Fisiología Molecular de la Vía Notch
La vía Notch es un ejemplo prístino de cómo la interacción de unas pocas proteínas puede desencadenar una cascada de eventos que culminan en cambios profundos en la expresión génica y el comportamiento celular. Su mecanismo es relativamente simple pero elegantemente eficiente.
Componentes Clave
La maquinaria Notch se compone de varios actores principales: el receptor Notch, sus ligandos y las enzimas de procesamiento. En mamíferos, existen cuatro receptores Notch (Notch1, Notch2, Notch3 y Notch4), que son proteínas transmembrana de un solo paso. Cada receptor tiene un gran dominio extracelular que contiene repeticiones de tipo EGF (Factor de Crecimiento Epidérmico), un dominio transmembrana y un dominio intracelular (NICD, Notch Intracellular Domain). Los ligandos de Notch son también proteínas transmembrana expresadas en células adyacentes. Se dividen en dos familias principales: la familia Delta-like (DLL1, DLL3, DLL4) y la familia Jagged (JAG1, JAG2). La interacción entre estos ligandos y receptores es el punto de inicio de la señalización.
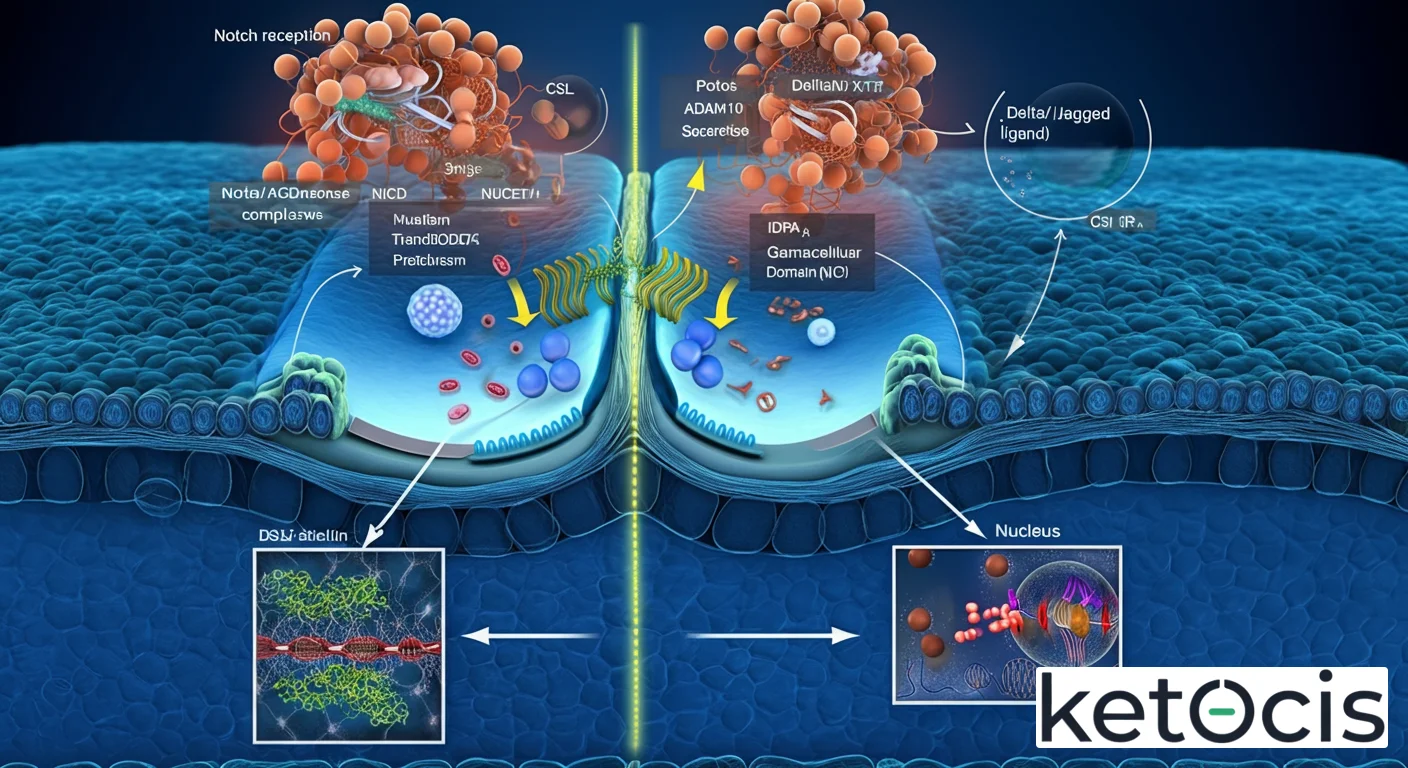
Mecanismo de Activación
La activación de Notch se inicia cuando un ligando (por ejemplo, DLL1) en la superficie de una célula se une a un receptor Notch en la superficie de una célula adyacente. Esta unión induce un cambio conformacional en el receptor Notch, haciéndolo susceptible a dos escisiones proteolíticas consecutivas. La primera escisión (S2) es realizada por metaloproteasas de la familia ADAM (ADAM10 o ADAM17), que liberan el dominio extracelular del receptor. Este evento deja un fragmento transmembrana que es el sustrato para la segunda y crucial escisión (S3). Esta escisión es llevada a cabo por el complejo de la γ-secretasa, una proteasa multiproteica notoria por su papel en la enfermedad de Alzheimer. La acción de la γ-secretasa libera el dominio intracelular de Notch (NICD) de la membrana. Una vez libre, el NICD es altamente inestable y se transloca rápidamente al núcleo celular.
Dentro del núcleo, el NICD no actúa solo. Se une al factor de transcripción CSL (también conocido como RBPJ en mamíferos o Suppressor of Hairless en Drosophila), que normalmente actúa como un represor transcripcional al reclutar complejos co-represores. La unión de NICD a CSL desplaza estos co-represores y recluta, en su lugar, coactivadores transcripcionales (como la familia de proteínas MAML, Mastermind-like). Esta reconfiguración del complejo de proteínas en el promotor de los genes diana transforma un represor en un activador transcripcional, induciendo la expresión de genes efectores de Notch. Los principales genes diana de Notch son los de la familia Hes (Homologs of hairy and enhancer of split) y Hey (hairy/enhancer-of-split related with YRPW motif), que son factores de transcripción que a su vez reprimen la expresión de genes involucrados en la diferenciación, manteniendo así a las células en un estado proliferativo e indiferenciado o dirigiendo su destino hacia una vía específica.
Regulación y Especificidad
La señalización Notch no es un sistema de ‘todo o nada’; está finamente regulada para asegurar la especificidad y la respuesta contextual. La glicosilación del dominio extracelular de Notch por enzimas de la familia Fringe (Lunatic, Manic, Radical Fringe) puede modular la afinidad de Notch por sus ligandos, sesgando la preferencia hacia los ligandos Delta-like o Jagged y, por ende, alterando la fuerza y duración de la señal. Además, la ubiquitilación y posterior degradación proteasomal del NICD actúan como un mecanismo de ‘apagado’ para limitar la duración de la señal. La complejidad aumenta con la existencia de múltiples receptores y ligandos, cada uno con patrones de expresión tisular específicos y afinidades de unión variables, permitiendo una gran diversidad de respuestas biológicas según el contexto celular y tisular.
Roles Biológicos Cruciales
La ubicuidad de Notch se traduce en su participación en una asombrosa variedad de procesos biológicos, desde la formación del embrión hasta el mantenimiento de la salud adulta.
Desarrollo Embrionario
En el desarrollo embrionario, Notch es un director de orquesta indispensable. En la neurogénesis, es fundamental para la determinación del destino neuronal, promoviendo la proliferación de células madre neurales y la inhibición lateral para asegurar la correcta proporción de neuronas y células gliales. En la somitogénesis, el proceso de segmentación del cuerpo embrionario en somitas, Notch actúa como un ‘reloj de segmentación’, oscilando su actividad para establecer los límites precisos de cada segmento. También es vital en la angiogénesis, donde regula la diferenciación de células endoteliales en vasos sanguíneos, controlando la formación de brotes y la maduración vascular. Su disfunción en estas etapas puede llevar a malformaciones congénitas severas en órganos como el corazón, el páncreas y el riñón.
Homeostasis Tisular y Células Madre Adultas
Más allá del desarrollo, Notch es un guardián de la integridad tisular en el adulto. Es crucial para el mantenimiento de nichos de células madre en diversos tejidos, incluyendo la médula ósea (células madre hematopoyéticas), el intestino (células madre intestinales), la piel y el cerebro. Al mantener a estas células en un estado indiferenciado y proliferativo, Notch asegura un suministro constante de células nuevas para la reparación y el reemplazo tisular. Por ejemplo, en el intestino, Notch promueve la proliferación de células madre criptales y la diferenciación de células absorbentes, mientras que inhibe la diferenciación de células caliciformes y enteroendocrinas, manteniendo el equilibrio del epitelio intestinal.
La comprensión de la vía Notch ha abierto fascinantes avenidas en medicina regenerativa. Al ser un regulador maestro de células madre, la modulación precisa de Notch podría, en el futuro, permitirnos expandir poblaciones específicas de células madre para reparar tejidos dañados o incluso ‘reprogramar’ células para terapias personalizadas, aunque aún estamos en las fases iniciales de investigación con desafíos significativos.
Notch y la Enfermedad
La importancia de Notch en la salud se hace dolorosamente evidente cuando la vía funciona mal. Su desregulación está en el centro de numerosas patologías.
Cáncer
La relación de Notch con el cáncer es compleja y contextual, pudiendo actuar tanto como oncogén como supresor tumoral dependiendo del tipo de cáncer y del tejido. En la leucemia linfoide aguda de células T (T-ALL), las mutaciones activadoras en el gen NOTCH1 son increíblemente comunes, llevando a una activación constitutiva de la vía que impulsa la proliferación incontrolada de los timocitos inmaduros. Aquí, Notch es un oncogén claro. Sin embargo, en otros cánceres, como algunos tipos de cáncer de pulmón o de piel, Notch puede actuar como supresor tumoral, promoviendo la diferenciación y deteniendo el crecimiento. Además, Notch desempeña un papel crucial en las células madre cancerosas, que son una pequeña subpoblación de células dentro de un tumor con capacidad de autorrenovación y tumorigenicidad, lo que las hace resistentes a las terapias convencionales y responsables de las recaídas.
Trastornos del Desarrollo
Las mutaciones en los genes de Notch o sus ligandos pueden dar lugar a trastornos congénitos. El Síndrome de Alagille, por ejemplo, es una enfermedad autosómica dominante caracterizada por anomalías hepáticas, cardíacas, esqueléticas y oculares, y es causado por mutaciones en el gen JAG1 (que codifica el ligando Jagged1) o, menos comúnmente, en NOTCH2. Otro ejemplo es la Arteriopatía Cerebral Autosómica Dominante con Infartos Subcorticales y Leukoencefalopatía (CADASIL), la forma más común de enfermedad cerebrovascular hereditaria, causada por mutaciones en el gen NOTCH3, que afectan la vasculatura cerebral y conducen a accidentes cerebrovasculares recurrentes y demencia.
Enfermedades Infecciosas e Inflamatorias
La vía Notch también modula la respuesta inmune, influyendo en la diferenciación y función de diversas células inmunitarias, como linfocitos T y B, macrófagos y células dendríticas. Su papel en la inflamación es bifacético, pudiendo ser pro- o antiinflamatorio según el contexto. Se ha demostrado que algunos patógenos, como virus y bacterias, manipulan la vía Notch para su propia replicación o para evadir la respuesta inmune del huésped, abriendo nuevas vías de investigación para terapias antivirales y antibacterianas.
Implicaciones Terapéuticas y Futuro
Dada la importancia de Notch en la enfermedad, no es sorprendente que se haya convertido en una diana terapéutica atractiva. La estrategia más explorada ha sido la inhibición de la vía, particularmente en el cáncer. Los inhibidores de γ-secretasa (GSI) son una clase de fármacos que bloquean la escisión S3 del receptor Notch, impidiendo la liberación de NICD y, por lo tanto, la activación de la vía. Estos han mostrado promesas en el tratamiento de la T-ALL y otros tumores donde Notch está hiperactivo. Sin embargo, el desafío principal con los GSI es la ubicuidad de Notch; su inhibición sistémica puede causar efectos secundarios significativos debido a su papel esencial en la homeostasis de tejidos normales como el intestino.
Otras estrategias incluyen el desarrollo de anticuerpos monoclonales dirigidos a los receptores Notch o a sus ligandos para bloquear la interacción célula-célula, o la modulación selectiva de isoformas específicas de Notch. La investigación actual se centra en desarrollar terapias más selectivas y con menos efectos secundarios, quizás mediante la entrega dirigida de fármacos o la identificación de inhibidores que actúen sobre isoformas específicas de Notch o sobre sus cofactores nucleares. La promesa de la manipulación de Notch en medicina regenerativa, para potenciar la reparación de tejidos o dirigir la diferenciación de células madre para trasplantes, es inmensa, aunque aún se encuentra en etapas experimentales y requiere una comprensión aún más profunda de su regulación contextual.
Es crucial desmitificar la idea de que ‘activar’ o ‘potenciar’ la vía Notch siempre es beneficioso. Aunque Notch es vital para la regeneración y el mantenimiento de células madre, su activación desregulada o inapropiada es un motor clave en muchos tipos de cáncer, promoviendo la proliferación descontrolada y la resistencia a la muerte celular. La modulación de Notch debe ser extremadamente precisa y contextual para evitar efectos adversos graves.
En resumen, la vía de señalización Notch es un eje central en la biología celular, un mecanismo elegante y potente que coordina el destino de las células en los organismos multicelulares. Desde el zigoto hasta el adulto, su función es indispensable para el desarrollo, la homeostasis y la regeneración. Su intrínseca conexión con la salud y la enfermedad la posiciona como un campo de investigación vibrante y una diana terapéutica con un potencial transformador. A medida que nuestra comprensión de sus intrincados mecanismos moleculares y sus interacciones con otras vías de señalización avanza, también lo hace nuestra capacidad para diseñar intervenciones precisas que puedan mitigar el sufrimiento y mejorar la calidad de vida.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.