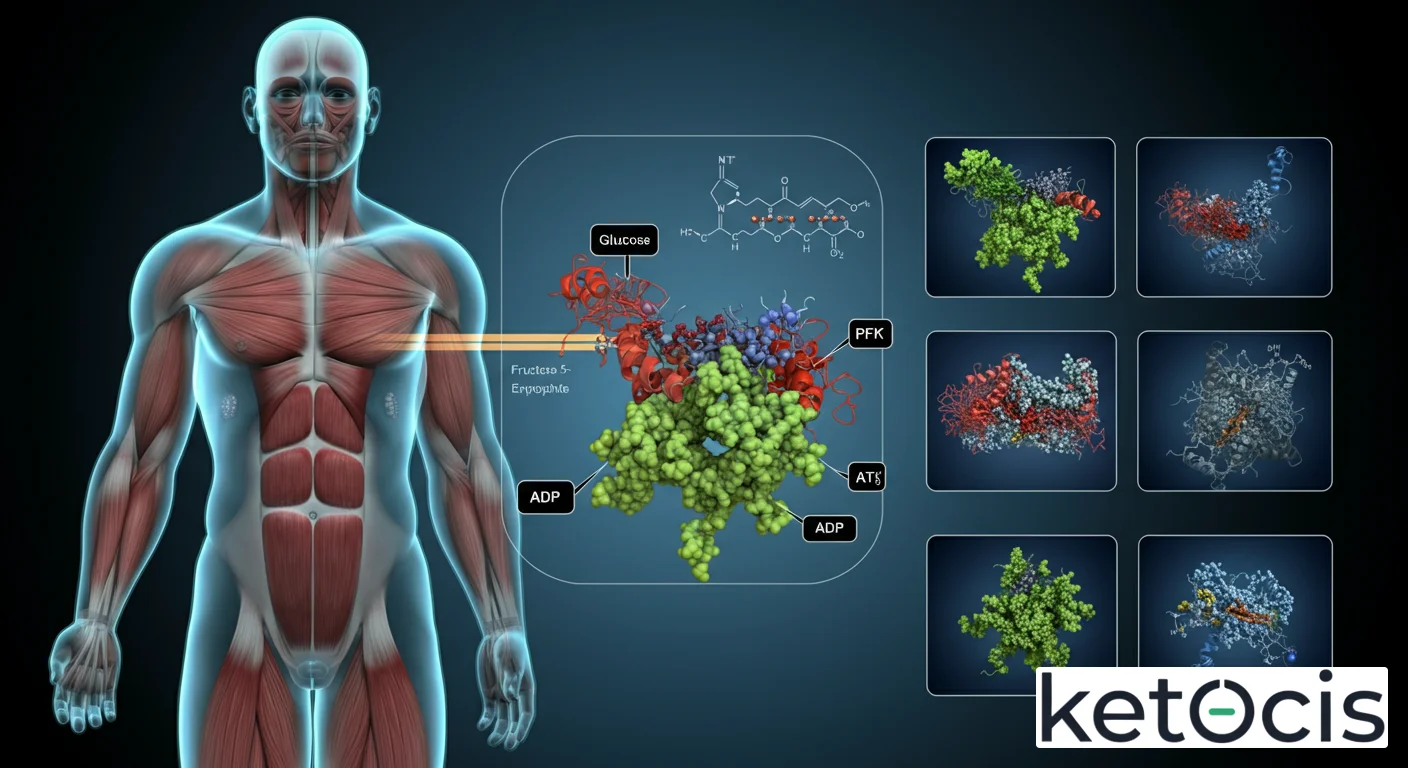
Fosfofructoquinasa (PFK): La Enzima Maestra de la Glucólisis
Resumen Clínico Rápido
🔬 Clasificación
Transferasa (quinasa) alostérica
⚙️ Función
Cataliza la fosforilación de fructosa-6-fosfato a fructosa-1,6-bisfosfato
📋 Impacto
Regulador clave e irreversible del flujo glucolítico y metabolismo energético
¿Qué es la Fosfofructoquinasa (PFK)? La Enzima Maestra del Flujo Energético
En el intrincado universo de la bioquímica humana, existen proteínas cuya función es tan pivotal que sin ellas, la vida tal como la conocemos sería imposible. Entre estas figuras estelares se encuentra la fosfofructoquinasa (PFK), una enzima que no solo cataliza una reacción crítica, sino que actúa como el director de orquesta de uno de los procesos metabólicos más fundamentales: la glucólisis. Comprender la PFK es desentrañar una parte esencial de cómo nuestro cuerpo genera energía, cómo se adapta a diferentes estados nutricionales como la cetosis y el ayuno, y cómo su disfunción puede impactar profundamente nuestra salud.
La PFK es mucho más que una simple catalizadora; es un sensor metabólico altamente sofisticado, capaz de integrar señales sobre el estado energético de la célula y ajustar el flujo de glucosa en consecuencia. Su actividad determina si la glucosa se quema rápidamente para obtener energía inmediata o si se conserva para otros fines. En esta guía definitiva, exploraremos cada faceta de esta fascinante enzima, desde su origen y mecanismo de acción hasta su papel en la flexibilidad metabólica y las implicaciones clínicas de su regulación.
Resumen Clínico
- Punto clave 1: La PFK-1 es la enzima reguladora clave e irreversible de la glucólisis, decidiendo el destino de la glucosa en el metabolismo.
- Punto clave 2: Su actividad es finamente modulada por el estado energético de la célula (ATP, AMP), metabolitos (citrato, fructosa-2,6-bisfosfato) y hormonas, adaptando la producción de energía.
- Punto clave 3: En estados de cetosis y ayuno, la PFK-1 se inhibe, desviando el metabolismo hacia la oxidación de grasas y la gluconeogénesis, optimizando el uso de sustratos energéticos.
Origen y Clasificación de la Fosfofructoquinasa
La fosfofructoquinasa es una enzima citosólica que pertenece a la clase de las transferasas, específicamente una quinasa. Su función principal es transferir un grupo fosfato de una molécula de ATP a un sustrato. Existen varias isoformas de PFK, pero las más estudiadas y relevantes en el metabolismo humano son la fosfofructoquinasa-1 (PFK-1) y la fosfofructoquinasa-2 (PFK-2).
PFK-1: El Punto de Control Principal
La PFK-1 es un enzima tetramérica, lo que significa que está compuesta por cuatro subunidades. En mamíferos, estas subunidades pueden ser de tres tipos: M (músculo), L (hígado) y C (cerebro), y se combinan para formar diferentes isoenzimas con propiedades cinéticas y reguladoras ligeramente distintas, adaptadas a las necesidades metabólicas de cada tejido. Es la PFK-1 la que cataliza la reacción irreversible y limitante de la velocidad en la glucólisis.
PFK-2: Un Regulador Indirecto
A diferencia de la PFK-1, la PFK-2 no participa directamente en la glucólisis principal. Su rol es sintetizar fructosa-2,6-bisfosfato (F-2,6-BP), un potente activador alostérico de la PFK-1. La PFK-2 es una enzima bifuncional, lo que significa que tiene dos actividades enzimáticas distintas: una actividad quinasa (PFK-2) que produce F-2,6-BP, y una actividad fosfatasa (fructosa-2,6-bisfosfatasa, FBPasa-2) que degrada F-2,6-BP. La regulación de la PFK-2 por hormonas como la insulina y el glucagón es crucial para controlar indirectamente la actividad de la PFK-1 y, por ende, el flujo glucolítico.
La glucólisis es siempre un proceso ineficiente y perjudicial para la salud.
La glucólisis es fundamental para la producción rápida de ATP en ausencia de oxígeno y para la síntesis de precursores metabólicos, siendo esencial para la función celular en diversos tejidos, como los eritrocitos y el cerebro. Su regulación es clave para la homeostasis energética y su desregulación puede contribuir a patologías.
Mecanismo de Acción: La Decisión Crucial de la Célula
La PFK-1 cataliza la siguiente reacción:
Fructosa-6-fosfato + ATP → Fructosa-1,6-bisfosfato + ADP
Esta reacción es el tercer paso de la glucólisis y es termodinámicamente irreversible. Es considerada el punto de compromiso de la vía glucolítica, ya que una vez que la glucosa-6-fosfato se convierte en fructosa-1,6-bisfosfato, el destino de esta molécula es continuar a través de la glucólisis hasta piruvato. Este paso consume una molécula de ATP, lo que subraya la importancia de su estricta regulación.
Regulación Alostérica: El Termostato Metabólico
La PFK-1 es una enzima alostérica, lo que significa que su actividad puede ser modificada por la unión de moléculas reguladoras en sitios distintos al sitio activo. Esta regulación es increíblemente compleja y permite a la célula ajustar finamente su metabolismo energético en respuesta a sus necesidades.
Activadores Clave: Señales de Baja Energía y Abundancia de Sustrato
- AMP (Adenosín Monofosfato): Es el activador alostérico más importante que señala un bajo estado energético de la célula. Cuando el ATP se hidroliza a ADP y luego a AMP, indica una demanda energética alta, lo que estimula la PFK-1 para aumentar la producción de ATP a través de la glucólisis.
- Fructosa-2,6-bisfosfato (F-2,6-BP): Es el activador más potente de la PFK-1. Su concentración está controlada por la PFK-2/FBPasa-2 y es un indicador clave de la disponibilidad de glucosa. Un aumento en F-2,6-BP señala abundancia de glucosa y promueve la glucólisis.
- Fosfato Inorgánico (Pi): También puede activar la PFK-1, especialmente en condiciones de ejercicio intenso cuando el ATP se hidroliza rápidamente.
Inhibidores Clave: Señales de Alta Energía y Abundancia de Productos
- ATP (Adenosín Trifosfato): Aunque es un sustrato, el ATP también actúa como un inhibidor alostérico de la PFK-1 a altas concentraciones. Esto es un mecanismo de retroalimentación negativa: cuando hay suficiente ATP, no es necesario producir más, por lo que la glucólisis se ralentiza.
- Citrato: Un intermediario del ciclo de Krebs, el citrato se acumula cuando hay un exceso de sustratos energéticos (grasas y carbohidratos) que entran al ciclo. Su acumulación indica que la célula tiene energía suficiente y que los precursores están disponibles para la biosíntesis, por lo que inhibe la PFK-1 para desviar la glucosa hacia otras vías (como el almacenamiento en glucógeno o la síntesis de ácidos grasos).
- Bajo pH (H+): La acumulación de iones de hidrógeno (H+) debido a la producción excesiva de lactato durante el ejercicio anaeróbico intenso, también inhibe la PFK-1. Esto protege al músculo de un daño excesivo por la acumulación de ácido láctico.
PFK y la Regulación Metabólica: Un Baile de Energía
La PFK-1 no opera de forma aislada. Su actividad se coordina con otras vías metabólicas y está bajo el control de señales hormonales, especialmente la insulina y el glucagón. En el hígado, por ejemplo, la PFK-1 es particularmente sensible a la F-2,6-BP, cuya síntesis está directamente regulada por estas hormonas.
- Estado Postprandial (Abundancia de Glucosa): Después de una comida rica en carbohidratos, la insulina aumenta. Esto activa la PFK-2 hepática, lo que lleva a un aumento en la producción de F-2,6-BP. El F-2,6-BP, a su vez, activa potentemente la PFK-1, impulsando la glucólisis para procesar el exceso de glucosa, que luego puede ser almacenada como glucógeno o convertida en grasa.
- Estado de Ayuno (Deficiencia de Glucosa): Durante el ayuno, el glucagón aumenta. El glucagón activa la FBPasa-2 (la actividad fosfatasa de la PFK-2), disminuyendo los niveles de F-2,6-BP. La reducción de F-2,6-BP inhibe la PFK-1, frenando la glucólisis hepática y desviando los precursores hacia la gluconeogénesis para mantener los niveles de glucosa en sangre.
Esta regulación diferencial permite que el hígado actúe como un glucostato, manteniendo la homeostasis de la glucosa en el cuerpo.
PFK en Contextos de Cetosis y Ayuno
En estados metabólicos como la cetosis nutricional o el ayuno prolongado, donde la disponibilidad de glucosa es limitada y el cuerpo se adapta a utilizar grasas y cuerpos cetónicos como principal fuente de energía, la actividad de la PFK-1 se ve significativamente modulada.
Cuando el cuerpo entra en cetosis, se produce un cambio metabólico profundo. La glucemia disminuye, y los niveles de insulina bajan, mientras que los de glucagón aumentan. Este perfil hormonal favorece la actividad de la FBPasa-2 (parte de la PFK-2), lo que reduce la concentración de F-2,6-BP. Con menos F-2,6-BP, la PFK-1 pierde su activador más potente y su actividad disminuye drásticamente. Esto asegura que la poca glucosa disponible se conserve para tejidos que dependen exclusivamente de ella, como los glóbulos rojos, o que se utilice en procesos vitales de gluconeogénesis.
Además, la oxidación de ácidos grasos, que se intensifica durante la cetosis y el ayuno, produce un aumento en las concentraciones de ATP y citrato. Ambos son potentes inhibidores alostéricos de la PFK-1. Por lo tanto, la abundancia de energía derivada de las grasas y los cuerpos cetónicos envía una señal a la PFK-1 para que “apague” la glucólisis, priorizando el uso de combustibles alternativos. Este es un ejemplo brillante de flexibilidad metabólica, donde la PFK-1 juega un papel central en la adaptación del cuerpo a diferentes fuentes de energía.
Biohacking Metabólico: Entrenando tu PFK para la Flexibilidad
Para optimizar la función de tu PFK y mejorar tu flexibilidad metabólica, considera la alternancia estratégica de estados nutricionales. La práctica de ayuno intermitente o períodos de alimentación baja en carbohidratos no solo educa a tu cuerpo a quemar grasas de manera más eficiente, sino que también modula la actividad de la PFK-1. Al reducir la dependencia constante de la glucosa, tu PFK-1 se vuelve más sensible a las señales de baja energía y más eficiente en la conservación de glucosa cuando escasea, promoviendo una adaptación metabólica robusta. Esto puede traducirse en mayor energía sostenida y mejor composición corporal.
Antagonistas y Moduladores Farmacológicos: PFK y la Enfermedad
La PFK-1 es un objetivo de interés en la investigación médica, particularmente en el contexto del cáncer. Las células cancerosas a menudo exhiben el “efecto Warburg”, un fenómeno donde prefieren la glucólisis aeróbica (producción de lactato incluso en presencia de oxígeno) para generar energía y precursores biosintéticos. En muchos cánceres, las isoformas de PFK-1 y PFK-2 están reguladas al alza, impulsando este metabolismo glucolítico acelerado. Por lo tanto, la inhibición de la PFK-1 o la modulación de la PFK-2/FBPasa-2 son estrategias que se están explorando para el desarrollo de terapias anticáncer.
Aunque no hay fármacos directamente dirigidos a la PFK-1 ampliamente utilizados en la clínica, algunos medicamentos como la 2-desoxiglucosa actúan como análogos de la glucosa y pueden inhibir indirectamente la glucólisis. Además, el estudio de moduladores específicos de PFK podría abrir nuevas vías para el tratamiento de enfermedades metabólicas y el cáncer, buscando “reprogramar” el metabolismo celular.
Optimización de la Función de la PFK y la Flexibilidad Metabólica
La PFK es una enzima fundamental para la salud metabólica. Mantener su capacidad de respuesta y su adecuada regulación es clave para una buena flexibilidad metabólica, es decir, la capacidad del cuerpo para cambiar eficientemente entre la quema de carbohidratos y grasas como combustible.
Estrategias Dietéticas
- Dietas Bajas en Carbohidratos y Cetogénicas: Como se mencionó, estas dietas naturalmente reducen el flujo glucolítico y, por ende, la actividad de la PFK-1, promoviendo la oxidación de grasas y la producción de cuerpos cetónicos. Esto “entrena” a tu metabolismo para ser más eficiente en el uso de grasas.
- Ayuno Intermitente: Períodos de ayuno inducen cambios hormonales (baja insulina, alto glucagón) que modulan la PFK-2/FBPasa-2, inhibiendo la PFK-1 y fomentando la lipólisis y la cetogénesis.
Ejercicio Físico
El ejercicio es un potente modulador del metabolismo. Durante el ejercicio intenso, la demanda de ATP aumenta drásticamente, lo que lleva a un aumento en los niveles de AMP y Pi, activando la PFK-1 para impulsar la glucólisis y la producción rápida de energía. A largo plazo, el entrenamiento regular mejora la capacidad oxidativa de los músculos, lo que puede influir en la sensibilidad de la PFK a sus reguladores, contribuyendo a una mejor flexibilidad metabólica.
Nutrientes Clave
Algunos micronutrientes son cofactores esenciales para enzimas metabólicas, incluyendo aquellas involucradas en la regulación de la PFK o en las vías que interactúan con ella:
- Magnesio: Es un cofactor importante para muchas quinasas, incluyendo la PFK, ya que el ATP se une a menudo en forma de complejo Mg-ATP.
- Vitaminas del Grupo B: Aunque no directamente cofactores de la PFK-1, son esenciales para otras enzimas de la glucólisis y el ciclo de Krebs, lo que indirectamente afecta el flujo de sustratos y productos que regulan la PFK.
Alerta Médica: Deficiencia de Fosfofructoquinasa (Enfermedad de Tarui)
La deficiencia de fosfofructoquinasa-1 es un trastorno metabólico genético raro, conocido como la enfermedad de Tarui (o glucogenosis tipo VII). Esta condición afecta principalmente a los músculos, causando fatiga muscular temprana, calambres, debilidad y mioglobinuria (presencia de mioglobina en la orina) después del ejercicio. En algunos casos, también puede afectar a los glóbulos rojos, provocando anemia hemolítica. La incapacidad de las células musculares para generar ATP a través de la glucólisis de manera eficiente limita severamente su capacidad para realizar trabajo, destacando la importancia crítica de la PFK-1 para la función muscular normal. Si experimentas síntomas inexplicables de fatiga muscular o calambres, consulta a un profesional de la salud.
Conclusión: La PFK, un Pilar del Metabolismo
La fosfofructoquinasa (PFK), y en particular la PFK-1, es una enzima de inmensa importancia en la bioquímica humana. Su papel como el principal punto de control de la glucólisis la posiciona como un regulador maestro del flujo energético, dictando cómo y cuándo nuestras células utilizan la glucosa para obtener energía. Su sofisticada regulación alostérica, influenciada por el estado energético celular y las señales hormonales, permite una adaptación metabólica excepcional a diversas condiciones, desde la abundancia de nutrientes hasta el ayuno prolongado y la cetosis.
Comprender la PFK no solo nos brinda una visión profunda de los mecanismos fundamentales de la vida, sino que también ilumina las bases de enfermedades metabólicas y ofrece posibles vías para intervenciones terapéuticas. Al optimizar su función a través de estrategias dietéticas y de estilo de vida, podemos fomentar una mayor flexibilidad metabólica, promoviendo así la salud y el bienestar general.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.