ATP Sintasa: El Motor Molecular de la Energía Celular | Ketocis
Resumen Clínico Rápido
🔬 Clasificación
Enzima (motor molecular)
⚙️ Función
Síntesis de ATP
📋 Impacto
Producción de energía celular
En el intrincado universo de la biología celular, existen máquinas moleculares de asombrosa complejidad y eficiencia que sustentan la vida tal como la conocemos. Entre ellas, la ATP sintasa se erige como una de las más fundamentales y elegantes. Considerada el motor molecular por excelencia de nuestras células, esta enzima multifuncional es la responsable directa de sintetizar la moneda energética universal: el adenosín trifosfato (ATP). Sin la ATP sintasa, la vasta mayoría de los organismos eucariotas y procariotas no podrían llevar a cabo las reacciones metabólicas esenciales que definen la vida, desde la contracción muscular hasta la transmisión nerviosa y la síntesis de proteínas.
Imagínese un diminuto generador rotatorio, un nanomotor biológico que, impulsado por un flujo de protones, es capaz de acoplar una reacción energéticamente desfavorable (la unión de ADP y fosfato inorgánico) con una favorable (el movimiento de iones a través de una membrana). Esta es, en esencia, la proeza que realiza la ATP sintasa. Su estudio no solo desvela los secretos de la bioenergética, sino que también ofrece perspectivas cruciales para entender enfermedades metabólicas, neurodegenerativas y el proceso de envejecimiento.
Resumen Clínico: Puntos Clave de la ATP Sintasa
- La ATP sintasa es un motor molecular esencial que sintetiza ATP, la principal fuente de energía celular, a partir de ADP y fosfato inorgánico.
- Su funcionamiento se basa en la fuerza motriz de protones, un gradiente electroquímico generado principalmente por la cadena de transporte de electrones en las mitocondrias.
- Es crucial para todas las funciones biológicas, y su disfunción está implicada en enfermedades metabólicas, neurodegenerativas y el envejecimiento.
Más ATP sintasa significa energía ilimitada y rendimiento sobrehumano.
La producción de ATP está finamente regulada por la demanda celular y la disponibilidad de sustratos; un exceso no se traduce en energía 'ilimitada' y la eficiencia depende de múltiples factores mitocondriales.
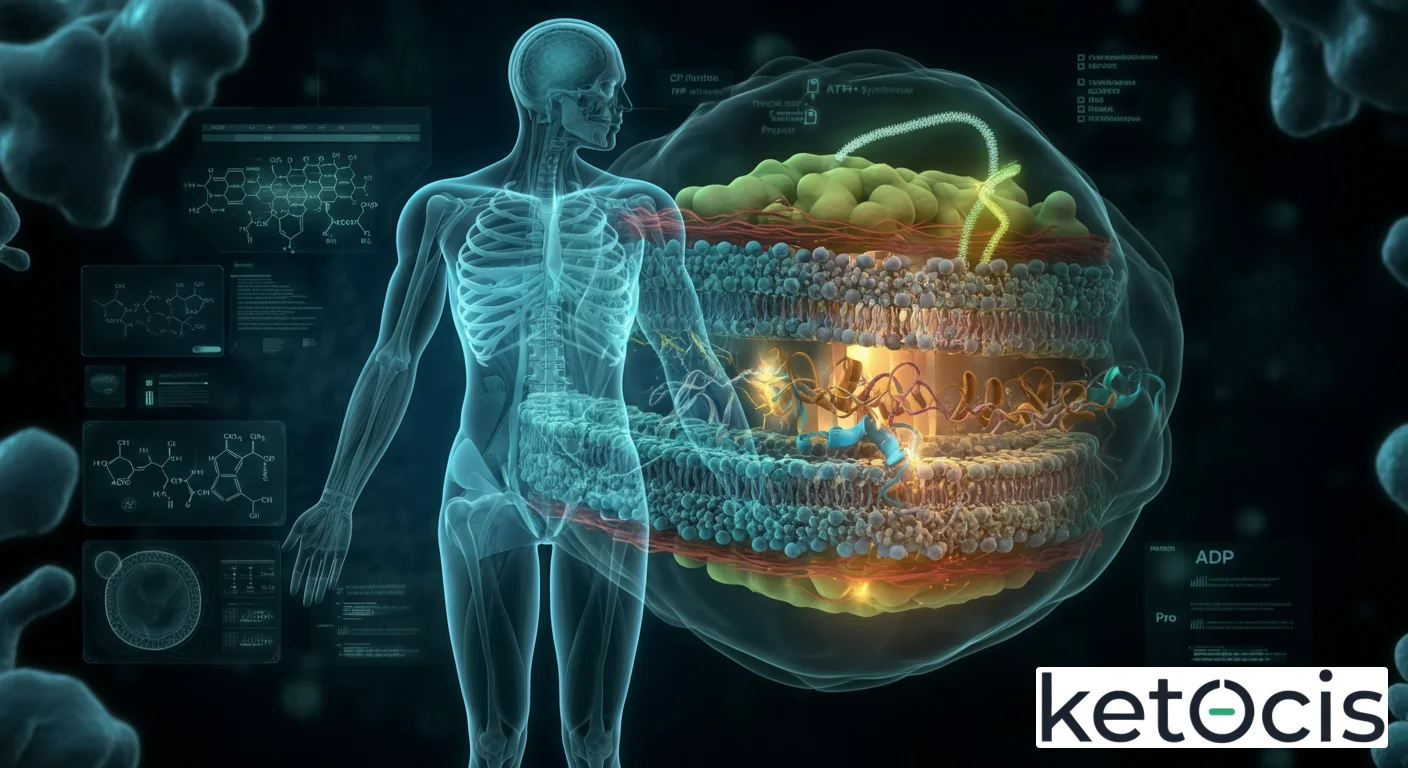
Ubicación y Estructura: El Santuario Energético Celular
La ATP sintasa no opera en el vacío; su ubicación estratégica es clave para su función. En las células eucariotas, reside principalmente en la membrana interna mitocondrial, ese pliegue intrincado que maximiza la superficie para la producción de energía. También se encuentra en las membranas tilacoidales de los cloroplastos en plantas y algas, y en la membrana plasmática de bacterias y arqueas, donde cumple la misma función vital.
Estructuralmente, la ATP sintasa es un complejo proteico masivo, compuesto por dos motores rotatorios principales: F0 y F1. Cada uno de estos motores es una máquina en sí misma, formada por múltiples subunidades proteicas:
- El motor F0: Es la porción transmembrana de la enzima, anclada en la membrana interna mitocondrial. Actúa como un canal y un rotor de protones. Está compuesto por varias subunidades, siendo las más destacadas el anillo de subunidades ‘c’ (que rota al paso de los protones) y la subunidad ‘a’ (que forma el canal de entrada y salida de protones). Este componente es el encargado de transformar la energía del gradiente electroquímico en movimiento mecánico rotatorio.
- El motor F1: Es la porción catalítica de la enzima, que se proyecta hacia la matriz mitocondrial. Es la sede donde se sintetiza el ATP. Se compone de un hexámero de subunidades α y β (tres de cada una), que forman los sitios activos para la unión de ADP y Pi. En el centro de este hexámero se encuentra una subunidad ‘γ’ (gamma) en forma de eje, que conecta F0 con F1 y transmite el movimiento rotatorio. Además, existen subunidades ‘δ’ (delta) y ‘ε’ (épsilon) que contribuyen a la estructura y función del complejo.
La interacción coordinada de estas subunidades permite que la ATP sintasa funcione como un verdadero nanomotor rotatorio, convirtiendo la energía potencial de un gradiente de protones en energía química almacenada en los enlaces de alta energía del ATP.
Mecanismo de Acción: La Danza Molecular de la Energía
El funcionamiento de la ATP sintasa es un testimonio de la elegancia y eficiencia de la evolución biológica, descrito por el Nobel Paul Boyer como el “mecanismo de cambio de conformación” o “catálisis rotatoria”. Todo comienza con la creación de un gradiente electroquímico de protones, también conocido como fuerza motriz de protones (PMF).
En las mitocondrias, la cadena de transporte de electrones (CTE) bombea protones (H+) desde la matriz hacia el espacio intermembrana, creando una mayor concentración de protones fuera de la matriz y una carga positiva en el espacio intermembrana. Esta diferencia de concentración y carga eléctrica genera la PMF, una forma de energía potencial.
La ATP sintasa aprovecha esta PMF de la siguiente manera:
- Flujo de Protones a Través de F0: Los protones, impulsados por el gradiente electroquímico, fluyen de regreso a la matriz mitocondrial a través de un canal específico en el motor F0. Al hacerlo, interactúan con las subunidades ‘c’ del anillo de F0, provocando su rotación. Cada protón que atraviesa el canal induce un giro específico en el anillo ‘c’.
- Rotación del Eje Gamma (γ): El giro del anillo ‘c’ en F0 se transmite directamente a la subunidad ‘γ’ (gamma), que actúa como un eje central. Este eje ‘γ’ se extiende hacia el motor F1 y gira dentro del anillo hexamérico de subunidades α3β3.
- Cambios Conformacionales en F1 y Síntesis de ATP: La rotación del eje ‘γ’ induce cambios conformacionales secuenciales en las tres subunidades ‘β’ del motor F1. Cada subunidad ‘β’ pasa por tres estados distintos:
- Estado L (Loose): Se une débilmente a ADP y Pi.
- Estado T (Tight): Une fuertemente a ADP y Pi, y cataliza la formación de ATP.
- Estado O (Open): Libera el ATP recién sintetizado y tiene baja afinidad por sustratos.
A medida que el eje ‘γ’ gira, cada subunidad ‘β’ pasa por estos tres estados en secuencia, lo que permite la unión de sustratos, la síntesis de ATP y su liberación de manera continua. Este proceso rotatorio es increíblemente eficiente, generando hasta 3 ATP por cada rotación completa del eje ‘γ’ (que típicamente requiere el paso de 8-10 protones, dependiendo de la especie). Es una verdadera maravilla de la nanotecnología biológica.
Rol Crucial en la Vida y el Metabolismo
La ATP sintasa es el epicentro de la producción de energía aeróbica en la mayoría de los organismos. Sin ella, la vida compleja, tal como la conocemos, sería inviable. El ATP que produce es esencial para:
- Contracción Muscular: La energía para el movimiento proviene directamente de la hidrólisis de ATP.
- Transporte Activo: Bombas iónicas, como la bomba de sodio-potasio, utilizan ATP para mantener los gradientes electroquímicos necesarios para la señalización nerviosa y el equilibrio osmótico.
- Biosíntesis de Macromoléculas: La síntesis de proteínas, ácidos nucleicos, lípidos y carbohidratos requiere un aporte constante de ATP.
- Termogénesis: La hidrólisis de ATP y los procesos metabólicos asociados generan calor, manteniendo la temperatura corporal.
- Mantenimiento Celular: Reparación de ADN, división celular, reciclaje de componentes celulares, todo depende del ATP.
La eficiencia de la ATP sintasa es notable; es capaz de convertir aproximadamente el 40-50% de la energía del gradiente de protones en energía química de ATP, lo que la convierte en una de las máquinas moleculares más eficientes conocidas.
Regulación y Factores Moduladores
La actividad de la ATP sintasa está finamente regulada para adaptarse a las demandas energéticas de la célula. Varios factores pueden influir en su función:
- Disponibilidad de Sustratos: La concentración de ADP y Pi en la matriz mitocondrial es un regulador clave. Un aumento en ADP indica una alta demanda de energía, estimulando la ATP sintasa.
- Gradiente de Protones: La magnitud de la fuerza motriz de protones es el principal determinante de la velocidad de síntesis de ATP.
- Inhibidor Natural (IF1): En condiciones de hipoxia o isquemia (falta de oxígeno), la proteína inhibidora IF1 se une a la ATP sintasa, bloqueando la hidrólisis de ATP. Esto es crucial para prevenir el agotamiento de ATP en la célula cuando la síntesis oxidativa no es posible.
- Inhibidores Farmacológicos y Toxinas: Sustancias como la oligomicina se unen a la porción F0, bloqueando el canal de protones e impidiendo la síntesis de ATP. La DCCD (diciclohexilcarbodiimida) también inhibe F0.
- Desacopladores: Moléculas como la termogenina (proteína desacoplante 1 o UCP1), presente en el tejido adiposo marrón, o el 2,4-dinitrofenol (DNP, un desacoplador sintético), permiten que los protones regresen a la matriz mitocondrial sin pasar por la ATP sintasa. Esto disipa el gradiente de protones, generando calor en lugar de ATP. Aunque la UCP1 tiene un rol fisiológico en la termogénesis, los desacopladores sintéticos son extremadamente peligrosos.
Biohacking Metabólico: Optimiza tu ATP Sintasa y Energía Celular
Para potenciar la función de tu ATP sintasa y, por ende, tu producción de energía, enfócate en la salud mitocondrial. La actividad física regular, especialmente el entrenamiento de alta intensidad por intervalos (HIIT) y el ejercicio de resistencia, estimula la biogénesis mitocondrial, es decir, la formación de nuevas mitocondrias y la mejora de las existentes. Una dieta rica en antioxidantes, como los polifenoles presentes en frutas y verduras de colores vibrantes, protege las mitocondrias del daño oxidativo. Nutrientes clave como el Coenzima Q10 (CoQ10), el magnesio y las vitaminas del grupo B son cofactores esenciales para la cadena de transporte de electrones y la propia ATP sintasa. Incluso la exposición controlada al frío, mediante duchas frías o crioterapia, puede activar la termogénesis y mejorar la función mitocondrial, ya que estimula la biogénesis y la actividad de las UCPs, lo que indirectamente puede optimizar la eficiencia de la ATP sintasa en otros tejidos al mejorar el estado metabólico general.
ATP Sintasa en Contextos Metabólicos Especiales: Cetosis y Ayuno
Los estados metabólicos como la cetosis nutricional y el ayuno intermitente o prolongado tienen un impacto profundo en la bioenergética celular y, por ende, en la ATP sintasa. Cuando el cuerpo cambia de la glucosa a las grasas y los cuerpos cetónicos como principal fuente de combustible, se producen adaptaciones significativas.
- Oxidación de Cuerpos Cetónicos: Los cuerpos cetónicos, como el β-hidroxibutirato, se oxidan en las mitocondrias para producir acetil-CoA, que entra en el ciclo de Krebs. Este proceso genera NADH y FADH2, que alimentan la cadena de transporte de electrones, manteniendo un robusto gradiente de protones para la ATP sintasa. La oxidación de cuerpos cetónicos puede ser energéticamente más eficiente en términos de ATP producido por unidad de oxígeno consumido en comparación con la glucosa, lo que podría indicar una mayor eficiencia del acoplamiento entre la CTE y la ATP sintasa.
- Aumento de Biogénesis Mitocondrial: El ayuno y la cetosis son potentes inductores de la biogénesis mitocondrial, el proceso de formación de nuevas mitocondrias. Un mayor número de mitocondrias, o mitocondrias más densas y funcionales, significa más ATP sintasa disponible, lo que mejora la capacidad de la célula para generar energía. Esto es mediado por vías de señalización como la AMPK y la SIRT1.
- Mayor Eficiencia del Acoplamiento: Algunas investigaciones sugieren que la oxidación de ácidos grasos y cuerpos cetónicos puede resultar en un acoplamiento más eficiente entre la cadena de transporte de electrones y la ATP sintasa, lo que se traduce en una menor producción de especies reactivas de oxígeno (ROS) por unidad de ATP producida, optimizando la salud mitocondrial.
En esencia, estos estados metabólicos no solo cambian el tipo de combustible, sino que también refinan la maquinaria que lo convierte en energía, haciendo que la ATP sintasa trabaje de manera más optimizada y resiliente.
Importancia Clínica y Patologías Asociadas
La disfunción de la ATP sintasa puede tener consecuencias devastadoras para la salud, dada su centralidad en la producción de energía. Se han identificado diversas patologías relacionadas con defectos en esta enzima:
- Enfermedades Mitocondriales: Mutaciones genéticas en las subunidades de la ATP sintasa (tanto en el ADN nuclear como en el mitocondrial) pueden llevar a síndromes severos. Ejemplos incluyen el síndrome de NARP (Neuropatía, Ataxia, Retinitis Pigmentosa) y algunas formas de la neuropatía óptica hereditaria de Leber (LHON), que afectan predominantemente tejidos de alta demanda energética como el cerebro, los músculos y los ojos.
- Enfermedades Neurodegenerativas: La disfunción mitocondrial, incluyendo defectos en la ATP sintasa, se ha implicado en la patogénesis de enfermedades como el Parkinson, el Alzheimer y la esclerosis lateral amiotrófica (ELA). Una producción de ATP comprometida puede llevar a estrés oxidativo, disfunción sináptica y muerte neuronal.
- Cáncer: El “Efecto Warburg”, característico de muchas células cancerosas, implica un cambio hacia el metabolismo glucolítico incluso en presencia de oxígeno. Aunque la ATP sintasa sigue presente, su actividad puede ser modulada o su papel en la producción de energía disminuido en favor de la glucólisis anaeróbica. Sin embargo, la ATP sintasa sigue siendo un objetivo terapéutico potencial, ya que algunas células cancerosas pueden volverse dependientes de la fosforilación oxidativa.
- Envejecimiento: La acumulación de daño mitocondrial con la edad, incluyendo la disminución de la eficiencia de la ATP sintasa y la cadena de transporte de electrones, es una de las teorías principales del envejecimiento. La reducción en la capacidad de producir ATP contribuye a la pérdida de función celular y tisular.
Alerta Metabólica: El Peligro de los Desacopladores No Controlados
Aunque la termogenina (UCP1) es un desacoplador natural vital para la termogénesis en el tejido adiposo marrón, el uso indiscriminado de desacopladores sintéticos como el 2,4-dinitrofenol (DNP) es extremadamente peligroso y ha causado muertes. Estos compuestos disipan el gradiente de protones mitocondrial sin producir ATP, generando un calor excesivo y descontrolado. Esto lleva a una hipertermia maligna, daño orgánico múltiple y colapso circulatorio. Nunca se deben usar estas sustancias fuera de un entorno clínico estrictamente controlado, y mucho menos como “ayuda para la pérdida de peso”. La optimización de la función mitocondrial debe buscarse a través de estrategias fisiológicas y seguras.
Mitos Comunes y Realidades Científicas
Con un tema tan fundamental como la energía celular, surgen inevitablemente mitos y simplificaciones:
- Mito: “Más ATP sintasa significa energía ilimitada y rendimiento sobrehumano.”
- Realidad: Aunque una ATP sintasa funcional es crucial, la producción de ATP está finamente regulada por la demanda celular y la disponibilidad de sustratos. Un exceso no se traduce necesariamente en energía “ilimitada”; el cuerpo opera con un equilibrio. Además, factores como la capacidad de la cadena de transporte de electrones para generar el gradiente de protones son igualmente limitantes.
- Mito: “Todos los suplementos energéticos actúan directamente sobre la ATP sintasa.”
- Realidad: Pocos suplementos tienen un efecto directo y comprobado sobre la ATP sintasa en sí. Muchos “potenciadores de energía” actúan aumentando la disponibilidad de sustratos para la cadena de transporte de electrones (como la creatina que regenera ATP rápidamente, o el CoQ10 que facilita el transporte de electrones), o mejorando la biogénesis mitocondrial general, lo que indirectamente beneficia a la ATP sintasa. Es fundamental buscar evidencia científica sólida detrás de cualquier afirmación.
Conclusión: El Nanomotor de la Vida
La ATP sintasa es mucho más que una simple enzima; es un nanomotor rotatorio que encarna la ingeniería perfecta de la naturaleza. Su capacidad para acoplar un flujo de protones con la síntesis de ATP es una de las proezas más impresionantes de la bioquímica, una que sustenta cada parpadeo, cada pensamiento y cada latido del corazón.
Comprender la ATP sintasa no solo nos permite apreciar la complejidad de la vida a nivel molecular, sino que también nos brinda herramientas para abordar la salud desde una perspectiva bioenergética. Mantener la función óptima de esta máquina molecular a través de un estilo de vida saludable, una nutrición adecuada y, potencialmente, intervenciones de biohacking basadas en la ciencia, es fundamental para la vitalidad, la prevención de enfermedades y la promoción de la longevidad. Es, sin duda, una de las heroínas silenciosas que trabajan incansablemente en cada una de nuestras células, garantizando que la chispa de la vida nunca se apague.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.