TLR2: Receptor Toll-like 2 y su Impacto en Inmunidad y Salud
Resumen Clínico Rápido
🔬 Clasificación
Receptor de Reconocimiento de Patrones (PRR)
⚙️ Función
Detección de patógenos y daño celular, iniciación de respuesta inmune
📋 Impacto
Regulación de inflamación, autoinmunidad, homeostasis metabólica
¿Qué es el Receptor de Tipo Toll 2 (TLR2)? La Guía Definitiva del Glosario Ketocis
En el vasto y complejo universo de la biología humana, nuestro sistema inmune actúa como un centinela incansable, dotado de una sofisticada red de sensores moleculares diseñados para distinguir lo propio de lo ajeno, y lo sano de lo dañado. Entre estos guardianes celulares, los Receptores de Tipo Toll (TLRs) se erigen como pilares fundamentales de la inmunidad innata, la primera línea de defensa de nuestro organismo. Dentro de esta familia crucial, el Receptor de Tipo Toll 2 (TLR2) ocupa un lugar de particular relevancia, actuando como un detector maestro de una amplia gama de amenazas microbianas y señales de peligro endógenas.
El TLR2 no es simplemente un receptor; es un integrador de información, una puerta de enlace que, al detectar patrones moleculares específicos, desencadena cascadas de señalización que culminan en una potente respuesta inflamatoria e inmune. Su papel va mucho más allá de la mera detección de patógenos. Se entrelaza con procesos metabólicos, la homeostasis intestinal y la modulación de enfermedades crónicas, convirtiéndolo en un objetivo fascinante para la investigación y las estrategias de optimización de la salud. En esta guía enciclopédica, desentrañaremos la intrincada biología del TLR2, explorando su estructura, su mecanismo de acción, su rol en la salud y la enfermedad, y cómo las estrategias de biohacking pueden influir en su función.
Resumen Clínico
- Punto clave 1: El TLR2 es un receptor clave de la inmunidad innata, crucial para la detección de una amplia variedad de patógenos bacterianos y fúngicos, así como de señales de daño celular.
- Punto clave 2: Funciona principalmente como un heterodímero (con TLR1 o TLR6), lo que le permite reconocer patrones moleculares específicos (PAMPs y DAMPs) y activar vías de señalización proinflamatorias.
- Punto clave 3: Su disfunción o activación crónica está implicada en diversas patologías, incluyendo enfermedades autoinmunes, metabólicas y la progresión del cáncer, subrayando la importancia de su regulación.
1. Estructura Molecular y Distribución Celular del TLR2
El TLR2 pertenece a una familia de diez receptores de tipo Toll identificados en humanos, caracterizados por su capacidad para reconocer patrones moleculares conservados. A nivel estructural, el TLR2 es una proteína transmembrana tipo I, que consta de tres dominios principales: un dominio extracelular rico en repeticiones de leucina (LRR), un dominio transmembrana y un dominio intracelular de homología con el receptor de interleucina-1 (TIR).
El dominio LRR extracelular es el sitio de reconocimiento de los ligandos. Su arquitectura en forma de herradura le permite interactuar con diversas moléculas, demostrando una notable plasticidad. A diferencia de otros TLRs que funcionan como homodímeros o monómeros, el TLR2 es excepcional por su obligatoria capacidad de formar heterodímeros para funcionar. Principalmente, se asocia con TLR1 para reconocer lipopéptidos triacilados, o con TLR6 para identificar lipopéptidos diacilados y el ácido lipoteicoico de bacterias Gram-positivas. Esta capacidad de heterodimerización amplía significativamente su espectro de reconocimiento de ligandos, convirtiéndolo en un sensor altamente versátil.
La distribución del TLR2 es ubicua, expresándose en una amplia gama de células inmunes y no inmunes. Se encuentra abundantemente en células mieloides como macrófagos, monocitos, células dendríticas y neutrófilos, donde su papel en la respuesta inmune es primordial. Sin embargo, su presencia en células no inmunes como fibroblastos, queratinocitos, células endoteliales y epiteliales (particularmente en el intestino y las vías respiratorias) resalta su función integral en la vigilancia tisular y la homeostasis. Esta amplia distribución subraya su importancia no solo en la eliminación de patógenos, sino también en la modulación de la inflamación local y sistémica.
Activar TLR2 siempre es bueno para la inmunidad.
Mientras que la activación de TLR2 es crucial para la defensa contra patógenos, su activación crónica o desregulada por DAMPs (patrones asociados a daño) puede conducir a inflamación crónica, autoinmunidad y contribuir a enfermedades metabólicas. El equilibrio es clave.
2. Mecanismo de Acción y Reconocimiento de Ligandos
El corazón de la función del TLR2 reside en su capacidad para actuar como un receptor de reconocimiento de patrones (PRR). Esto significa que no reconoce antígenos específicos como lo hace el sistema inmune adaptativo, sino que identifica estructuras moleculares conservadas que son esenciales para la supervivencia de los microorganismos (PAMPs o Patrones Moleculares Asociados a Patógenos) o que son liberadas por células dañadas (DAMPs o Patrones Moleculares Asociados a Daño).
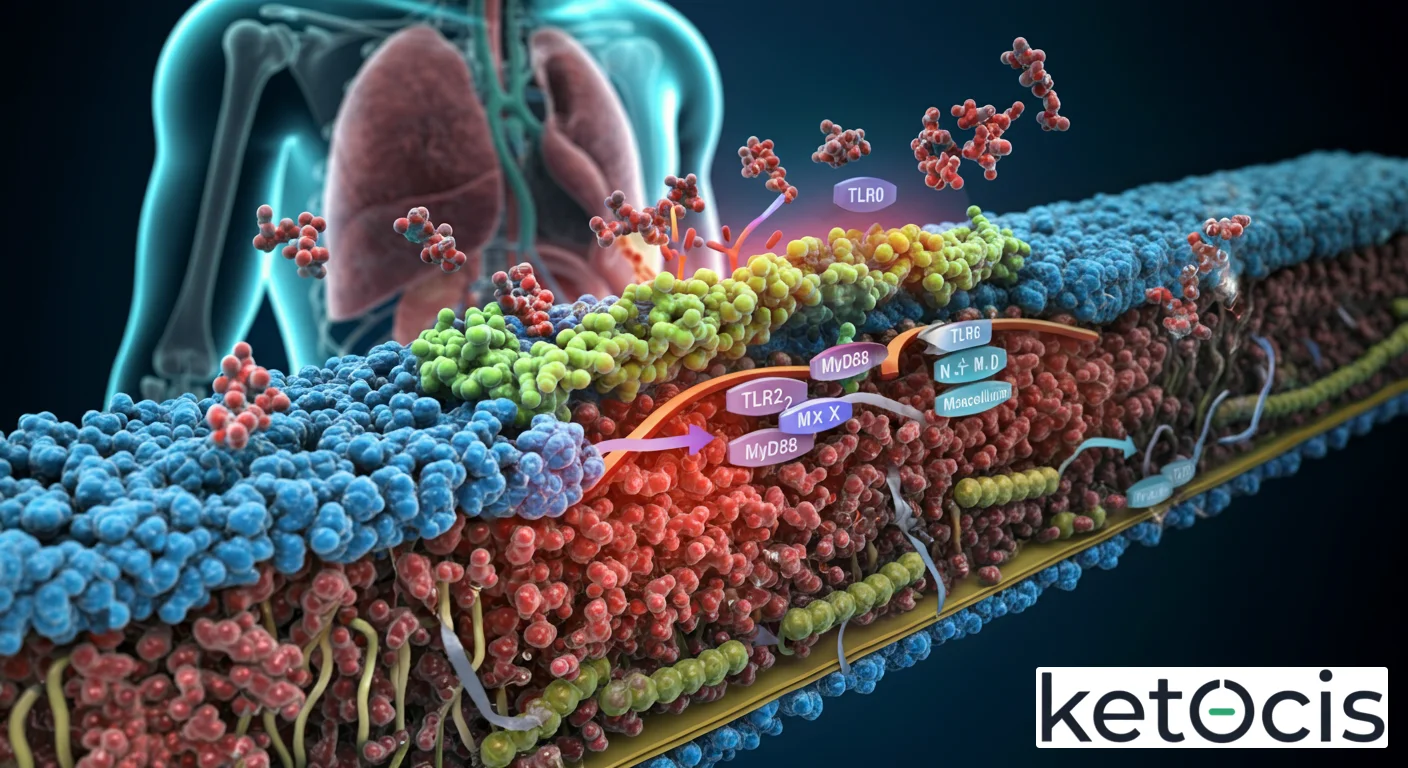
Cuando el TLR2, en su configuración heterodimérica (TLR2/TLR1 o TLR2/TLR6), se une a su ligando específico, se desencadena un cambio conformacional que permite el reclutamiento de proteínas adaptadoras al dominio TIR intracelular. La principal proteína adaptadora para el TLR2 es la proteína de diferenciación mieloide 88 (MyD88). La unión de MyD88 inicia una cascada de señalización intracelular que involucra a quinasas como IRAK1, IRAK4 y TRAF6. Esta vía culmina en la activación de factores de transcripción clave, principalmente el Factor Nuclear Kappa B (NF-κB) y las quinasas activadas por mitógenos (MAPKs).
La activación de NF-κB y MAPKs resulta en la transcripción de genes que codifican para una amplia variedad de moléculas proinflamatorias y antimicrobianas. Esto incluye citoquinas (como IL-6, TNF-α, IL-1β), quimiocinas (que atraen a otras células inmunes), moléculas de adhesión y péptidos antimicrobianos. Esta respuesta coordinada es esencial para montar una defensa eficaz contra los invasores y para reparar el tejido dañado. Los principales ligandos del TLR2 incluyen lipopéptidos bacterianos (como el Pam3CSK4 para TLR2/TLR1 y el Pam2CSK4 para TLR2/TLR6), el ácido lipoteicoico de bacterias Gram-positivas, el peptidoglicano, la porina de Neisseria, y el zimógeno de hongos. Además, el TLR2 también puede reconocer DAMPs, como las proteínas de choque térmico (HSPs) o el ácido hialurónico de alto peso molecular, que son liberadas por células estresadas o necróticas, contribuyendo a la inflamación estéril.
3. Rol Fisiológico y Patológico del TLR2
Inmunidad Innata y Defensa Antimicrobiana
La función más estudiada del TLR2 es su papel central en la inmunidad innata contra una miríada de patógenos. Es indispensable para la detección de bacterias Gram-positivas, micobacterias y ciertas espiroquetas, así como para la respuesta antifúngica. En el intestino, el TLR2 juega un rol crítico en el mantenimiento de la homeostasis, detectando componentes de la microbiota comensal y modulando la respuesta inmune local para prevenir una inflamación excesiva o una disbiosis. Una función adecuada del TLR2 en las barreras epiteliales es vital para la integridad de la defensa.
Inflamación y Autoinmunidad
Dada su capacidad para iniciar respuestas proinflamatorias, no sorprende que el TLR2 esté profundamente implicado en diversas condiciones inflamatorias y autoinmunes. La activación crónica o desregulada del TLR2, a menudo por DAMPs liberados durante el daño tisular o por una microbiota disbiótica, puede perpetuar la inflamación. Se ha demostrado que el TLR2 contribuye a la patogénesis de enfermedades como la artritis reumatoide, el lupus eritematoso sistémico y la esclerosis múltiple, donde el reconocimiento de autoantígenos o la respuesta exacerbada a infecciones pueden desencadenar o agravar la enfermedad.
Cáncer
El papel del TLR2 en el cáncer es complejo y bidireccional. Por un lado, la activación del TLR2 en células inmunes puede promover una respuesta antitumoral, estimulando la producción de citoquinas y la activación de células T citotóxicas. Por otro lado, la activación crónica del TLR2 por el microambiente tumoral (que a menudo contiene DAMPs y componentes microbianos) puede promover la proliferación de células tumorales, la angiogénesis y la supresión inmune, favoreciendo la progresión del cáncer. Esta dualidad hace que el TLR2 sea un objetivo prometedor, pero desafiante, para terapias oncológicas.
Biohacking y Optimización del TLR2: El Poder de los Fitonutrientes
Ciertos compuestos bioactivos presentes en nuestra dieta pueden modular la actividad del TLR2, ofreciendo una vía para el biohacking de la inmunidad. Por ejemplo, los polifenoles como la curcumina (cúrcuma) y el resveratrol (uvas rojas) han demostrado inhibir la señalización de TLR2/MyD88, atenuando la inflamación. De manera similar, los ácidos grasos omega-3 (EPA y DHA) pueden reducir la expresión de TLR2 y la producción de citoquinas proinflamatorias. Integrar estos fitonutrientes y grasas saludables en una dieta cetogénica o baja en carbohidratos puede ser una estrategia inteligente para optimizar una respuesta inmune equilibrada y mitigar la inflamación excesiva mediada por TLR2.
4. TLR2, Metabolismo y Estrategias de Modulación (Enfoque Ketocis)
La intersección entre la inmunidad innata y el metabolismo es un campo de investigación vibrante, y el TLR2 se encuentra en el centro de esta interacción. La activación desregulada del TLR2 se ha implicado en la patogénesis de enfermedades metabólicas como la obesidad, la resistencia a la insulina y la diabetes tipo 2.
En estados de sobrecarga nutricional o lipotoxicidad, los ácidos grasos saturados (especialmente el ácido palmítico) y otros DAMPs pueden activar el TLR2 en adipocitos, hepatocitos y células inmunes residentes en tejidos metabólicos. Esta activación conduce a una inflamación crónica de bajo grado, que es un sello distintico de la resistencia a la insulina y la disfunción metabólica. La señalización de TLR2 activa NF-κB, lo que interfiere con la señalización de la insulina y promueve la lipólisis, exacerbando aún más la disfunción metabólica.
Dieta Cetogénica y Ayuno Intermitente: Moduladores Potenciales
Aquí es donde el enfoque Ketocis (dieta cetogénica y ayuno intermitente) ofrece un terreno fértil para la modulación del TLR2. Los cuerpos cetónicos, en particular el beta-hidroxibutirato (BHB), no son solo fuentes de energía alternativas, sino también moléculas de señalización con potentes efectos antiinflamatorios. El BHB ha demostrado inhibir el inflamasoma NLRP3, una vía inflamatoria que a menudo se cruza con la señalización de TLRs.
Aunque la investigación directa sobre el efecto de la cetosis en la expresión o actividad del TLR2 es un área en desarrollo, se postula que al reducir la lipotoxicidad (mediante la quema de grasa y la disminución de ácidos grasos libres circulantes), mejorar la sensibilidad a la insulina y modular la microbiota intestinal, la dieta cetogénica y el ayuno pueden indirectamente atenuar la activación patológica del TLR2. Un intestino más sano, con una menor translocación de PAMPs bacterianos, significa menos estímulos para el TLR2 en la circulación sistémica. Además, la reducción general de la inflamación sistémica en estados cetogénicos puede contribuir a un perfil de señalización de TLR2 más equilibrado.
Estrategias de Optimización y Modulación
- Modulación de la Microbiota Intestinal: Dado que el TLR2 es un sensor clave de la microbiota, mantener una microbiota diversa y equilibrada a través de prebióticos (fibra fermentable) y probióticos específicos puede influir positivamente en su señalización. Algunas cepas probióticas han demostrado modular la expresión de TLR2.
- Ácidos Grasos Omega-3: Como se mencionó en la caja de biohacking, los ácidos grasos poliinsaturados omega-3, como el EPA y el DHA, pueden suprimir la activación de TLR2 y la producción de citoquinas proinflamatorias, ofreciendo un efecto protector contra la inflamación crónica.
- Compuestos Bioactivos Vegetales: Polifenoles (curcumina, resveratrol, quercetina, EGCG del té verde) y otros fitoquímicos tienen la capacidad de modular las vías de señalización de TLR2, a menudo inhibiendo NF-κB y reduciendo la respuesta inflamatoria.
- Ejercicio Regular: La actividad física ha demostrado tener efectos inmunomoduladores, incluyendo la atenuación de la inflamación crónica, lo que podría influir indirectamente en la sensibilidad y respuesta del TLR2.
ALERTA MÉDICA: La Doble Cara de la Inmunidad – No Siempre Más es Mejor
Existe un mito persistente de que “activar” el sistema inmune o “potenciarlo” es siempre beneficioso. En el contexto del TLR2, esto es una simplificación peligrosa. Si bien la activación de TLR2 es vital para combatir infecciones agudas, la estimulación crónica o desregulada de este receptor puede ser altamente perjudicial. Una activación excesiva o prolongada del TLR2 por DAMPs (como los generados en el estrés oxidativo o el daño tisular crónico) o por una disbiosis intestinal persistente, puede llevar a una inflamación crónica sistémica. Esta inflamación es un motor clave en la progresión de enfermedades autoinmunes, resistencia a la insulina, aterosclerosis y ciertos tipos de cáncer. El objetivo no es activar a ciegas, sino buscar un equilibrio que permita una respuesta robusta cuando sea necesario, y una supresión eficiente cuando la amenaza haya pasado. La homeostasis es la clave, no la hiperexcitación.
5. Implicaciones Terapéuticas y Futuras Direcciones
Dada la multifacética implicación del TLR2 en la salud y la enfermedad, este receptor representa un objetivo terapéutico atractivo. La modulación de su actividad podría ofrecer nuevas estrategias para el tratamiento de una amplia gama de patologías.
En el ámbito de las enfermedades infecciosas, agonistas específicos del TLR2 podrían potenciar la respuesta inmune en individuos inmunocomprometidos o como adyuvantes vacunales. Sin embargo, el mayor interés reside en el desarrollo de antagonistas o moduladores de TLR2 para mitigar la inflamación patológica. Por ejemplo, el desarrollo de péptidos o pequeñas moléculas que impidan la unión de ligandos al TLR2 o que interrumpan su heterodimerización podría ser beneficioso en enfermedades autoinmunes, sepsis o condiciones inflamatorias crónicas.
El desafío radica en la especificidad y la evitación de efectos secundarios indeseables, ya que el TLR2 desempeña un papel protector vital. Las estrategias futuras probablemente se centrarán en la modulación selectiva, quizás apuntando a subtipos específicos de heterodímeros de TLR2 o a vías de señalización descendentes. La investigación continúa explorando cómo los fármacos existentes y los compuestos naturales pueden influir en la actividad del TLR2, abriendo puertas a terapias más dirigidas y personalizadas en la era de la medicina de precisión.
Conclusión
El Receptor de Tipo Toll 2 (TLR2) es mucho más que un simple sensor de patógenos; es un director de orquesta molecular que orquesta respuestas inmunes e inflamatorias cruciales para nuestra supervivencia. Su capacidad para heterodimerizar y reconocer una amplia gama de PAMPs y DAMPs lo posiciona como un actor central en la inmunidad innata, la homeostasis tisular y la interconexión entre la inflamación y el metabolismo.
Comprender la intrincada biología del TLR2 no solo desvela los mecanismos fundamentales de nuestra defensa, sino que también ilumina caminos para intervenir en enfermedades crónicas que van desde la autoinmunidad hasta las patologías metabólicas. La capacidad de modular su actividad a través de estrategias de biohacking, como la dieta cetogénica, el ayuno, la optimización de la microbiota y la ingesta de fitonutrientes específicos, subraya el poder que tenemos para influir en nuestra salud a nivel molecular. En el Glosario Ketocis, el TLR2 emerge como un ejemplo paradigmático de cómo los detalles moleculares más finos se traducen en implicaciones profundas para el bienestar integral, invitándonos a una exploración continua de los límites de la ciencia y la optimización de la salud.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.