IκB: El Guardián de la Inflamación y NF-κB | Glosario Ketocis
Resumen Clínico Rápido
🔬 Clasificación
Proteína reguladora
⚙️ Función
Inhibición de NF-κB
📋 Impacto
Regulación inflamatoria
El Inhibidor de Kappa B (IκB): Centinela Molecular de la Inflamación
En el intrincado universo de la biología celular, donde cada proteína y vía de señalización orquesta una sinfonía de respuestas fisiológicas, existe un guardián molecular de la inflamación: el Inhibidor de Kappa B, o simplemente IκB. Esta familia de proteínas es absolutamente fundamental para mantener la homeostasis, actuando como un freno crucial sobre una de las vías proinflamatorias más potentes y estudiadas del organismo: el factor nuclear kappa B (NF-κB). Sin IκB, la maquinaria de respuesta inmune y el control de la inflamación se descontrolarían, llevando a consecuencias devastadoras para la salud.
La inflamación, en su forma aguda, es una respuesta vital para la defensa contra patógenos y la reparación de tejidos. Sin embargo, cuando esta respuesta se vuelve crónica o desregulada, se convierte en la raíz de innumerables enfermedades, desde autoinmunes y neurodegenerativas hasta metabólicas y oncológicas. Comprender el papel de IκB no solo nos permite desentrañar los mecanismos moleculares de la inflamación, sino que también abre puertas a estrategias innovadoras de biohacking y terapias dirigidas para restaurar el equilibrio y promover la salud.
Esta guía enciclopédica explorará en profundidad la naturaleza de IκB, su origen, su fascinante mecanismo de acción, los factores que lo regulan y, lo más importante, su relevancia en el contexto de la salud y la enfermedad, así como las prometedoras vías para su optimización.
Resumen Clínico
- El IκB es una familia de proteínas citoplasmáticas que actúan como inhibidores clave del factor de transcripción NF-κB.
- Su función principal es secuestrar a NF-κB en el citoplasma, impidiendo su translocación al núcleo y la consecuente activación de genes proinflamatorios.
- La degradación de IκB, inducida por el complejo IKK en respuesta a estímulos inflamatorios, es el paso crítico para la activación de NF-κB y el inicio de la respuesta inmune.
Origen y Naturaleza Molecular de IκB: La Familia de los Inhibidores
El término IκB no se refiere a una única proteína, sino a una familia de proteínas reguladoras que comparten una característica estructural y funcional común: la presencia de dominios de anquirina que les permiten unirse a los factores NF-κB. Los miembros más estudiados y prominentes de esta familia incluyen IκBα, IκBβ, IκBε, y también proteínas como Bcl-3 y IκBζ, cada una con matices en su regulación y función.
Estas proteínas son sintetizadas en el citoplasma celular y su expresión génica está, en muchos casos, regulada por el propio NF-κB, lo que establece un elegante bucle de retroalimentación negativa. Por ejemplo, la expresión de IκBα es inducida rápidamente tras la activación de NF-κB, lo que permite al sistema restaurar la inactividad de NF-κB una vez que el estímulo inflamatorio ha cesado o ha sido controlado. Esta característica es vital para prevenir una respuesta inflamatoria prolongada y potencialmente dañina.
La diversidad en la familia IκB no es meramente redundante; cada isoformo exhibe diferencias en su afinidad por los distintos dímeros de NF-κB (p. ej., p50/RelA, p50/c-Rel), en su cinética de degradación y en su capacidad para influir en la duración y especificidad de la respuesta inflamatoria. Esta especificidad permite a las células afinar su respuesta ante diferentes tipos de estímulos, asegurando que la activación de los factores de transcripción NF-κB sea precisa y contextualmente apropiada.
La inflamación es siempre mala y debe ser suprimida por completo.
La inflamación es una respuesta inmune esencial para la defensa y reparación. Es la inflamación crónica y desregulada la que es perjudicial. IκB ayuda a mantener un equilibrio crucial, permitiendo respuestas agudas necesarias y previniendo la cronicidad excesiva.
El Mecanismo de Acción de IκB: Controlando el Interruptor Inflamatorio
El núcleo de la función de IκB reside en su capacidad para secuestrar a NF-κB en el citoplasma de las células. En su estado inactivo, los dímeros de NF-κB (comúnmente p50/RelA) se encuentran unidos a IκB en el citosol. Esta unión es crucial porque IκB enmascara la señal de localización nuclear (NLS) de NF-κB, impidiendo que el factor de transcripción entre al núcleo y acceda al ADN para activar la transcripción génica.
La activación de la vía NF-κB es un proceso finamente regulado que se desencadena por una multitud de estímulos, incluyendo citocinas proinflamatorias como el Factor de Necrosis Tumoral alfa (TNF-α) e interleucina-1 beta (IL-1β), lipopolisacáridos (LPS) bacterianos, estrés oxidativo, daños en el ADN y señales de receptores de células T y B. Estos estímulos convergen en la activación de un complejo enzimático clave: el complejo de la quinasa IκB (IKK).
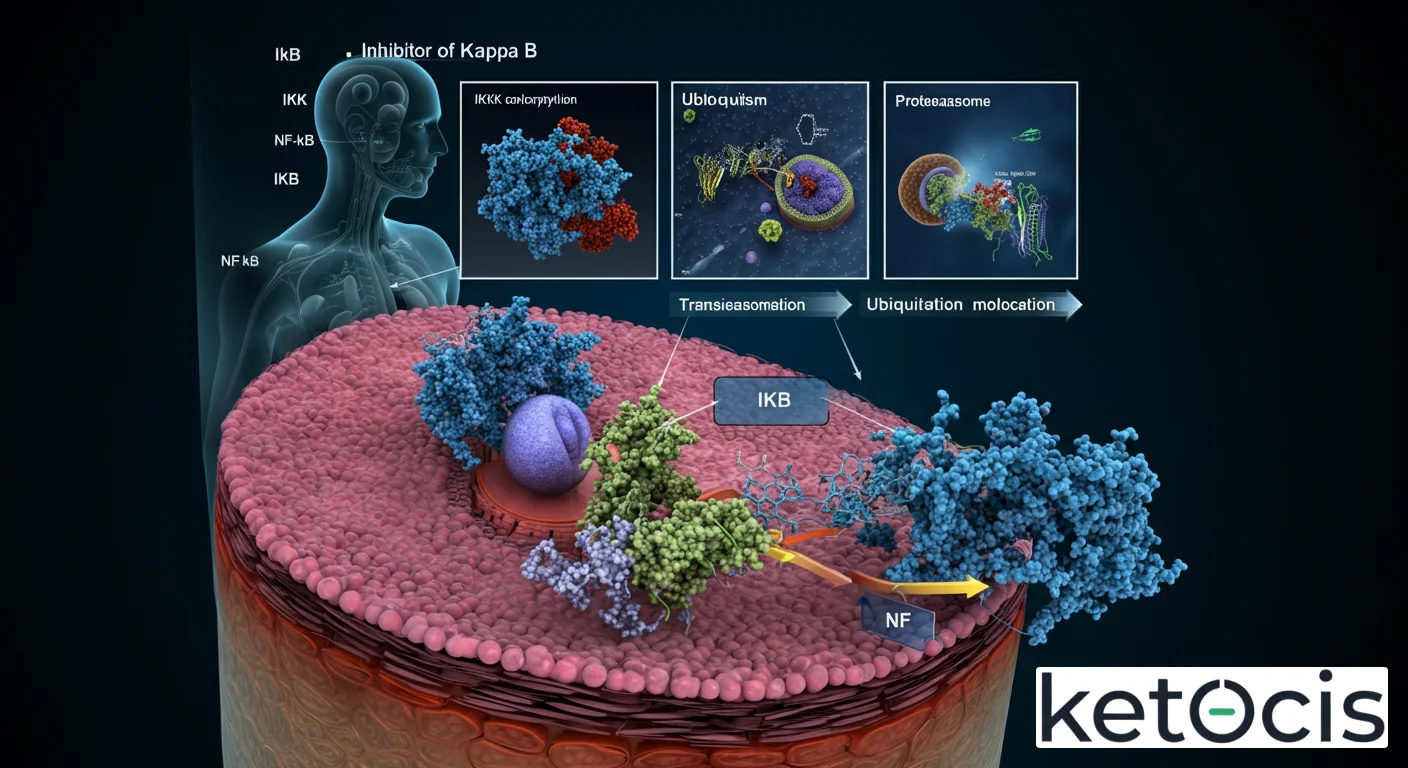
La Cascada de Activación de NF-κB:
- Activación de IKK: Los estímulos inflamatorios activan una serie de quinasas río arriba que, a su vez, fosforilan y activan el complejo IKK. Este complejo está compuesto principalmente por dos subunidades catalíticas, IKKα e IKKβ, y una subunidad reguladora, NEMO (IKKγ). IKKβ es a menudo la subunidad crítica para la activación ‘clásica’ de NF-κB en respuesta a la mayoría de los estímulos proinflamatorios.
- Fosforilación de IκB: Una vez activado, el complejo IKK fosforila residuos de serina específicos en el dominio N-terminal de IκB (por ejemplo, Ser32 y Ser36 en IκBα). Esta fosforilación es la señal crítica para la degradación de IκB.
- Ubiquitinación y Degradación Proteasomal: La fosforilación de IκB crea un sitio de reconocimiento para un complejo E3 ubiquitín ligasa. Este complejo añade cadenas de ubiquitina a IκB, marcándolo para su destrucción. Posteriormente, el IκB ubiquitinado es rápidamente reconocido y degradado por el proteasoma 26S, una máquina molecular encargada de la eliminación de proteínas dañadas o reguladas.
- Liberación y Translocación Nuclear de NF-κB: Con la degradación de IκB, el NF-κB queda libre. Su señal de localización nuclear se expone, permitiéndole translocarse desde el citoplasma al núcleo celular.
- Activación de la Transcripción Génica: Una vez en el núcleo, NF-κB se une a secuencias específicas de ADN (conocidas como sitios κB) en las regiones promotoras de sus genes diana. Esto conduce a la activación de la transcripción de una vasta red de genes involucrados en la inflamación, la respuesta inmune, la proliferación celular, la supervivencia y la apoptosis. Entre estos genes se encuentran citocinas proinflamatorias (como IL-6, IL-8, TNF-α), quimiocinas, moléculas de adhesión celular y enzimas como la ciclooxigenasa-2 (COX-2) y la óxido nítrico sintasa inducible (iNOS).
Este proceso es notablemente rápido y eficiente, permitiendo una respuesta celular casi inmediata a las amenazas. Sin embargo, su regulación estricta por IκB y el bucle de retroalimentación negativa (donde NF-κB induce la síntesis de nuevo IκBα) son esenciales para asegurar que la respuesta inflamatoria sea transitoria y se resuelva adecuadamente.
Reguladores y Moduladores de la Vía IκB/NF-κB
La vía IκB/NF-κB no es un sistema binario de ‘encendido y apagado’, sino una red compleja sujeta a múltiples niveles de regulación. Además del complejo IKK, otras enzimas y proteínas pueden influir en la estabilidad y función de IκB:
- Otras Quinasas: Aunque IKK es el jugador principal, otras quinasas pueden fosforilar IκB en diferentes sitios o en diferentes contextos, alterando su destino.
- Fosfatasas: Las fosfatasas son enzimas que eliminan grupos fosfato. Si IκB es desfosforilado por una fosfatasa antes de ser ubiquitinado, su degradación puede ser prevenida, prolongando su efecto inhibidor sobre NF-κB.
- Deubiquitinasas (DUBs): Estas enzimas eliminan las cadenas de ubiquitina de las proteínas. Las DUBs pueden ‘rescatar’ a IκB de la degradación proteasomal al eliminar las marcas de ubiquitina, lo que resulta en una estabilización de IκB y una supresión de la actividad de NF-κB. Un ejemplo es la enzima A20, que actúa como un regulador negativo clave de la vía NF-κB.
- Isoformas de IκB: Como se mencionó, las diferentes isoformas de IκB (IκBβ, IκBε) tienen diferentes cinéticas de degradación. IκBβ, por ejemplo, se degrada más lentamente que IκBα, lo que puede contribuir a una fase más sostenida de activación de NF-κB en ciertas respuestas.
El equilibrio entre la fosforilación, ubiquitinación, desfosforilación y desubiquitinación de IκB es lo que determina la duración y la intensidad de la activación de NF-κB. Esta orquestación molecular es crucial para la salud, ya que una disfunción en cualquiera de estos pasos puede llevar a una activación aberrante o insuficiente de NF-κB, con graves implicaciones patológicas.
Biohacking para la Optimización de IκB/NF-κB
Ciertos compuestos bioactivos presentes en alimentos pueden modular la actividad de la vía IκB/NF-κB. Por ejemplo, la curcumina, el polifenol activo de la cúrcuma, ha demostrado inhibir la activación de IKKβ, reduciendo así la fosforilación y degradación de IκB y, consecuentemente, la activación de NF-κB. De manera similar, el resveratrol, encontrado en uvas rojas y vino, puede influir en esta vía, ofreciendo una estrategia dietética fascinante para mitigar la inflamación crónica.
IκB en el Contexto de la Salud y la Enfermedad
Dada su posición central en la regulación de NF-κB, no es sorprendente que IκB y su vía estén implicados en una amplia gama de condiciones de salud y enfermedades.
Inflamación Crónica y Enfermedades Autoinmunes
Una activación persistente o desregulada de NF-κB, a menudo debido a fallos en la regulación de IκB, es un sello distintivo de la inflamación crónica. En enfermedades autoinmunes como la artritis reumatoide, el lupus eritematoso sistémico o la enfermedad inflamatoria intestinal (EII), los niveles elevados de citocinas proinflamatorias mantenidas por una activación anómala de NF-κB contribuyen a la patología. La modulación de la estabilidad de IκB o la actividad de IKK son, por lo tanto, objetivos terapéuticos atractivos para estas condiciones.
Cáncer
La vía NF-κB es un promotor bien conocido del cáncer. La activación constitutiva de NF-κB en muchas células tumorales promueve la proliferación celular, la supervivencia (inhibiendo la apoptosis), la angiogénesis y la metástasis. En este contexto, IκB actúa como un supresor tumoral potencial. Estrategias que restauran la función de IκB o inhiben su degradación podrían ser valiosas en la terapia oncológica, haciendo las células cancerosas más susceptibles a la quimioterapia o la radiación.
Enfermedades Metabólicas
La inflamación de bajo grado es un componente clave de la resistencia a la insulina, la obesidad y la diabetes tipo 2. La activación crónica de NF-κB en tejidos como el adiposo, el hígado y el músculo esquelético contribuye a la disfunción metabólica. La modulación de IκB/NF-κB a través de intervenciones dietéticas o farmacológicas podría mejorar la sensibilidad a la insulina y mitigar otras complicaciones metabólicas.
Neurodegeneración
Enfermedades como el Alzheimer y el Parkinson se caracterizan por neuroinflamación. La activación de NF-κB en las células gliales (microglía y astrocitos) puede conducir a la liberación de neurotoxinas y citocinas proinflamatorias, contribuyendo al daño neuronal. La regulación de IκB en el sistema nervioso central es un área activa de investigación para el desarrollo de nuevas terapias neuroprotectoras.
Estrategias de Biohacking y Optimización del Eje IκB/NF-κB
Dada la importancia de IκB en la regulación de la inflamación, existen varias estrategias de biohacking y estilo de vida que pueden influir positivamente en esta vía, promoviendo un equilibrio inflamatorio saludable.
Dieta y Nutrición
La alimentación es una de las herramientas más potentes para modular la inflamación. Una dieta rica en compuestos antiinflamatorios puede influir directamente en la actividad de IKK y la estabilidad de IκB:
- Polifenoles y Antioxidantes: Compuestos como la curcumina (cúrcuma), el resveratrol (uvas, vino tinto), la quercetina (cebolla, manzanas) y los galato de epigalocatequina (EGCG) del té verde han demostrado inhibir la activación de IKK y, por ende, la degradación de IκB.
- Ácidos Grasos Omega-3: Presentes en pescados grasos, semillas de chía y lino, los omega-3 son conocidos por sus propiedades antiinflamatorias, en parte a través de la modulación de vías de señalización, incluyendo la de NF-κB.
- Dieta Cetogénica: La dieta cetogénica, al promover un estado metabólico de cetosis, puede tener efectos antiinflamatorios significativos. Los cuerpos cetónicos, en particular el beta-hidroxibutirato (BHB), han demostrado inhibir el inflamasoma NLRP3 y modular la actividad de NF-κB, lo que indirectamente podría influir en la regulación de IκB. Una reducción en la carga glucémica y el estrés oxidativo asociados a dietas bajas en carbohidratos también puede disminuir los estímulos que activan la vía IKK/NF-κB.
- Ayuno Intermitente y Prolongado: El ayuno puede inducir la autofagia y reducir la inflamación sistémica. Aunque la relación directa con IκB es compleja, la reducción general de citocinas proinflamatorias y el estrés metabólico durante el ayuno pueden llevar a una menor activación de IKK y una mayor estabilidad de IκB.
Estilo de Vida
- Ejercicio Físico Regular: El ejercicio moderado y constante es un potente antiinflamatorio. Puede reducir los niveles de citocinas proinflamatorias y mejorar la función inmunológica, lo que sugiere una modulación favorable de la vía NF-κB/IκB.
- Manejo del Estrés: El estrés crónico puede activar la vía NF-κB a través de la liberación de hormonas como el cortisol y neurotransmisores. Técnicas de reducción del estrés como la meditación, el yoga o la respiración consciente pueden ayudar a mitigar esta activación.
- Sueño de Calidad: La privación del sueño está ligada a un aumento de marcadores inflamatorios. Asegurar un sueño reparador es fundamental para la regulación de los procesos inflamatorios, incluyendo la vía IκB/NF-κB.
La integración de estos compuestos bioactivos y hábitos de vida saludables puede fortalecer la función de IκB, manteniendo a NF-κB bajo control y promoviendo un entorno celular menos proinflamatorio.
Alerta Médica: El Riesgo de la Supresión Excesiva
Aunque la inhibición de NF-κB y la estabilización de IκB pueden ser deseables en el contexto de la inflamación crónica, una supresión excesiva o indiscriminada de esta vía puede ser peligrosa. La activación de NF-κB es vital para la respuesta inmune contra infecciones, la cicatrización de heridas y la supervivencia celular. La inhibición completa podría comprometer gravemente la capacidad del cuerpo para defenderse de patógenos o reparar tejidos, llevando a inmunodeficiencia o problemas de cicatrización. El equilibrio es clave.
El Futuro de la Investigación de IκB
La investigación sobre IκB y su papel en la regulación de NF-κB continúa siendo un campo vibrante y prometedor. Los avances en la comprensión de las especificidades de cada isoforma de IκB, la identificación de nuevos moduladores de IKK y la exploración de fármacos que restauran la función de IκB o previenen su degradación abren nuevas avenidas terapéuticas.
La medicina de precisión busca desarrollar tratamientos que se dirijan a componentes específicos de la vía NF-κB/IκB en contextos de enfermedad particulares, minimizando los efectos secundarios y maximizando la eficacia. La modulación dietética y los enfoques de biohacking, respaldados por una sólida base científica, ofrecen una poderosa estrategia complementaria para mantener esta vía en un estado de equilibrio saludable, previniendo la enfermedad y promoviendo la longevidad.
Conclusión
El Inhibidor de Kappa B (IκB) es mucho más que una simple proteína; es un maestro regulador, un centinela molecular que resguarda el equilibrio entre la respuesta inmune protectora y la inflamación dañina. Su intrincado mecanismo de acción, que implica la fosforilación, ubiquitinación y degradación proteasomal, es un ejemplo sublime de la sofisticación de la biología celular. Comprender a IκB no solo nos ilumina sobre la patogénesis de un sinfín de enfermedades, sino que también nos empodera con el conocimiento para influir en nuestra salud a través de elecciones conscientes de dieta y estilo de vida. Al optimizar la función de IκB, podemos aspirar a mitigar la inflamación crónica, fortalecer nuestras defensas y, en última instancia, vivir vidas más sanas y plenas.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.