Distrofina: La Guía Definitiva de un Investigador PhD
Resumen Clínico Rápido
🔬 Clasificación
Proteína citoesquelética
⚙️ Función
Estabilización de sarcolema, transmisión de fuerza
📋 Impacto
Causa principal de Distrofia Muscular de Duchenne y Becker
Introducción: La Arquitectura Molecular del Músculo
En el vasto y complejo universo de la biología humana, cada componente juega un papel irremplazable en el mantenimiento de la homeostasis y la función. Entre estas moléculas esenciales, la distrofina emerge como una proteína pivotal, una verdadera arquitecta de la integridad muscular. Su estudio no solo desvela los intrincados mecanismos de la contracción y estabilidad de nuestras fibras musculares, sino que también ilumina las causas subyacentes de algunas de las enfermedades neuromusculares más devastadoras. Para el Glosario Ketocis, comprender la distrofina es fundamental, ya que la salud muscular es un pilar de la función metabólica y la calidad de vida.
La distrofina es una proteína citoplasmática de gran tamaño, codificada por el gen DMD, uno de los genes humanos más grandes conocidos. Su descubrimiento en 1987 marcó un hito en la comprensión de las distrofias musculares, ofreciendo una dirección clara para la investigación y el desarrollo de terapias. Sin ella, o con una versión defectuosa, la delicada estructura del músculo esquelético y cardíaco se desmorona progresivamente, llevando a la debilidad y degeneración características de afecciones como la distrofia muscular de Duchenne y Becker.
Esta guía enciclopédica se adentrará en la esencia de la distrofina: su origen genético, su compleja estructura, su mecanismo de acción molecular y las devastadoras consecuencias de su ausencia o disfunción. Exploraremos también los avances más recientes en la investigación y las prometedoras estrategias de ‘biohacking’ molecular que buscan restaurar su función o mitigar sus efectos, brindando esperanza a millones de personas.
Resumen Clínico
- Punto clave 1: La distrofina es una proteína estructural gigante, esencial para la estabilidad y función de las células musculares esqueléticas y cardíacas.
- Punto clave 2: Codificada por el gen DMD, el gen humano más grande, actúa como un amortiguador mecánico vital entre el citoesqueleto y la matriz extracelular.
- Punto clave 3: Las mutaciones en el gen DMD causan las distrofias musculares de Duchenne (ausencia total o casi total) y Becker (distrofina defectuosa o reducida), llevando a la degeneración muscular progresiva.
La distrofia muscular es solo una enfermedad que afecta a niños y siempre es mortal.
Existen múltiples tipos de distrofias musculares, algunas con inicio en la adultez y variada severidad. La DMD es la más grave, pero los avances médicos están extendiendo la esperanza de vida y mejorando la calidad de vida de los pacientes. La BMD es una forma más leve.
Origen y Estructura Molecular de la Distrofina
El Gen DMD: Un Gigante Genético
La distrofina es el producto de un gen extraordinario: el gen DMD, localizado en el brazo corto del cromosoma X (Xp21). Con aproximadamente 2.4 millones de pares de bases, es el gen humano más grande identificado hasta la fecha. Esta inmensa longitud no es trivial; alberga 79 exones que deben ser cuidadosamente empalmados para producir el ARN mensajero (ARNm) funcional, que luego se traduce en la proteína distrofina. La magnitud del gen DMD lo convierte en un ‘punto caliente’ para mutaciones, lo que explica la alta incidencia de distrofias musculares ligadas al cromosoma X.
Las mutaciones en el gen DMD son predominantemente deleciones de uno o más exones, aunque también se observan duplicaciones y mutaciones puntuales. La gravedad de la enfermedad resultante, ya sea la distrofia muscular de Duchenne (DMD) o la distrofia muscular de Becker (BMD), depende en gran medida de si la mutación altera el ‘marco de lectura’ del gen. Una mutación que interrumpe el marco de lectura generalmente resulta en la ausencia completa de distrofina funcional, llevando a la DMD, la forma más grave. Si el marco de lectura se mantiene, se produce una distrofina más corta pero parcialmente funcional, lo que resulta en la BMD, una forma más leve y de progresión más lenta.
La Proteína Distrofina: Una Molécula Multifuncional
La proteína distrofina es una molécula alargada, con un peso molecular de 427 kDa, compuesta por cuatro dominios principales: un dominio N-terminal de unión a actina, un gran dominio central de repeticiones de espectrina, un dominio rico en cisteína y un dominio C-terminal. Cada uno de estos dominios contribuye a la función estructural y de señalización de la proteína.
- Dominio N-terminal: Se une a los filamentos de actina del citoesqueleto, anclando la distrofina a la red interna de la célula muscular.
- Dominio central de repeticiones de espectrina: Una región extensa que contiene múltiples repeticiones de 100-120 aminoácidos, lo que confiere a la distrofina una gran flexibilidad y resistencia a la tensión mecánica. Actúa como un muelle molecular, absorbiendo y distribuyendo las fuerzas generadas durante la contracción muscular.
- Dominio rico en cisteína: Contiene sitios de unión para el complejo de distroglicano.
- Dominio C-terminal: Interactúa con otras proteínas del complejo de distrofina-glicoproteína (DGC), sirviendo como un punto de anclaje crucial para la conexión con la membrana celular y la matriz extracelular.
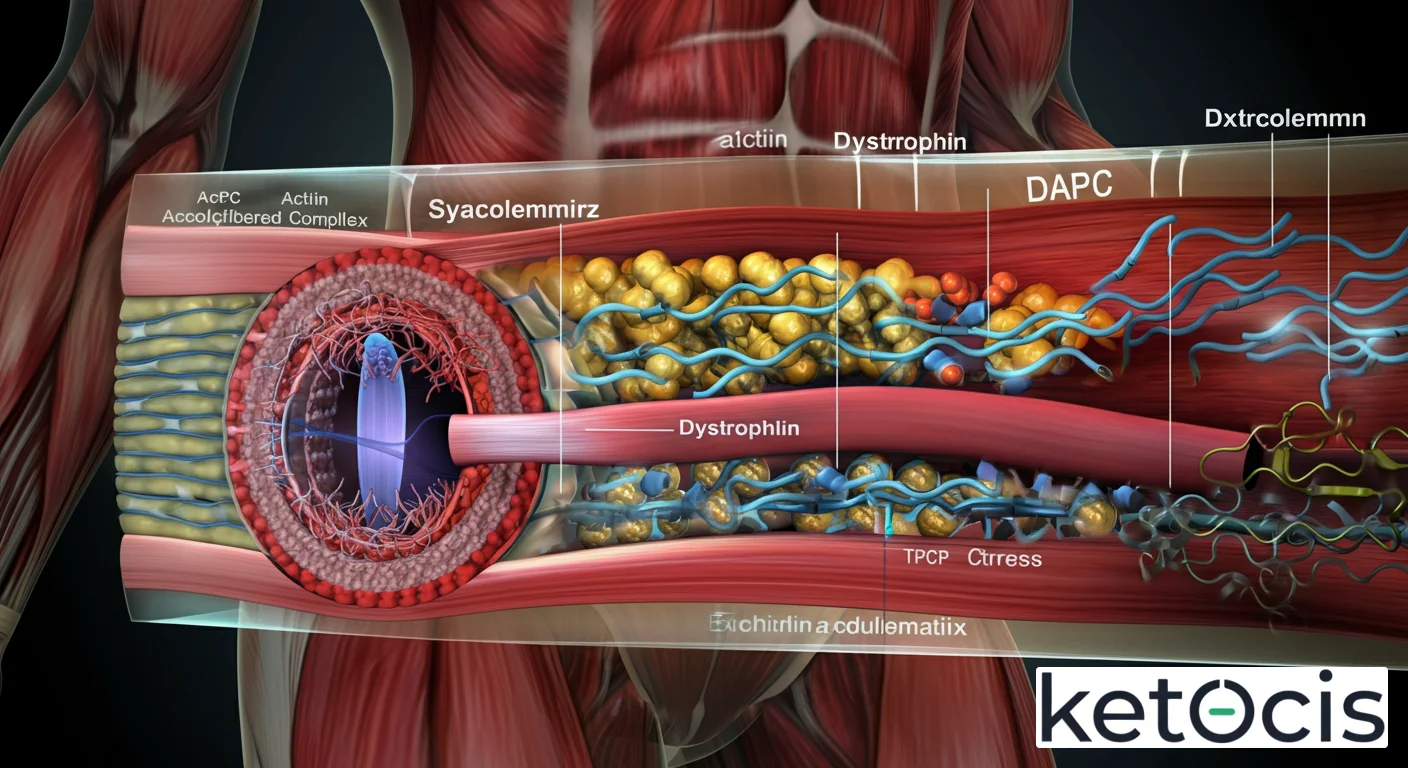
Mecanismo de Acción: El Complejo de Distrofina-Glicoproteína (DGC)
El Andamiaje Sarcolémico
La función principal de la distrofina es actuar como un componente clave del complejo de distrofina-glicoproteína (DGC), un andamiaje multiproteico que atraviesa la membrana plasmática de la célula muscular, conocida como sarcolema. Este complejo es esencial para la estabilidad mecánica de la fibra muscular durante la contracción y relajación, protegiéndola de daños inducidos por el estrés.
El DGC establece un vínculo vital entre el citoesqueleto intracelular (específicamente los filamentos de actina) y la matriz extracelular. La distrofina se une a la actina en el interior de la célula y, a través de sus dominios C-terminal y ricos en cisteína, se conecta con otras proteínas transmembrana del DGC, como los sarcoglicanos y el distroglicano. El distroglicano, a su vez, se une a proteínas de la matriz extracelular como la laminina-2. Esta conexión ininterrumpida asegura que las fuerzas generadas por la contracción de las miofibrillas se transmitan eficazmente a la matriz extracelular, protegiendo la integridad del sarcolema y evitando su ruptura.
Rol en la Señalización Celular
Más allá de su función estructural, la distrofina y el DGC también participan en la señalización celular. Se ha demostrado que el complejo influye en vías de señalización que regulan la homeostasis del calcio, la supervivencia celular, la regeneración muscular y la diferenciación. Por ejemplo, la ausencia de distrofina puede llevar a una desregulación de la señalización de óxido nítrico (NO), lo que contribuye a la patología de la DMD. La integridad del DGC es, por tanto, crucial no solo para la estabilidad física, sino también para el correcto funcionamiento metabólico y de señalización de la célula muscular.
Consecuencias de la Ausencia o Disfunción: Las Distrofias Musculares
Distrofia Muscular de Duchenne (DMD)
La distrofia muscular de Duchenne (DMD) es la distrofia muscular más común y grave, afectando aproximadamente a 1 de cada 3,500 niños varones nacidos vivos. Se caracteriza por la ausencia total o casi total de distrofina funcional debido a mutaciones en el gen DMD que provocan un cambio en el marco de lectura. Sin distrofina, el DGC es inestable, lo que hace que el sarcolema sea extremadamente vulnerable al daño durante la contracción muscular.
El ciclo patológico de la DMD comienza con microdesgarros en la membrana de las fibras musculares. Estos desgarros permiten la entrada de calcio extracelular, lo que activa proteasas dependientes de calcio y desencadena una cascada de eventos que conducen a la necrosis de las fibras musculares. El cuerpo intenta reparar este daño a través de la regeneración, pero con el tiempo, la capacidad regenerativa se agota y el tejido muscular es reemplazado por tejido conectivo (fibrosis) y grasa. Esto resulta en una debilidad muscular progresiva, que afecta primero los músculos proximales (caderas, muslos, hombros) y luego se extiende a todos los músculos esqueléticos, incluyendo los músculos respiratorios y el corazón. La esperanza de vida de los pacientes con DMD suele ser limitada, con la mayoría falleciendo por insuficiencia cardíaca o respiratoria en la tercera década de vida.
Distrofia Muscular de Becker (BMD)
La distrofia muscular de Becker (BMD) es una forma más leve y menos común de distrofia muscular, causada por mutaciones en el gen DMD que permiten la producción de una distrofina acortada o disfuncional, pero que mantiene el marco de lectura. Debido a la presencia de alguna distrofina, aunque sea defectuosa, el DGC es parcialmente funcional, lo que resulta en una progresión de la enfermedad más lenta y menos severa que la DMD. Los síntomas suelen aparecer más tarde en la infancia o adolescencia, y la debilidad muscular progresa de manera más gradual. La afectación cardíaca es común, y los pacientes con BMD suelen tener una esperanza de vida normal o ligeramente reducida.
Alerta Médica: El Peligro de las Terapias No Comprobadas
Ante la desesperación de enfermedades incurables como las distrofias musculares, surgen a menudo terapias alternativas sin base científica sólida. Es crucial advertir que el uso de suplementos ‘milagrosos’, dietas extremas no validadas o tratamientos experimentales no regulados puede no solo ser ineficaz, sino también peligroso. Estos pueden retrasar el acceso a terapias prometedoras basadas en la evidencia, agravar condiciones existentes o generar efectos secundarios nocivos. Siempre consulte con un equipo médico especializado antes de considerar cualquier intervención para enfermedades musculares graves.
Estrategias Terapéuticas y ‘Biohacking’ Molecular
El campo de la investigación de la distrofina y las distrofias musculares ha experimentado avances revolucionarios en las últimas décadas. Aunque no existe una cura definitiva, las estrategias actuales se centran en modificar el curso de la enfermedad, restaurar la expresión de distrofina o mitigar el daño muscular. Estas aproximaciones representan un verdadero ‘biohacking’ a nivel molecular.
Terapia Génica y Exón Skipping
Una de las estrategias más prometedoras es la terapia génica, que busca introducir una versión funcional del gen DMD en las células musculares. Debido al gran tamaño del gen DMD, se han desarrollado vectores virales (generalmente virus adenoasociados, AAV) para entregar ‘minidistrofina’ o ‘microdistrofina’, versiones más cortas pero funcionales de la proteína, a los músculos de los pacientes. Estos tratamientos están en fases avanzadas de ensayos clínicos y han mostrado resultados alentadores en la mejora de la fuerza muscular y la función.
El exon skipping es otra estrategia ingeniosa que busca corregir las mutaciones que alteran el marco de lectura. Utiliza oligonucleótidos antisentido (AON) para ‘saltar’ un exón mutado durante el proceso de empalme del ARNm. Al saltar el exón problemático, se puede restaurar el marco de lectura, permitiendo la producción de una distrofina acortada pero funcional, similar a la que se encuentra en los pacientes con BMD. Varios fármacos basados en esta tecnología ya han sido aprobados para subtipos específicos de DMD.
Edición Genómica (CRISPR/Cas9)
La tecnología de edición genómica CRISPR/Cas9 ofrece la posibilidad de corregir directamente las mutaciones en el gen DMD. Esta técnica permite cortar y pegar secuencias de ADN con una precisión sin precedentes, lo que teóricamente podría reparar el gen defectuoso en las células del paciente. Aunque aún se encuentra en etapas experimentales y presenta desafíos significativos en cuanto a la entrega y la especificidad, CRISPR/Cas9 representa una frontera emocionante en la búsqueda de una cura.
Terapias Farmacológicas y de Apoyo
Además de las terapias genéticas, se están investigando y utilizando diversas terapias farmacológicas para abordar los síntomas de la DMD. Los corticosteroides (como la prednisona o deflazacort) son el estándar de oro actual, ya que reducen la inflamación y retardan la progresión de la enfermedad, aunque con efectos secundarios significativos. Otros enfoques incluyen la modulación de la fibrosis, la mejora de la regeneración muscular y la protección contra el estrés oxidativo. La fisioterapia, la terapia ocupacional y el apoyo nutricional también son componentes cruciales del manejo integral de la enfermedad.
Biohacking Molecular: La Promesa de la Mini-Distrofina
Imagina ‘hackear’ el genoma para insertar una versión compacta pero completamente funcional de la distrofina. Esto es precisamente lo que busca la terapia de microdistrofina: utilizar virus adenoasociados (AAV) para entregar un gen de distrofina diseñado genéticamente, mucho más pequeño que el gen DMD original, pero que codifica una proteína capaz de restaurar la función del complejo distrofina-glicoproteína. Esta estrategia no busca corregir el gen defectuoso, sino proporcionar un ‘sustituto’ funcional, permitiendo que las células musculares recuperen parte de su resistencia y estabilidad. Los ensayos clínicos han mostrado una expresión robusta de microdistrofina y mejoras funcionales en pacientes, abriendo un camino esperanzador hacia la detención de la progresión de la enfermedad.
La Distrofina y el Contexto Metabólico (Glosario Ketocis)
Aunque la distrofina es una proteína estructural con una función específica en la integridad muscular, su estudio resalta la interconexión entre la estructura muscular y la salud metabólica general. En el contexto de un glosario centrado en la cetosis y el bienestar metabólico, la comprensión de la distrofina subraya varios puntos clave:
- Importancia de la Masa Muscular: La masa muscular es un tejido metabólicamente activo crucial para la homeostasis de la glucosa, la sensibilidad a la insulina y el gasto energético. Las distrofias musculares, al comprometer la integridad y función muscular, tienen un impacto profundo en el metabolismo general del individuo.
- Inflamación Crónica: La degeneración muscular en la DMD se asocia con una inflamación crónica. La inflamación sistémica es un factor conocido en la resistencia a la insulina y otras disfunciones metabólicas, un área de interés para la comunidad Ketocis.
- Salud Cardíaca: La afectación cardíaca es una causa principal de mortalidad en las distrofias musculares. La salud cardiovascular es un objetivo primordial en muchas estrategias de bienestar, incluyendo las relacionadas con dietas cetogénicas bien formuladas.
- Regeneración y Reparación: La capacidad de los músculos para regenerarse y repararse es fundamental para la adaptación al ejercicio y la resiliencia metabólica. La distrofina es indirectamente clave en este proceso al proteger la célula del daño inicial.
Si bien la dieta cetogénica no es una cura para las distrofias musculares genéticas, la optimización de la salud muscular a través de la nutrición y el ejercicio adecuado (adaptado a cada caso) puede apoyar el bienestar general. La investigación futura podría explorar cómo ciertos enfoques metabólicos pueden influir en la inflamación o la función mitocondrial en el contexto de la debilidad muscular.
Conclusión: Un Pilar de Esperanza y Conocimiento
La distrofina, esta colosal proteína anclada a la membrana de nuestras células musculares, representa mucho más que un mero componente estructural. Es un testimonio de la complejidad y la delicadeza de la maquinaria biológica, cuya ausencia o defecto puede desencadenar una cascada de eventos devastadores. A través de la lente de la distrofina, hemos explorado los intrincados lazos entre la genética, la fisiología molecular y la manifestación clínica de enfermedades que afectan profundamente la vida humana.
El camino hacia la curación de las distrofias musculares es arduo, pero los avances en terapia génica, edición genómica y exon skipping han transformado el panorama de la investigación, infundiendo una nueva esperanza. Comprender la distrofina no solo es esencial para los investigadores y clínicos, sino para cualquier persona interesada en la profunda interconexión de la salud humana, desde la escala molecular hasta el bienestar metabólico integral. La historia de la distrofina es un potente recordatorio de que, incluso ante los desafíos biológicos más grandes, el conocimiento y la innovación continúan abriendo nuevas vías para la sanación y la mejora de la calidad de vida.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.