Actina F: Citoesqueleto, Función Celular y Biohacking
Resumen Clínico Rápido
🔬 Clasificación
Filamento del citoesqueleto (microfilamento)
⚙️ Función Principal
Soporte estructural, motilidad, contracción muscular
📋 Impacto Metabólico
Mantenimiento de la integridad celular durante el ayuno/cetosis mediante ATP y autofagia
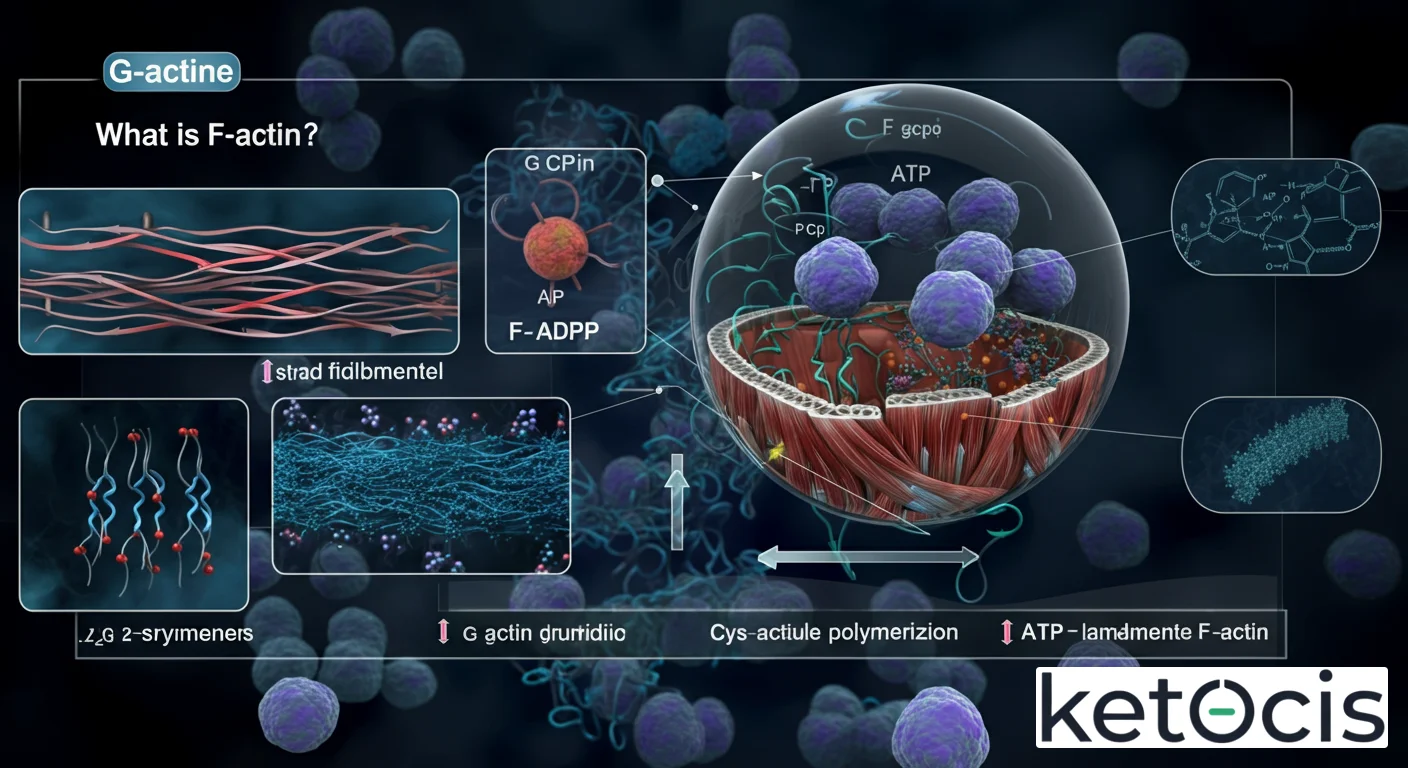
¿Qué es la Actina F? La Guía Definitiva del Citoesqueleto Celular
En el fascinante universo de la biología celular, existen componentes fundamentales que orquestan la vida a su nivel más íntimo. Entre ellos, la actina F (actina filamentosa) se erige como una de las proteínas más abundantes y versátiles, un pilar esencial del citoesqueleto que dota a nuestras células de forma, movimiento y capacidad de respuesta. Lejos de ser una mera estructura estática, la actina F es un andamiaje dinámico, en constante remodelación, que posibilita desde la contracción muscular hasta la división celular y la migración de células inmunes. Comprender su fisiología molecular y sus intrincadas interacciones es adentrarse en la mecánica fundamental de la vida.
Esta guía enciclopédica, diseñada para el Glosario Ketocis, profundizará en la composición, el propósito evolutivo, la fisiología molecular y las funciones multifacéticas de la actina F, explorando su relevancia en la salud, la enfermedad y su interacción indirecta con estados metabólicos como la cetosis y el ayuno. Prepárese para desvelar los secretos de este microfilamento vital.
Resumen Clínico
- La actina F es un polímero de actina G, formando microfilamentos esenciales del citoesqueleto eucariota.
- Su dinamismo es crucial para la motilidad celular, la contracción muscular y el mantenimiento de la forma celular.
- La regulación precisa de la polimerización y despolimerización de la actina F es vital para la fisiología y la homeostasis celular.
La actina F es una estructura estática y permanente en las células.
La actina F es una de las estructuras más dinámicas de la célula, en constante polimerización y despolimerización, adaptándose a las necesidades cambiantes del entorno celular y la actividad fisiológica.
Propósito Evolutivo y Estructural de la Actina F
La presencia de la actina en prácticamente todas las células eucariotas, desde las levaduras hasta los mamíferos, subraya su importancia fundamental y su conservación evolutiva. Su origen se remonta a los primeros eucariotas, donde probablemente desempeñó un papel crucial en la adquisición de la complejidad celular. El propósito evolutivo primordial de la actina F es proporcionar un marco estructural adaptable que permita a la célula interactuar con su entorno, responder a estímulos y realizar funciones complejas que van más allá de la mera existencia pasiva. Antes del desarrollo de estructuras más rígidas, la actina ofreció la flexibilidad necesaria para la endocitosis, la fagocitosis y, eventualmente, la motilidad. Esta adaptabilidad es lo que la ha convertido en un componente indispensable para la vida multicelular y la especialización de los tejidos.
Estructuralmente, la actina F es un polímero helicoidal formado por monómeros de actina G (globular). Estos monómeros se ensamblan cabeza con cola, formando dos protofilamentos que se enrollan entre sí en una doble hélice, creando un filamento con polaridad definida, es decir, un extremo ‘más’ (de crecimiento rápido) y un extremo ‘menos’ (de crecimiento lento). Esta polaridad es crucial para la direccionalidad de los procesos celulares que dependen de la actina, como el movimiento de motores moleculares o el crecimiento diferencial del filamento. La capacidad de la actina F para formar redes, haces y geles de diversas arquitecturas le permite cumplir una amplia gama de funciones estructurales y dinámicas dentro de la célula, actuando como un verdadero esqueleto interno y un sistema de ‘carreteras’ intracelulares.
Fisiología Molecular de la Actina F: De Monómero a Filamento
La Transformación de Actina G a Actina F
El ciclo de vida de la actina F comienza con la actina G, una proteína globular de aproximadamente 42 kDa que constituye el monómero básico. Cada monómero de actina G tiene un sitio de unión para ATP (adenosín trifosfato) o ADP (adenosín difosfato), siendo el ATP el estado preferido para su polimerización. La polimerización es un proceso altamente regulado que se inicia con una fase de nucleación, donde unos pocos monómeros de actina G se asocian para formar un núcleo estable. Una vez formado este núcleo, la elongación procede rápidamente, con la adición de más monómeros de actina G-ATP a ambos extremos del filamento, aunque preferentemente al extremo ‘más’.
Durante o poco después de la incorporación al filamento, el ATP unido a la actina G se hidroliza a ADP y fosfato inorgánico (Pi). Esta hidrólisis de ATP a ADP-Pi, y la posterior liberación de Pi, induce un cambio conformacional en los monómeros de actina dentro del filamento, afectando su afinidad por otros monómeros y su estabilidad. Los filamentos con actina-ADP son intrínsecamente menos estables y más propensos a la despolimerización, especialmente en el extremo ‘menos’. Este ciclo de polimerización (con ATP) y despolimerización (de monómeros con ADP) es lo que confiere a los filamentos de actina su notable dinamismo y la capacidad de remodelarse rápidamente en respuesta a las necesidades celulares. La hidrólisis de ATP es, por tanto, el motor molecular que impulsa la dinámica de la actina F.
Proteínas Asociadas a la Actina (ABP)
La increíble versatilidad de la actina F no sería posible sin la acción coordinada de una vasta colección de proteínas asociadas a la actina (ABP, por sus siglas en inglés). Estas proteínas regulan cada aspecto de la vida del filamento, desde su nucleación y elongación hasta su ramificación, corte, entrecruzamiento y despolimerización. Algunas de las ABP más importantes incluyen:
- Proteínas de Nucleación: Complejo ARP2/3 y forminas. El complejo ARP2/3 nuclea filamentos ramificados en ángulos de 70 grados, crucial para estructuras como los lamellipodios. Las forminas nuclean filamentos rectos y no ramificados, importantes para los haces de estrés.
- Proteínas de Elongación: Profilina. Se une a la actina G-ADP, promueve el intercambio de ADP por ATP y facilita la adición de actina G-ATP al extremo ‘más’.
- Proteínas de Despolimerización y Corte: Cofilin. Se une a filamentos de actina-ADP, torciendo el filamento y promoviendo su fragmentación y despolimerización en el extremo ‘menos’.
- Proteínas de Capping (Cubierta): Proteínas de capping (como CapZ). Se unen al extremo ‘más’ de los filamentos, inhibiendo el crecimiento y estabilizando el filamento, lo que permite la creación de filamentos de longitud definida.
- Proteínas de Entrecruzamiento: Fimbrina, alfa-actinina, filamina. Organizan los filamentos de actina en haces paralelos (fimbrina, alfa-actinina) o redes tridimensionales (filamina), proporcionando diferentes propiedades mecánicas.
- Proteínas Motoras: Miosinas. Utilizan la energía de la hidrólisis de ATP para ‘caminar’ a lo largo de los filamentos de actina, generando fuerza y movimiento, como en la contracción muscular o el transporte de vesículas.
La interacción entre la actina F y estas ABP permite a la célula construir y deconstruir rápidamente estructuras de actina complejas en respuesta a señales internas y externas, adaptándose a un entorno en constante cambio.
Funciones Clave de la Actina F en la Fisiología Celular
La actina F es un actor principal en una miríada de procesos celulares, cada uno esencial para la vida y la función de un organismo. Su versatilidad la convierte en un componente indispensable para la supervivencia y la especialización celular.
1. Motilidad Celular y Migración
La capacidad de las células para moverse y migrar es fundamental para el desarrollo embrionario, la cicatrización de heridas, la respuesta inmune y, lamentablemente, la metástasis tumoral. La actina F es el motor principal detrás de la motilidad celular. En células que se arrastran, la polimerización de la actina en el borde de ataque genera una protrusión (como los lamellipodios o los filopodios), empujando la membrana plasmática hacia adelante. Simultáneamente, los filamentos de actina interactúan con las proteínas motoras de miosina para generar fuerzas contráctiles en la parte posterior de la célula, permitiendo que el cuerpo celular avance. Este proceso coordinado de protrusión, adhesión y contracción impulsa el movimiento celular direccional.
2. Contracción Muscular
Quizás la función más conocida de la actina F es su papel central en la contracción de las células musculares. En el músculo esquelético, los filamentos de actina F forman los ‘filamentos delgados’ de las miofibrillas, interactuando con los ‘filamentos gruesos’ de miosina II. Durante la contracción, las cabezas de miosina se unen a la actina, hidrolizan ATP y pivotan, tirando de los filamentos de actina unos sobre otros, lo que acorta el sarcómero y, en última instancia, el músculo entero. Este mecanismo de ‘deslizamiento de filamentos’ es un ejemplo paradigmático de cómo la actina F convierte la energía química en trabajo mecánico.
3. Citoesqueleto y Soporte Estructural
La actina F es un componente clave del citoesqueleto, la red tridimensional de filamentos proteicos que proporciona a la célula su forma, resistencia mecánica y organiza sus componentes internos. Los filamentos de actina forman una densa red bajo la membrana plasmática, conocida como córtex celular, que confiere rigidez y elasticidad a la superficie celular. Esta red es crucial para resistir el estrés mecánico y mantener la integridad celular. Además, los filamentos de actina ayudan a posicionar orgánulos, como el núcleo y las mitocondrias, y a mantener la polaridad celular, esencial para la función de muchas células epiteliales y neuronales.
4. División Celular (Citocinesis)
Durante la fase final de la división celular, conocida como citocinesis, la actina F juega un papel indispensable. Después de que los cromosomas se han segregado a los polos opuestos de la célula, se forma un anillo contráctil de actina y miosina II justo debajo de la membrana plasmática ecuatorial. La contracción de este anillo, impulsada por la interacción actina-miosina, estrangula la célula madre en dos células hijas, asegurando una distribución equitativa del citoplasma y los orgánulos. Sin la actina F, la división celular completa sería imposible.
5. Transporte Intracelular y Señalización
Aunque los microtúbulos son más conocidos por su papel en el transporte de larga distancia, los filamentos de actina también sirven como ‘autopistas’ para el movimiento de vesículas, orgánulos y complejos macromoleculares a distancias más cortas, especialmente en la periferia celular. Las miosinas de clase I y V son motores que se desplazan a lo largo de los filamentos de actina, transportando su carga. Además, la actina F participa activamente en la señalización celular, actuando como un sensor de fuerzas mecánicas (mecanotransducción) y transmitiendo señales desde la membrana plasmática al núcleo, afectando la expresión génica y el destino celular.
El Rol de la Actina F en la Salud y la Enfermedad
Dada su ubicuidad y sus múltiples funciones, no es sorprendente que las disfunciones en la actina F o sus proteínas reguladoras estén implicadas en una amplia gama de patologías humanas. Las mutaciones en los genes de la actina o de las proteínas asociadas pueden llevar a miopatías (enfermedades musculares), defectos cardíacos, y trastornos neurológicos. Por ejemplo, ciertas mutaciones en la actina cardíaca pueden causar miocardiopatía dilatada o hipertrófica.
En el contexto del cáncer, la remodelación aberrante del citoesqueleto de actina es un sello distintivo de las células malignas. La capacidad de las células cancerosas para migrar, invadir tejidos circundantes y formar metástasis depende críticamente de la reorganización dinámica de su red de actina. La manipulación de la actina F se ha convertido en un objetivo terapéutico para inhibir la progresión del cáncer. De manera similar, muchos patógenos intracelulares, como bacterias (por ejemplo, Listeria monocytogenes) y virus, han evolucionado mecanismos sofisticados para secuestrar y manipular el citoesqueleto de actina del huésped para su propia motilidad dentro de la célula o para propagarse a células adyacentes.
Actina F, Cetosis y Ayuno: Mantenimiento Celular en Estados Metabólicos
Mientras que la actina F no es directamente un objetivo o un producto de la cetosis o el ayuno, su función y mantenimiento son intrínsecamente ligados a la salud metabólica general de la célula. Durante estados de cetosis y ayuno, el cuerpo experimenta un cambio fundamental en el uso de combustible, pasando de la glucosa a los cuerpos cetónicos y los ácidos grasos como fuentes de energía. Este cambio requiere una adaptación celular significativa, y el mantenimiento de la integridad estructural y funcional de la célula es primordial.
La síntesis de proteínas, incluida la actina G, requiere energía y aminoácidos. Aunque el ayuno prolongado puede llevar a la degradación proteica, el ayuno intermitente y la cetosis nutricional son conocidos por inducir mecanismos de reparación y reciclaje celular, como la autofagia. La autofagia es un proceso catabólico fundamental para la renovación de componentes celulares dañados o viejos, lo que incluye proteínas del citoesqueleto. Al reciclar estos componentes, la autofagia contribuye a la salud general de la célula y asegura un suministro de aminoácidos para la síntesis de nuevas proteínas, manteniendo así un fondo de actina G disponible para la formación de actina F.
Además, la dinámica de la actina F es un proceso que consume ATP. La hidrólisis de ATP impulsa la polimerización, la acción de las miosinas y la remodelación general del filamento. En un estado de cetosis, donde las mitocondrias están optimizadas para la producción de ATP a partir de cuerpos cetónicos, se asegura un suministro energético robusto para mantener la maquinaria de la actina F en funcionamiento. Por lo tanto, aunque no hay una interacción directa ‘cetosis-actina F’ única, un metabolismo celular saludable y eficiente, promovido por la cetosis y el ayuno, apoya indirectamente la capacidad de la célula para mantener y remodelar su citoesqueleto de actina F, crucial para su función y resiliencia.
Biohacking y Actina F: Nutrición para la Resiliencia Celular
Para optimizar la salud de tu citoesqueleto de actina, concéntrate en la nutrición celular integral. Asegura un consumo adecuado de proteínas de alta calidad para proporcionar los aminoácidos necesarios para la síntesis de actina G. Además, apoya la función mitocondrial con nutrientes como el magnesio, el complejo B y la coenzima Q10, ya que una producción eficiente de ATP es vital para la dinámica de la actina F. El ejercicio regular, especialmente el entrenamiento de fuerza, estimula la remodelación muscular y la síntesis proteica, lo que indirectamente beneficia la integridad y la función de la actina en las células musculares y otras.
Optimización y Mantenimiento de la Red de Actina F
Mantener una red de actina F funcional y adaptable es sinónimo de salud celular. La optimización comienza a nivel fundamental con una nutrición adecuada. Los aminoácidos esenciales son los bloques de construcción de la actina G, por lo que una dieta rica en proteínas de alta calidad es indispensable. Además, la producción de ATP, el combustible de la dinámica de la actina, depende de la salud mitocondrial, que se apoya con micronutrientes como el magnesio, el zinc y las vitaminas del grupo B, así como antioxidantes que protegen las mitocondrias del estrés oxidativo.
El ejercicio físico regular también juega un papel crucial. La contracción muscular, que depende de la actina F, no solo fortalece los músculos sino que también envía señales a las células para remodelar y mantener sus citoesqueletos. La carga mecánica estimula la síntesis de proteínas y la renovación celular, lo que es beneficioso para la red de actina. Finalmente, la promoción de procesos de autofagia y reciclaje celular, a través de estrategias como el ayuno intermitente o la restricción calórica, ayuda a eliminar componentes celulares dañados, incluyendo filamentos de actina viejos o disfuncionales, y a reciclar sus componentes para construir nuevas estructuras. Este ciclo de degradación y síntesis es esencial para la resiliencia y la adaptación celular.
Alerta Médica: Mitos y Riesgos de la Manipulación Directa de la Actina
Existe el mito de que ciertos suplementos pueden ‘fortalecer’ directamente la actina F o ‘mejorar’ el citoesqueleto. La realidad es que la manipulación directa de la actina F con compuestos externos es extremadamente compleja y, en la mayoría de los casos, perjudicial. Toxinas como la faloidina (de hongos venenosos) y la citocalasina B son conocidas por unirse directamente a la actina F, estabilizándola o desestabilizándola, respectivamente, con consecuencias celulares devastadoras y letales. Por ello, la ‘optimización’ de la actina F debe abordarse a través de un apoyo metabólico y nutricional general, y no mediante la ingestión de sustancias que prometen una ‘mejora’ directa y no validada científicamente. Siempre priorice un estilo de vida saludable y consulte a profesionales médicos.
Conclusión: La Actina F como Maestra de la Adaptación Celular
La actina F, o actina filamentosa, trasciende la definición de una simple proteína estructural para emerger como una verdadera maestra de la adaptación celular. Desde su humilde origen como monómero globular, la actina G, hasta su ensamblaje en complejos y dinámicos microfilamentos, su papel es indispensable para la vida eucariota. Es el andamiaje que da forma a la célula, el motor que impulsa su movimiento, el director que orquesta la división y el mensajero que transmite señales vitales.
Su intrincada regulación por un sinfín de proteínas asociadas y su dependencia de la energía metabólica subrayan la interconexión de todos los sistemas celulares. Comprender la actina F no es solo entender una proteína; es desentrañar los mecanismos fundamentales de la biología, la fisiología y la patología. Para el Glosario Ketocis, la lección es clara: el mantenimiento de un citoesqueleto de actina robusto y funcional es un reflejo de la salud metabólica general, un testimonio de la resiliencia celular que una nutrición adecuada y un estilo de vida consciente pueden fomentar. La investigación futura continuará desvelando nuevas facetas de esta proteína omnipresente, profundizando nuestra apreciación por la complejidad y elegancia de la vida a nivel molecular.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.