Antígeno: Guía Definitiva de Inmunología | Glosario Ketocis
Resumen Clínico Rápido
🔬 Clasificación
Exógeno, Endógeno, Autoantígeno, Tumoral
⚙️ Función
Inducir respuesta inmune específica
📋 Impacto
Base de vacunas, diagnóstico y autoinmunidad
¿Qué es un Antígeno? La Clave Molecular de tu Defensa Inmune
En el vasto y complejo universo de la biología humana, el sistema inmunitario se erige como un guardián incansable, una fortaleza biológica diseñada para protegernos de un sinfín de amenazas, desde virus microscópicos hasta células cancerosas mutantes. En el corazón de esta intrincada red de defensa se encuentra un concepto fundamental: el antígeno. Para el Glosario Ketocis, comprender qué es un antígeno no solo es una cuestión de rigor científico, sino una puerta de entrada para entender cómo nuestro cuerpo interactúa con su entorno, cómo se defiende y cómo podemos optimizar su funcionamiento.
Como Investigador Médico PhD y Copywriter Clínico, mi objetivo es desentrañar la esencia del antígeno, desde su definición molecular hasta su impacto en la salud y la enfermedad, y cómo su conocimiento puede influir en estrategias de biohacking y bienestar metabólico. Prepárate para un viaje fascinante al epicentro de la inmunología.
Resumen Clínico
- Punto clave 1: Un antígeno es cualquier molécula que el sistema inmunitario reconoce como extraña o potencialmente peligrosa, desencadenando una respuesta inmune.
- Punto clave 2: La especificidad de la respuesta inmune se basa en el reconocimiento de pequeñas regiones antigénicas llamadas epítopos.
- Punto clave 3: Los antígenos son fundamentales para la vacunación, el diagnóstico de enfermedades y la comprensión de trastornos autoinmunes y alergias.
La Definición Fundamental y el Propósito Evolutivo del Antígeno
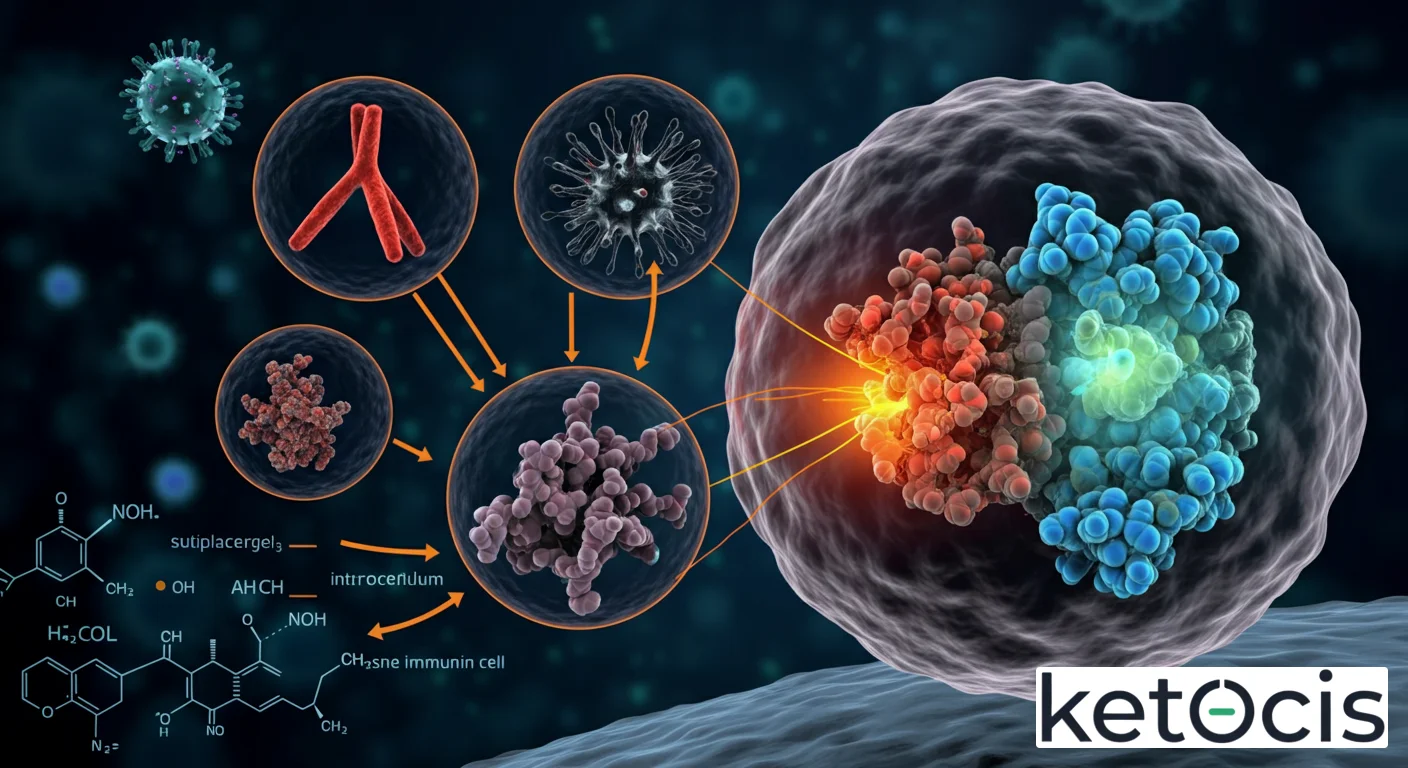
Un antígeno (del griego anti-, ‘contra’, y -genos, ‘generador’) es, en su definición más pura, cualquier sustancia que puede provocar una respuesta inmunitaria. Esta sustancia puede ser una proteína, un polisacárido, un lípido, un ácido nucleico o incluso una molécula más pequeña (un hapteno, que se vuelve antigénico al unirse a una proteína transportadora). Lo que distingue a un antígeno es su capacidad para ser reconocido por los receptores específicos de las células inmunitarias, como los anticuerpos de las células B o los receptores de células T (TCRs).
Desde una perspectiva evolutiva, la existencia de los antígenos es intrínseca a la supervivencia de los organismos multicelulares. La vida en la Tierra está inmersa en un mar de microorganismos, muchos de los cuales son patógenos. La capacidad de discernir entre lo ‘propio’ (self) y lo ‘no propio’ (non-self) es una adaptación crucial. Los antígenos son las ‘señales de alarma’ moleculares que permiten al sistema inmunitario identificar y neutralizar amenazas, ya sean bacterias invasoras, virus replicantes o células propias que han mutado y se han vuelto cancerosas.
El propósito evolutivo del antígeno es doble: primero, permitir la detección temprana de agentes patógenos o células aberrantes; y segundo, guiar la especificidad de la respuesta inmune, asegurando que el ataque se dirija precisamente contra la amenaza y minimizando el daño a los tejidos sanos del huésped. Sin esta capacidad de reconocimiento antigénico, la vida tal como la conocemos sería inviable, sucumbiendo rápidamente a infecciones incontrolables o a la proliferación celular desregulada.
Todos los antígenos son peligrosos y deben ser eliminados por el sistema inmune.
El sistema inmune desarrolla tolerancia a muchos antígenos inofensivos (alimentos, microbiota). La clave es la discriminación entre 'propio' y 'no propio', y la capacidad de responder adecuadamente a las amenazas sin atacar lo benigno.
La Fisiología Molecular del Reconocimiento Antigénico: Un Balet Preciso
El reconocimiento de un antígeno no es un evento aleatorio, sino un proceso de una precisión molecular asombrosa, orquestado por componentes especializados del sistema inmunitario. Las células inmunes no ‘ven’ el antígeno completo en su totalidad, sino que reconocen fragmentos específicos llamados epítopos o determinantes antigénicos. Un solo antígeno, especialmente si es una proteína grande, puede contener múltiples epítopos diferentes, cada uno capaz de unirse a un anticuerpo o receptor de célula T distinto.
El Papel Crucial de las Células Presentadoras de Antígenos (APCs)
Para que las células T (linfocitos T), que son los directores de la respuesta inmune celular, puedan reconocer un antígeno, este debe ser ‘presentado’ a ellas por las células presentadoras de antígeno (APCs), como las células dendríticas, los macrófagos y los linfocitos B. Las APCs internalizan el antígeno, lo procesan en péptidos más pequeños y luego exhiben estos péptidos en su superficie, anclados en moléculas del Complejo Mayor de Histocompatibilidad (MHC).
- MHC de Clase I: Presente en casi todas las células nucleadas del cuerpo, muestra péptidos derivados de proteínas intracelulares (endógenas), como las de virus o células tumorales. Son reconocidos por los linfocitos T citotóxicos (CD8+), que están programados para destruir esas células infectadas o anormales.
- MHC de Clase II: Se encuentra principalmente en las APCs profesionales. Presenta péptidos derivados de proteínas extracelulares (exógenas) que han sido internalizadas y procesadas. Son reconocidos por los linfocitos T cooperadores (CD4+), que orquestan la respuesta inmune activando a otras células inmunes.
Los linfocitos B, por otro lado, pueden reconocer antígenos directamente a través de sus receptores de membrana (anticuerpos de superficie), sin necesidad de una presentación MHC. Una vez activados, los linfocitos B pueden diferenciar en células plasmáticas que secretan grandes cantidades de anticuerpos solubles, los cuales se unirán a los antígenos para neutralizarlos o marcarlos para su destrucción.
Tipos de Antígenos: Una Clasificación para la Claridad
La diversidad de antígenos es tan vasta como la de las amenazas biológicas. Se pueden clasificar según su origen o su relación con el huésped:
- Antígenos Exógenos: Son antígenos que entran al cuerpo desde el exterior. Incluyen componentes de bacterias (como toxinas, proteínas de la pared celular), virus (proteínas de la cápside o envoltura), hongos, parásitos, polen, polvo y alimentos. Son internalizados por las APCs y presentados vía MHC de Clase II.
- Antígenos Endógenos: Son antígenos generados dentro de las células del cuerpo. Esto incluye proteínas virales sintetizadas dentro de una célula infectada o proteínas mutadas de células tumorales. Se presentan vía MHC de Clase I.
- Autoantígenos: Son componentes normales de las células del propio cuerpo que, bajo ciertas circunstancias (como en enfermedades autoinmunes), son erróneamente reconocidos como extraños por el sistema inmunitario, provocando un ataque contra los propios tejidos. Ejemplos incluyen la mielina en la esclerosis múltiple o las proteínas de las articulaciones en la artritis reumatoide.
- Antígenos Tumorales: Son proteínas o carbohidratos expresados por células cancerosas que las distinguen de las células normales. Pueden ser proteínas mutadas, proteínas normalmente expresadas solo durante el desarrollo fetal, o proteínas normales sobreexpresadas. Son cruciales para el desarrollo de inmunoterapias contra el cáncer.
- Superantígenos: Una clase especial de antígenos (a menudo toxinas bacterianas) que pueden activar un gran número de linfocitos T de manera inespecífica, sin necesidad de un procesamiento antigénico convencional. Esto conduce a una liberación masiva de citocinas y una respuesta inflamatoria sistémica severa, como en el choque tóxico.
- Haptenos: Pequeñas moléculas que por sí solas no son inmunogénicas (no pueden inducir una respuesta inmune), pero se vuelven antigénicas cuando se unen a una proteína portadora más grande en el cuerpo. Ejemplos incluyen algunos fármacos (como la penicilina en personas alérgicas) o metales pesados.
La Respuesta Inmune: Primaria y Secundaria al Antígeno
La exposición a un antígeno desencadena una respuesta inmunitaria que puede ser primaria o secundaria, cada una con características distintivas:
- Respuesta Inmune Primaria: Ocurre en el primer contacto con un antígeno. Es más lenta y menos potente. Las células B y T vírgenes se activan, proliferan y se diferencian en células efectoras (por ejemplo, células plasmáticas secretoras de anticuerpos) y células de memoria. La producción de anticuerpos (principalmente IgM al principio, luego IgG) es gradual y los títulos son bajos.
- Respuesta Inmune Secundaria (Memoria Inmunológica): Se desencadena en exposiciones posteriores al mismo antígeno. Es más rápida, más fuerte y más duradera debido a la presencia de un gran número de células de memoria B y T específicas para ese antígeno. La producción de anticuerpos es mucho mayor y predomina la IgG, con mayor afinidad por el antígeno. Esta es la base de la inmunidad protectora conferida por las vacunas y por haber superado una infección.
Esta distinción es vital para entender la eficacia de las vacunas, que buscan generar una respuesta primaria controlada para preparar al sistema inmune para una respuesta secundaria rápida y eficaz ante una infección real.
Antígenos en la Patología y la Medicina: De la Enfermedad a la Cura
El estudio de los antígenos es fundamental en múltiples campos de la medicina:
- Enfermedades Autoinmunes: Como mencionamos, la respuesta a autoantígenos es el sello distintivo de estas condiciones devastadoras, donde el sistema inmune ataca erróneamente los propios tejidos del cuerpo. Comprender qué autoantígenos están implicados es clave para el diagnóstico y el desarrollo de terapias específicas.
- Alergias: Las alergias son respuestas inmunes exageradas a antígenos inofensivos del ambiente, conocidos como alérgenos (por ejemplo, polen, ácaros del polvo, ciertos alimentos). La identificación del alérgeno específico es crucial para el manejo y la desensibilización.
- Cáncer: Los antígenos tumorales son el talón de Aquiles de las células cancerosas. La inmunoterapia contra el cáncer, como los inhibidores de puntos de control o las terapias con células CAR-T, explotan el reconocimiento de estos antígenos para dirigir el ataque inmunitario contra los tumores.
- Enfermedades Infecciosas y Vacunas: Las vacunas funcionan introduciendo antígenos (o instrucciones para producirlos) de un patógeno para estimular una respuesta inmune protectora sin causar la enfermedad. La elección de antígenos adecuados es el pilar del diseño vacunal.
- Diagnóstico: La detección de antígenos específicos en muestras biológicas es una herramienta diagnóstica poderosa. Por ejemplo, las pruebas rápidas de antígenos para COVID-19 detectan proteínas virales, o la detección del antígeno prostático específico (PSA) para el cáncer de próstata. Inversamente, la detección de anticuerpos contra antígenos específicos puede indicar una infección pasada o presente.
Biohacking del Reconocimiento Antigénico y la Inmunidad
La optimización de la respuesta inmune, una meta central del biohacking, pasa por comprender cómo se presentan y reconocen los antígenos. Estrategias como el ayuno intermitente o la dieta cetogénica pueden influir en la autofagia, un proceso celular que recicla componentes dañados y puede afectar la presentación de antígenos endógenos. Al mejorar la autofagia, se podría optimizar la eliminación de células disfuncionales o infectadas, presentando sus antígenos de manera más eficiente y fortaleciendo la vigilancia inmunológica contra amenazas internas. Es una sutil pero profunda interconexión entre el metabolismo y la inmunovigilancia.
Antígenos y el Contexto Metabólico: Una Conexión Emergente
Aunque los antígenos son moléculas per se, el contexto metabólico del organismo influye profundamente en la forma en que se presentan, reconocen y responden a ellos. La dieta, el estado nutricional y los ciclos metabólicos como el ayuno y la cetosis pueden modular la función de las células inmunes y, por ende, la eficacia de la respuesta antigénica.
- Inflamación y Antígenos: Estados proinflamatorios crónicos, a menudo asociados con disfunción metabólica (resistencia a la insulina, obesidad), pueden alterar la presentación antigénica y la diferenciación de las células T. Una inflamación desregulada puede llevar a respuestas inmunes ineficaces o incluso autoimunes.
- Autofagia y Procesamiento Antigénico: La autofagia, un proceso de reciclaje celular que se potencia durante el ayuno y la cetosis, juega un papel crucial en el procesamiento de antígenos endógenos. Una autofagia eficiente asegura que los péptidos antigénicos derivados de componentes celulares dañados o patógenos intracelulares sean presentados correctamente en las moléculas MHC de Clase I, potenciando la respuesta de las células T citotóxicas.
- Metabolismo de Lípidos y Células Inmunes: El metabolismo de los lípidos, alterado en la cetosis, influye en la composición de las membranas celulares y en la señalización intracelular de las células inmunes. Esto puede afectar la expresión de receptores antigénicos y la capacidad de las células para interactuar con los antígenos y las APCs. Por ejemplo, los cuerpos cetónicos pueden actuar como moléculas de señalización que modulan la activación de las células T y la producción de citocinas.
- Microbiota y Antígenos Alimentarios: La microbiota intestinal, influenciada por la dieta (incluida la cetogénica), produce una vasta gama de antígenos. Un equilibrio saludable de la microbiota es vital para la tolerancia inmunológica a los antígenos alimentarios y para prevenir la sensibilización a componentes de la dieta que podrían desencadenar respuestas inflamatorias o alérgicas.
En resumen, si bien un antígeno es una entidad molecular específica, la respuesta del cuerpo a él no ocurre en un vacío. El estado metabólico del individuo actúa como un modulador poderoso, determinando la eficiencia, especificidad y la resolución de la respuesta inmune.
Advertencia Médica: El Mito de ‘Todos los Antígenos son Malos’
Existe un mito común de que cualquier sustancia reconocida como ‘antígeno’ es inherentemente dañina o debe ser eliminada. Esto es un error peligroso. Muchos antígenos son inofensivos (como los componentes de alimentos o la flora comensal) y el sistema inmune desarrolla tolerancia hacia ellos. De hecho, la exposición controlada a ciertos antígenos (como en las vacunas) es vital para construir una inmunidad robusta. El verdadero peligro radica en un sistema inmune que falla en distinguir entre antígenos benignos y patógenos, o que ataca a los autoantígenos, resultando en alergias, autoinmunidad o inmunodeficiencia. No todos los antígenos son ‘enemigos’; muchos son simplemente ‘información’ que el sistema inmune debe procesar correctamente.
Conclusión: El Antígeno como Pilar de la Inmunología y la Salud
El antígeno es mucho más que una simple molécula extraña; es el lenguaje fundamental a través del cual nuestro sistema inmunitario interpreta el mundo, discrimina entre lo propio y lo ajeno, y decide cuándo montar una defensa. Su estudio ha revolucionado la medicina, permitiéndonos desarrollar vacunas que han erradicado enfermedades, diagnosticar patologías con precisión, y concebir terapias innovadoras para el cáncer y las enfermedades autoinmunes.
Para el biohacker y el entusiasta del bienestar, comprender el antígeno y su interacción con el sistema inmune, especialmente en el contexto de la salud metabólica, abre nuevas avenidas para la optimización. Al modular nuestra dieta, estilo de vida y entorno, podemos influir en cómo nuestros cuerpos procesan y responden a los antígenos, fortaleciendo nuestra resiliencia y promoviendo una salud duradera. El antígeno no es solo un concepto biológico; es una clave maestra para desvelar los secretos de nuestra propia inmunidad y longevidad.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.