Chaperonas Moleculares: Guía Definitiva para el Plegamiento Proteico
Resumen Clínico Rápido
🔬 Clasificación
Proteínas de choque térmico (Hsp) y otras familias.
⚙️ Función
Asistencia en el plegamiento, ensamblaje y transporte proteico; prevención de agregación.
📋 Impacto
Mantenimiento de la proteostasis, prevención de enfermedades por mal plegamiento, longevidad.
¿Qué es una Chaperona Molecular? La Arquitectura Invisible de la Vida Celular
En el vasto y complejo universo de la célula, donde billones de proteínas realizan intrincadas funciones cada segundo, existe una clase de guardianes silenciosos, pero absolutamente esenciales: las chaperonas moleculares. Estas proteínas especializadas no son enzimas en el sentido tradicional de catalizar reacciones químicas directas, sino más bien asistentes cruciales que aseguran que otras proteínas adopten y mantengan su forma tridimensional funcional, un proceso conocido como plegamiento proteico. Sin su intervención, la maquinaria celular colapsaría bajo una avalancha de proteínas mal plegadas y agregadas, lo que subraya su papel indispensable en la homeostasis proteica y, en última instancia, en la vida misma.
Desde la síntesis de una nueva cadena de aminoácidos en el ribosoma hasta su destino final, ya sea en el citoplasma, el núcleo o una organela específica, cada proteína debe navegar un paisaje energético complejo para alcanzar su conformación nativa. Este proceso es sorprendentemente propenso a errores, especialmente en el entorno celular abarrotado y a menudo estresante. Las chaperonas moleculares actúan como una red de seguridad, previniendo el mal plegamiento, facilitando el plegamiento correcto y, en ocasiones, incluso ayudando a las proteínas dañadas a refoldarse o dirigiéndolas hacia vías de degradación cuando la reparación es inviable. Comprender su fisiología es adentrarse en uno de los pilares fundamentales de la biología celular y la salud humana.
Resumen Clínico
- Punto clave 1: Las chaperonas moleculares son proteínas esenciales que asisten a otras proteínas en su correcto plegamiento tridimensional.
- Punto clave 2: Previenen la agregación de proteínas mal plegadas y son cruciales para mantener la homeostasis proteica celular.
- Punto clave 3: Su función es vital para la respuesta al estrés celular, la prevención de enfermedades neurodegenerativas y la longevidad.
Propósito Evolutivo: La Imperiosa Necesidad de un Guardián Celular
La vida, tal como la conocemos, depende de la precisión milimétrica de las proteínas. Cada enzima, cada receptor, cada proteína estructural o de transporte debe adoptar una forma específica para realizar su trabajo. Sin embargo, el proceso de plegamiento de una cadena lineal de aminoácidos en una estructura tridimensional funcional es intrínsecamente desafiante. El entorno celular es un caldo de cultivo denso, donde las concentraciones de macromoléculas son extremadamente altas, aumentando el riesgo de interacciones erróneas y agregación de proteínas hidrofóbicas expuestas.
Desde una perspectiva evolutiva, la aparición de las chaperonas moleculares fue una adaptación crítica. Permitió a las células manejar el estrés térmico, oxidativo y otras condiciones adversas que podrían desnaturalizar o mal plegar las proteínas. Imaginen un mundo sin ellas: cada vez que una célula experimentara un aumento de temperatura o un cambio en su metabolismo, un gran porcentaje de sus proteínas se volverían no funcionales, llevando a la muerte celular. Las chaperonas, por lo tanto, no son un lujo, sino una necesidad fundamental que garantizó la estabilidad y la resiliencia de los sistemas biológicos a lo largo de millones de años de evolución.
Además, muchas proteínas, incluso en condiciones óptimas, no pueden plegarse de manera eficiente por sí mismas. Requieren la guía de las chaperonas desde el momento en que emergen del ribosoma. Este papel de “niñera molecular” es vital para evitar que las regiones hidrofóbicas, que normalmente estarían enterradas en el interior de la proteína plegada, interactúen de forma inapropiada con otras moléculas o con otras regiones hidrofóbicas de la misma proteína, lo que llevaría a un plegamiento incorrecto o a la formación de agregados insolubles, que son la base de muchas patologías.
Las chaperonas solo actúan cuando una célula está bajo estrés o cuando las proteínas ya están dañadas.
Las chaperonas son fundamentales para el plegamiento correcto de muchas proteínas recién sintetizadas, incluso en condiciones celulares normales, además de su rol crucial en la respuesta al estrés proteotóxico.
Fisiología Molecular: Mecanismos de Acción y Diversidad de Chaperonas
El término “chaperona” fue acuñado por primera vez en 1978 para describir proteínas que asistían en el ensamblaje de nucleosomas sin ser parte de la estructura final. Desde entonces, el concepto se ha expandido enormemente, revelando una familia diversa de proteínas con mecanismos de acción variados, pero con el objetivo común de mantener la proteostasis (homeostasis proteica) celular.
El Ciclo de Plegamiento Asistido
La mayoría de las chaperonas operan mediante ciclos dependientes de ATP, donde se unen y liberan repetidamente de sus proteínas cliente. Este ciclo permite que la chaperona asuma diferentes conformaciones que facilitan el plegamiento. Típicamente, una chaperona se une a una proteína en un estado parcialmente plegado o desplegado, a menudo reconociendo regiones hidrofóbicas expuestas. La hidrólisis de ATP induce un cambio conformacional en la chaperona, lo que puede resultar en la liberación de la proteína cliente o en la alteración de su conformación para promover un plegamiento más eficiente. Este proceso se repite hasta que la proteína cliente alcanza su estado nativo o es entregada a otra chaperona o a un sistema de degradación.
Las Grandes Familias de Chaperonas
Dentro del vasto repertorio de chaperonas moleculares, varias familias destacan por su ubicuidad y la criticidad de sus funciones:
-
Hsp70 (Heat Shock Protein 70): Esta es una de las familias de chaperonas más conservadas y abundantes. Las Hsp70 actúan tempranamente en el proceso de plegamiento, uniéndose a las cadenas polipeptídicas nacientes a medida que emergen del ribosoma. También desempeñan un papel crucial en el transporte de proteínas a través de membranas de orgánulos y en la desaglomeración de proteínas agregadas. Su función está regulada por co-chaperonas, como las proteínas con dominio J (JDPs) que estimulan la actividad ATPasa de Hsp70, y los factores de intercambio de nucleótidos (NEFs) que promueven la liberación de ADP y la unión de ATP.
-
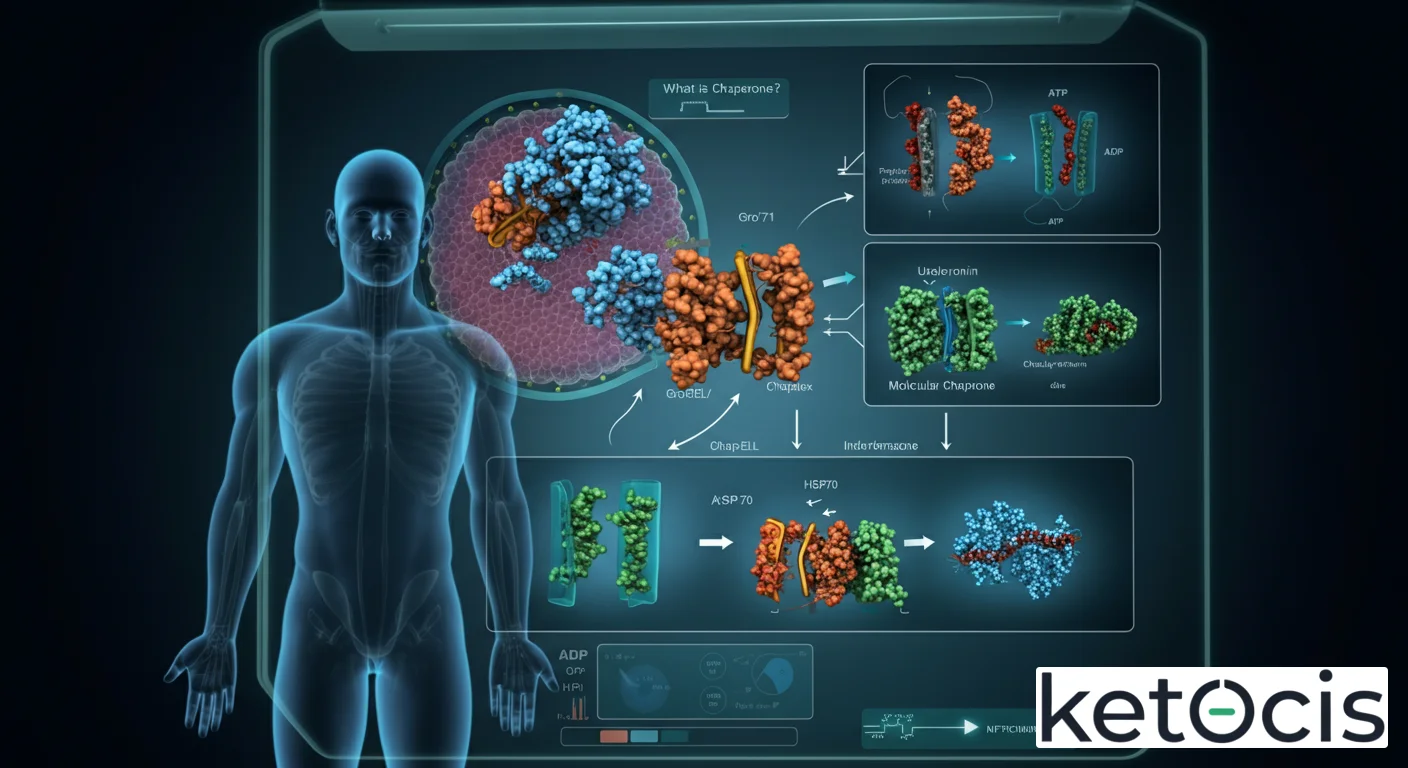
Chaperoninas (Hsp60 y CCT/TRiC): Estas chaperonas forman estructuras en forma de barril o jaula, proporcionando un microambiente aislado para el plegamiento de proteínas. La chaperonina procariota más estudiada es GroEL/GroES, mientras que en eucariotas se encuentra la CCT (Chaperonin Containing TCP-1) o TRiC (TCP-1 Ring Complex). Actúan encapsulando proteínas desplegadas o parcialmente plegadas, utilizando ciclos de hidrólisis de ATP para promover cambios conformacionales que facilitan el plegamiento en un entorno protegido, lejos de interacciones que podrían llevar a la agregación.
-
Hsp90 (Heat Shock Protein 90): A diferencia de Hsp70 y Hsp60, Hsp90 se especializa en la maduración y activación de una clientela más selecta de proteínas, incluyendo muchas quinasas, receptores de hormonas esteroideas y factores de transcripción. Estas proteínas cliente suelen ser grandes y complejas, y Hsp90 actúa como un “andamio” molecular, facilitando su ensamblaje final y su activación. Su función es especialmente crítica en la señalización celular y la respuesta a estímulos.
-
sHsps (Small Heat Shock Proteins): Estas chaperonas son ATP-independientes y actúan como “mantenedores” o “holdases”. Bajo condiciones de estrés severo, las sHsps se unen a proteínas desplegadas, previniendo su agregación irreversible y manteniéndolas en un estado que puede ser refoldado por otras chaperonas (como Hsp70) una vez que las condiciones celulares mejoran. Son particularmente importantes en la protección celular contra el estrés térmico y oxidativo.
-
Chaperonas del Retículo Endoplasmático (RE): En el RE, un compartimento crucial para la síntesis de proteínas secretadas y de membrana, chaperonas como BiP (Hsp70 del RE), calnexina y calreticulina aseguran el plegamiento y ensamblaje correctos de las proteínas antes de su exportación. Un fallo en este sistema puede desencadenar la respuesta a proteínas desplegadas (UPR), una compleja vía de señalización que intenta restaurar la homeostasis del RE o inducir la apoptosis si el estrés es insuperable.
Dato Médico de Optimización: El ayuno intermitente y la restricción calórica activan vías de respuesta al estrés celular, como la autofagia y la biogénesis mitocondrial, que están íntimamente ligadas a la expresión y actividad de chaperonas. Optimizar estos procesos mediante patrones alimenticios específicos puede mejorar la capacidad de tu cuerpo para manejar proteínas dañadas, promoviendo una mayor longevidad y resiliencia celular.
Beneficios para la Salud: Más Allá del Plegamiento Proteico
La importancia de las chaperonas moleculares trasciende el ámbito del plegamiento básico, impactando profundamente la salud y la enfermedad. Su función protectora es un baluarte contra una multitud de patologías.
Protección contra el Estrés Celular
Las chaperonas, especialmente las proteínas de choque térmico (Hsps), fueron inicialmente identificadas por su aumento de expresión en respuesta al calor. Sin embargo, su papel se extiende a casi todas las formas de estrés celular, incluyendo el estrés oxidativo, la exposición a metales pesados, la isquemia y la inflamación. Al proteger las proteínas vitales de la desnaturalización y la agregación bajo estas condiciones, las chaperonas permiten que la célula sobreviva y se recupere, un mecanismo fundamental para la resiliencia de los tejidos y órganos.
Prevención de Enfermedades Neurodegenerativas
Las enfermedades neurodegenerativas como el Alzheimer, el Parkinson, la enfermedad de Huntington y las enfermedades priónicas se caracterizan por la acumulación y agregación de proteínas mal plegadas en el cerebro. En estas condiciones, la capacidad de las chaperonas para manejar la carga de proteínas tóxicas se ve comprometida o superada. Por ejemplo, en el Alzheimer, la acumulación de la proteína beta-amiloide y la proteína tau hiperfosforilada forman agregados insolubles. Las chaperonas intentan mitigar esta toxicidad, y la modulación de su actividad representa una estrategia terapéutica prometedora para estas devastadoras enfermedades.
Inmunidad y Cáncer
En el sistema inmunitario, algunas chaperonas como Hsp70 y Hsp90 pueden actuar como moléculas de señalización extracelulares, presentadoras de antígenos o activadoras de respuestas inmunitarias. Dentro de las células, son cruciales para el plegamiento de componentes del complejo mayor de histocompatibilidad (MHC), esenciales para la presentación de antígenos. En el contexto del cáncer, muchas células tumorales sobreexpresan chaperonas para lidiar con el alto estrés metabólico y la proliferación descontrolada. Esto las convierte en blancos terapéuticos atractivos; la inhibición de chaperonas específicas como Hsp90 puede sensibilizar las células cancerosas a la quimioterapia y la radioterapia, mientras que la activación de otras puede inducir la muerte celular programada en tumores.
Longevidad y Envejecimiento
El envejecimiento se asocia con un declive gradual en la eficiencia de los sistemas de proteostasis, incluyendo la función de las chaperonas. Este deterioro contribuye a la acumulación de proteínas dañadas, al estrés oxidativo y a la disfunción celular, factores clave en el proceso de envejecimiento. La modulación genética o farmacológica de la actividad de las chaperonas ha demostrado extender la vida útil en organismos modelo como levaduras, gusanos y moscas, sugiriendo un vínculo directo entre la robustez de la red de chaperonas y la longevidad.
Mitos y Realidades sobre las Chaperonas Moleculares
Advertencia Médica: Es un error común pensar que todas las proteínas pueden ser «reparadas» por chaperonas. Si bien son altamente eficientes, su capacidad tiene límites. Una sobrecarga de proteínas mal plegadas o daños estructurales severos pueden superar la capacidad de las chaperonas, llevando a la activación de vías de degradación (como el sistema ubiquitina-proteasoma o la autofagia) o, en casos extremos, a la apoptosis celular. No son una solución universal que garantice la invulnerabilidad proteica.
Mito: Las chaperonas solo actúan cuando una célula está bajo estrés o cuando las proteínas ya están dañadas.
Realidad: Si bien las chaperonas son cruciales en la respuesta al estrés celular y en la reparación de proteínas dañadas, muchas de ellas, como las Hsp70, son constitutivamente expresadas (es decir, están presentes en la célula en todo momento) y son absolutamente esenciales para el plegamiento correcto de un gran número de proteínas recién sintetizadas, incluso en condiciones celulares normales. Muchas proteínas nunca alcanzarían su conformación nativa sin la asistencia de chaperonas desde el momento de su traducción, lo que las convierte en componentes integrales de la maquinaria de síntesis proteica.
Mito: Todas las chaperonas funcionan de la misma manera y pueden reemplazar la función de otras.
Realidad: El sistema de chaperonas es altamente diverso y especializado. Aunque comparten el objetivo general de mantener la proteostasis, las diferentes familias de chaperonas (Hsp70, Hsp60, Hsp90, sHsps, etc.) tienen mecanismos de acción distintos, reconocen diferentes tipos de proteínas cliente y operan en compartimentos celulares específicos. Hay cierta redundancia, pero también una especificidad funcional considerable. Por ejemplo, una Hsp70 no puede reemplazar la función de una chaperonina en el plegamiento de proteínas que requieren un ambiente de “jaula”, ni una Hsp90 puede encargarse del plegamiento de cadenas nacientes en el ribosoma con la misma eficacia que una Hsp70.
Perspectivas Futuras y Conclusión
El estudio de las chaperonas moleculares sigue siendo un campo vibrante de investigación, con implicaciones profundas para la medicina y la comprensión fundamental de la biología. La manipulación farmacológica de las chaperonas, ya sea potenciando su actividad para combatir enfermedades por mal plegamiento o inhibiéndolas para atacar células cancerosas que dependen de ellas, representa una estrategia terapéutica con un enorme potencial.
A medida que la ciencia avanza, se desvela la intrincada red de interacciones entre las chaperonas y otros componentes del sistema de proteostasis, como el sistema ubiquitina-proteasoma y la autofagia. Comprender cómo estos sistemas se coordinan para mantener la salud celular es clave para desarrollar intervenciones que puedan retrasar el envejecimiento, prevenir enfermedades crónicas y mejorar la calidad de vida. Las chaperonas moleculares son, en esencia, los arquitectos invisibles que sostienen la estructura y función de la vida, un testimonio de la elegancia y eficiencia de la evolución.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.