Proteína Precursora Amiloidea (APP): Guía Definitiva Ketocis
Resumen Clínico Rápido
🔬 Clasificación
Proteína transmembrana tipo I
⚙️ Función Principal
Neuroprotección, sinaptogénesis, señalización
📋 Impacto Clínico
Precursor de péptidos beta-amiloide en Alzheimer
En el vasto y complejo universo de la neurobiología, pocas moléculas han capturado la atención científica con la intensidad de la Proteína Precursora Amiloidea (APP). Lejos de ser un mero actor secundario, APP es una proteína transmembrana omnipresente que desempeña roles fundamentales en la fisiología neuronal y que, paradójicamente, se encuentra en el epicentro de la patogénesis de la Enfermedad de Alzheimer (EA). Para el Glosario Ketocis, comprender APP no es solo un ejercicio de erudición molecular; es una inmersión en los mecanismos que rigen la salud cerebral y cómo ciertas intervenciones metabólicas pueden influir en su destino.
La APP es una molécula multifacética, cuya función normal es vital para la supervivencia y el funcionamiento óptimo de las neuronas. Sin embargo, su procesamiento aberrante es el principal factor impulsor de la acumulación de péptidos beta-amiloide (Aβ), característicos de las placas seniles en el cerebro de pacientes con EA. Esta guía enciclopédica desentrañará la doble naturaleza de APP, explorando su estructura, sus funciones fisiológicas esenciales, las vías de procesamiento que determinan su destino y su innegable relevancia en la neurodegeneración, con una perspectiva que integra la influencia de estados metabólicos como la cetosis.
Desde su papel en la sinaptogénesis y la plasticidad neuronal hasta su compleja implicación en la homeostasis del hierro y la señalización intracelular, APP es un testimonio de la intrincada maquinaria biológica. Analizaremos cómo su escisión por enzimas específicas puede generar fragmentos con funciones neuroprotectoras o, por el contrario, dar origen a los péptidos Aβ neurotóxicos. Esta comprensión es crucial para cualquier investigador, clínico o entusiasta de la salud que busque optimizar la función cerebral y mitigar el riesgo de enfermedades neurodegenerativas.
Resumen Clínico
- Punto clave 1: La Proteína Precursora Amiloidea (APP) es una proteína transmembrana esencial para la función neuronal normal, incluyendo la sinaptogénesis y la neuroprotección.
- Punto clave 2: APP se procesa a través de dos vías principales: la no amiloidogénica (beneficiosa, mediada por α-secretasas) y la amiloidogénica (precursora de Aβ, mediada por β- y γ-secretasas).
- Punto clave 3: El procesamiento anómalo de APP y la acumulación de péptidos beta-amiloide (Aβ), especialmente Aβ42, son eventos centrales en la patogénesis de la Enfermedad de Alzheimer.
El péptido beta-amiloide (Aβ) es siempre y completamente perjudicial para el cerebro.
Investigaciones recientes sugieren que los monómeros y oligómeros pequeños de Aβ pueden tener funciones fisiológicas normales, como la regulación sináptica y la defensa antimicrobiana. El peligro reside en su agregación y acumulación descontrolada, no en su existencia.
Origen y Estructura Molecular de APP
La Proteína Precursora Amiloidea es codificada por el gen APP, ubicado en el cromosoma 21 en humanos. Este hecho genético es particularmente relevante, ya que la trisomía del cromosoma 21, presente en el Síndrome de Down, se asocia con un mayor riesgo y una aparición más temprana de la Enfermedad de Alzheimer debido a la sobreexpresión de APP. La APP es una glicoproteína integral de membrana tipo I, lo que significa que posee un gran dominio extracelular (N-terminal), una única región transmembrana y un dominio intracelular (C-terminal) más corto.
La estructura de APP es fundamental para sus múltiples funciones y para su procesamiento. El dominio extracelular contiene sitios de unión para diversos ligandos y es crucial para funciones como la adhesión celular y la señalización. La región transmembrana ancla la proteína a la membrana plasmática, mientras que el dominio intracelular interactúa con proteínas adaptadoras y de señalización, participando en la regulación de la expresión génica y el transporte axonal. La conservación evolutiva de APP a lo largo de diversas especies, desde invertebrados hasta mamíferos, subraya su importancia biológica fundamental, sugiriendo roles que trascienden la mera patología.
El Rol Evolutivo de APP: Más allá de la Patología
Durante décadas, APP fue predominantemente estudiada por su asociación con la Enfermedad de Alzheimer. Sin embargo, su presencia universal en el reino animal y su expresión ubicua en el cerebro y otros tejidos sugieren un propósito evolutivo mucho más amplio que la simple generación de péptidos Aβ. APP es esencial para el desarrollo neuronal normal y el mantenimiento de la homeostasis cerebral. Se ha demostrado que los ratones con deficiencia de APP presentan defectos neurológicos significativos, incluyendo alteraciones en la morfología sináptica, déficits cognitivos y una mayor susceptibilidad a la excitotoxicidad.
El papel de APP en la neurogénesis, la migración neuronal y la diferenciación celular es bien documentado. Actúa como un factor de crecimiento y supervivencia para las neuronas, promoviendo la arborización dendrítica y la formación de nuevas sinapsis. En esencia, la función evolutiva de APP parece ser la de un regulador maestro de la estructura y función de las redes neuronales, un guardián de la integridad cerebral que, bajo ciertas condiciones de estrés o predisposición genética, puede desviarse de su camino protector.
Fisiología Molecular: Las Vías de Procesamiento de APP
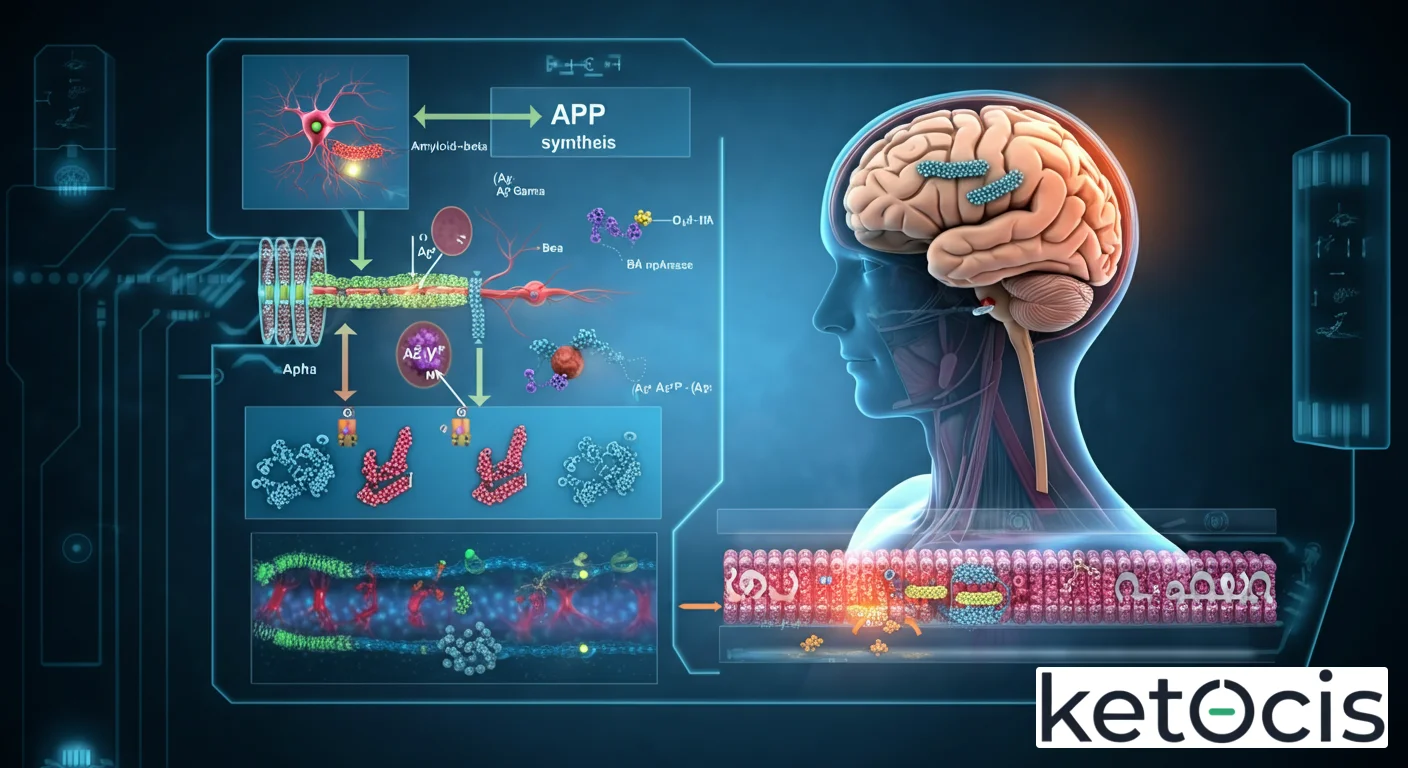
El destino de la proteína APP está determinado por una serie de eventos de escisión proteolítica llevados a cabo por enzimas conocidas como secretasas. Existen dos vías principales de procesamiento que compiten entre sí: la vía no amiloidogénica y la vía amiloidogénica. El equilibrio entre estas dos vías es crucial para la salud cerebral y la prevención de la acumulación de Aβ.
La Vía No Amiloidogénica: Neuroprotección y Plasticidad Sináptica
La vía no amiloidogénica se considera la ruta fisiológica y beneficiosa para el procesamiento de APP. En esta vía, la APP es inicialmente escindida dentro del dominio Aβ por una enzima conocida como α-secretasa. Las α-secretasas son un grupo de enzimas que incluye miembros de la familia ADAM (A Disintegrin And Metalloproteinase), como ADAM10 y ADAM17. La escisión por α-secretasa ocurre en una región crucial del péptido Aβ, impidiendo así su formación.
La escisión por α-secretasa genera dos fragmentos principales: el sAPPα (soluble APP-alpha) y el C83. El sAPPα es un gran fragmento soluble liberado al espacio extracelular que posee potentes propiedades neuroprotectoras y neurotróficas. Promueve la supervivencia neuronal, potencia la plasticidad sináptica y mejora la memoria. El fragmento C83, que permanece unido a la membrana, puede ser posteriormente escindido por la γ-secretasa para liberar un péptido más pequeño, p3, y el dominio intracelular de APP (AICD). Esta vía es vital para mantener la homeostasis neuronal y se asocia con un cerebro sano.
La Vía Amiloidogénica: El Camino hacia la Patología
En contraste con la vía no amiloidogénica, la vía amiloidogénica es la que conduce a la producción de péptidos beta-amiloide y está intrínsecamente ligada a la patogénesis de la Enfermedad de Alzheimer. Esta vía comienza con la escisión de APP por la β-secretasa (también conocida como BACE1, Beta-site APP Cleaving Enzyme 1).
La β-secretasa escinde APP en el extremo N-terminal del péptido Aβ, generando dos fragmentos: el sAPPβ (soluble APP-beta) y el C99. A diferencia del sAPPα, el sAPPβ no posee las mismas propiedades neuroprotectoras y su acumulación puede ser indicativa de una mayor actividad amiloidogénica. El fragmento C99, que permanece en la membrana, es entonces el sustrato para la segunda escisión crucial, realizada por el complejo de γ-secretasa. Este complejo proteico, compuesto por presenilina (PSEN1 o PSEN2), nicastrina, APH-1 y PEN-2, realiza una escisión intramembrana de C99.
La escisión por γ-secretasa es heterogénea y puede generar péptidos Aβ de diferentes longitudes, siendo los más comunes Aβ40 y Aβ42. De estos, Aβ42 es particularmente problemático debido a su mayor hidrofobicidad y su propensión a agregarse y formar oligómeros solubles y, eventualmente, las placas amiloides insolubles que son una característica patológica distintiva de la Enfermedad de Alzheimer. El equilibrio entre la producción de Aβ40 y Aβ42 es un factor crítico en el riesgo de desarrollar EA, con un aumento en la proporción Aβ42/Aβ40 siendo un indicador de riesgo.
Funciones Fisiológicas Clave de APP y sus Fragmentos
Además de su papel en la patología de Alzheimer, APP y sus diversos fragmentos derivados del procesamiento no amiloidogénico desempeñan una miríada de funciones biológicas esenciales:
- Sinaptogénesis y Plasticidad Neuronal: sAPPα es un potente modulador de la plasticidad sináptica, promoviendo la formación y el mantenimiento de sinapsis. Es crucial para el aprendizaje y la memoria, influyendo en la potenciación a largo plazo (LTP).
- Neuroprotección y Reparación: sAPPα actúa como un factor neuroprotector, defendiendo a las neuronas del estrés oxidativo, la excitotoxicidad y la apoptosis. También se ha implicado en la respuesta a lesiones cerebrales, promoviendo la reparación tisular.
- Regulación del Metabolismo del Hierro: APP puede unirse al hierro y participar en su transporte y almacenamiento dentro de las neuronas, un proceso vital para la función mitocondrial y la prevención del estrés oxidativo. Una disfunción en esta regulación puede contribuir a la neurodegeneración.
- Adhesión Celular y Migración: El dominio extracelular de APP contiene sitios de unión que facilitan la interacción célula-célula y célula-matriz extracelular, lo que es importante para el desarrollo neuronal y el mantenimiento de la arquitectura tisular.
- Señalización Intracelular (AICD): El dominio intracelular de APP (AICD), liberado por la γ-secretasa en ambas vías, puede translocarse al núcleo y actuar como un factor de transcripción, regulando la expresión de genes implicados en la supervivencia neuronal y la homeostasis.
APP y la Enfermedad de Alzheimer: Una Conexión Crítica
La conexión entre APP y la Enfermedad de Alzheimer es ineludible. La Hipótesis de la Cascada Amiloidea postula que la acumulación de péptidos Aβ, particularmente Aβ42, es el evento iniciador clave en la patogénesis de la EA. Esta acumulación conduce a la formación de oligómeros tóxicos y placas amiloides, que a su vez desencadenan una serie de eventos patológicos, incluyendo la formación de ovillos neurofibrilares de proteína tau, neuroinflamación, disfunción sináptica y, finalmente, la muerte neuronal.
Evidencia genética robusta apoya esta hipótesis. Mutaciones en el gen APP (así como en los genes de las presenilinas, PSEN1 y PSEN2, que codifican componentes de la γ-secretasa) están directamente asociadas con formas hereditarias y de inicio temprano de la Enfermedad de Alzheimer. Estas mutaciones alteran el procesamiento de APP, favoreciendo la producción de Aβ42 o aumentando la relación Aβ42/Aβ40, lo que acelera la agregación amiloidea. Comprender cómo estos factores genéticos interactúan con factores ambientales y de estilo de vida es fundamental para desarrollar estrategias preventivas y terapéuticas.
Biohacking APP: La Danza de las Secretasas y la Cetosis
Un fascinante dato de biohacking relacionado con APP es la observación de que la dieta cetogénica y los cuerpos cetónicos pueden modular indirectamente la actividad de las secretasas. Estudios preclínicos sugieren que el β-hidroxibutirato (BHB), el principal cuerpo cetónico, puede reducir la expresión o actividad de BACE1 (β-secretasa), la enzima clave en la vía amiloidogénica. Al desviar el metabolismo neuronal hacia la oxidación de cuerpos cetónicos, se podría no solo mejorar la bioenergética cerebral, sino también potencialmente inclinar la balanza hacia la vía no amiloidogénica de APP, favoreciendo la producción de sAPPα neuroprotector y disminuyendo la formación de Aβ. Este es un campo activo de investigación con implicaciones prometedoras para la prevención y el manejo de la neurodegeneración.
Impacto de la Dieta y el Estilo de Vida en el Procesamiento de APP
Más allá de la genética, una creciente cantidad de evidencia sugiere que factores de estilo de vida y dietéticos pueden influir significativamente en el procesamiento de APP y el riesgo de EA. La integración de estos conocimientos es clave para un enfoque holístico de la salud cerebral.
- Dieta Cetogénica: Como se mencionó, la cetosis nutricional puede tener un impacto positivo. Al proporcionar una fuente de energía alternativa y eficiente para el cerebro, los cuerpos cetónicos pueden mejorar la función mitocondrial, reducir el estrés oxidativo y la inflamación, y potencialmente modular la actividad de BACE1, favoreciendo el procesamiento no amiloidogénico de APP. La reducción de la glucotoxicidad y la resistencia a la insulina en el cerebro, a menudo observadas en dietas altas en carbohidratos, también pueden ser beneficiosas.
- Ejercicio Físico: La actividad física regular ha demostrado ser un potente neuroprotector. Promueve la neurogénesis, mejora el flujo sanguíneo cerebral y puede reducir la producción de Aβ. El ejercicio también influye en la expresión de factores neurotróficos, como el BDNF (Brain-Derived Neurotrophic Factor), que a su vez pueden impactar positivamente el procesamiento de APP.
- Sueño de Calidad: El sueño juega un papel crítico en la eliminación de metabolitos tóxicos del cerebro, incluyendo el péptido Aβ, a través del sistema glinfático. La privación crónica del sueño se asocia con un aumento en la producción de Aβ y una reducción en su eliminación, lo que puede acelerar la acumulación de placas.
- Manejo del Estrés: El estrés crónico y los altos niveles de glucocorticoides pueden aumentar la expresión y actividad de BACE1, promoviendo la vía amiloidogénica. La implementación de estrategias de reducción del estrés, como la meditación o el yoga, puede ser beneficiosa para la salud cerebral.
- Dieta Antiinflamatoria y Antioxidante: Una dieta rica en antioxidantes (vitaminas C y E, polifenoles) y ácidos grasos omega-3 puede reducir la inflamación y el estrés oxidativo, factores que exacerban la patología amiloide. Estos componentes pueden influir indirectamente en la función de las secretasas o en la eliminación de Aβ.
Alerta Metabólica: No todo el Aβ es Malo
Es crucial desmitificar la idea de que todo el péptido beta-amiloide (Aβ) es inherentemente perjudicial. Aunque las formas agregadas de Aβ, especialmente Aβ42, son neurotóxicas, estudios recientes sugieren que los monómeros de Aβ y los oligómeros pequeños pueden tener funciones fisiológicas normales. Se ha propuesto que Aβ actúa como un péptido antimicrobiano endógeno, participando en la respuesta inmune innata del cerebro. También se ha sugerido su papel en la regulación sináptica. El peligro no reside en la producción de Aβ per se, sino en su desequilibrio de producción y eliminación, lo que lleva a su agregación y a la patología. Intentar eliminar completamente Aβ podría tener consecuencias inesperadas y perjudiciales para la fisiología cerebral.
Desafíos y Futuras Direcciones en la Investigación de APP
La complejidad de APP y su procesamiento presenta tanto desafíos como oportunidades para la investigación y el desarrollo de terapias. Los enfoques actuales incluyen:
- Inhibidores de Secretasas: El desarrollo de fármacos que modulen la actividad de β- o γ-secretasas ha sido un área intensa de investigación. Sin embargo, la inhibición indiscriminada de estas enzimas ha enfrentado dificultades debido a sus múltiples sustratos y a los efectos secundarios asociados. La modulación selectiva, en lugar de la inhibición total, es una dirección prometedora.
- Inmunoterapia: Las vacunas y los anticuerpos monoclonales dirigidos a Aβ han mostrado cierto éxito en la eliminación de placas amiloides, aunque su impacto en la reversión del declive cognitivo ha sido variable y complejo.
- Enfoques Multifactoriales: Dada la naturaleza multifactorial de la Enfermedad de Alzheimer, las futuras estrategias probablemente implicarán una combinación de terapias dirigidas a APP/Aβ junto con intervenciones que aborden la inflamación, el estrés oxidativo, la disfunción metabólica y otros factores de riesgo.
- Biomarcadores Tempranos: La identificación de biomarcadores que permitan detectar cambios en el procesamiento de APP y la acumulación de Aβ en etapas preclínicas es fundamental para la intervención temprana.
Conclusión: La Complejidad de APP, una Proteína Central para la Salud Cerebral
La Proteína Precursora Amiloidea es mucho más que el precursor de las placas de Alzheimer. Es una molécula fundamental con funciones vitales en la salud y el desarrollo del sistema nervioso. Su procesamiento dual, mediado por diversas secretasas, determina si APP contribuye a la neuroprotección y la plasticidad sináptica o si, por el contrario, inicia la cascada patológica de la Enfermedad de Alzheimer.
Para los interesados en la optimización metabólica y la salud cerebral, comprender la APP subraya la importancia de mantener un equilibrio fisiológico. La dieta cetogénica, el ejercicio regular, un sueño reparador y la gestión del estrés no son solo estrategias de bienestar general; son intervenciones que pueden influir directamente en el delicado equilibrio del procesamiento de APP, inclinando la balanza hacia la vía no amiloidogénica y promoviendo la resiliencia cerebral. La investigación continua sobre APP no solo ilumina los misterios de la neurodegeneración, sino que también nos empodera con el conocimiento para tomar decisiones informadas sobre nuestro estilo de vida y nutrir la salud de nuestro cerebro.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.