Proteína FAS (CD95): Guía Definitiva de Apoptosis Celular
Resumen Clínico Rápido
🔬 Clasificación
Receptor de Muerte (Superfamilia TNFR)
⚙️ Función Principal
Inducción de Apoptosis Extrínseca
📋 Impacto
Homeostasis, Inmunidad, Cáncer
La Proteína FAS (CD95): Guardián Molecular de la Muerte Celular Programada
En el intrincado universo de la biología celular, donde la vida y la muerte coexisten en un equilibrio dinámico, la proteína FAS, también conocida como CD95 o TNFRSF6, emerge como un actor central. No es una simple molécula, sino un receptor de superficie celular que orquesta uno de los procesos más fundamentales para la salud de un organismo: la apoptosis o muerte celular programada. En este glosario de Ketocis, nos sumergiremos en la fascinante fisiología de FAS, explorando su propósito evolutivo, su mecanismo molecular y su impacto ineludible en la salud, la enfermedad y, potencialmente, en la optimización metabólica.
La apoptosis es un suicidio celular altruista, un mecanismo finamente regulado que elimina células no deseadas, dañadas o potencialmente peligrosas, sin causar inflamación en los tejidos circundantes. A diferencia de la necrosis, que es una muerte celular descontrolada y a menudo traumática, la apoptosis es un proceso ordenado y energéticamente dependiente, esencial para el desarrollo embrionario, la homeostasis tisular y la erradicación de células infectadas o cancerosas. Y en el corazón de una de las principales vías de apoptosis, la extrínseca, se encuentra la proteína FAS.
Propósito Evolutivo: La Necesidad de un Final Ordenado
La capacidad de las células para autodestruirse de manera controlada no es un capricho biológico, sino una característica profundamente arraigada y conservada a lo largo de la evolución. Desde organismos multicelulares primitivos hasta los mamíferos más complejos, la apoptosis garantiza la integridad y funcionalidad del organismo. El sistema FAS/FASL es un testimonio de esta necesidad evolutiva.
Desde el punto de vista evolutivo, la proteína FAS y su ligando, FASL, se desarrollaron como un mecanismo de defensa y control de calidad celular. Su propósito es múltiple:
- Eliminación de Células Dañadas: Las células que han sufrido daño irreparable en su ADN o que funcionan de manera defectuosa pueden ser un riesgo para el organismo. FAS actúa como un sensor, marcándolas para su eliminación.
- Modelado Tisular y Desarrollo Embrionario: Durante el desarrollo, la apoptosis esculpe órganos y tejidos, eliminando estructuras transitorias (como la cola de los renacuajos o el tejido interdigital para formar los dedos). FAS contribuye a este proceso de remodelado.
- Homeostasis Inmunológica: El sistema inmunitario genera millones de linfocitos, pero algunos son autorreactivos (atacan los propios tejidos) o ya no son necesarios tras una infección. FAS es fundamental para eliminar estos linfocitos, previniendo enfermedades autoinmunes y regulando la respuesta inmunitaria. Es clave en la «contracción» de la respuesta inmune, donde los linfocitos T activados mueren por apoptosis una vez que la amenaza ha sido neutralizada.
- Supresión Tumoral: Las células cancerosas a menudo desarrollan mecanismos para evadir la apoptosis. Sin embargo, la activación de FAS en células tumorales es una de las estrategias naturales del cuerpo para combatirlas. Comprender y potenciar esta vía es un objetivo clave en la investigación oncológica.
En esencia, FAS es un componente de un sistema de control de calidad celular que asegura que solo las células aptas y funcionales persistan, manteniendo la homeostasis y la salud del organismo.
La muerte celular es siempre perjudicial y debe evitarse a toda costa.
La apoptosis, o muerte celular programada, es un proceso vital y controlado, esencial para el desarrollo, la eliminación de células dañadas/peligrosas y la homeostasis de los tejidos. La proteína FAS es clave en esta limpieza celular.
Fisiología Molecular: El Baile de la Muerte Celular
La proteína FAS es un receptor transmembrana de tipo I, miembro de la superfamilia de receptores del factor de necrosis tumoral (TNFR). Posee un dominio extracelular rico en cisteínas, un dominio transmembrana y un dominio intracelular conocido como «dominio de muerte» (DD, por death domain).
Mecanismo de Acción: La Cascada de las Caspasas
La activación de FAS es un proceso elegante y preciso:
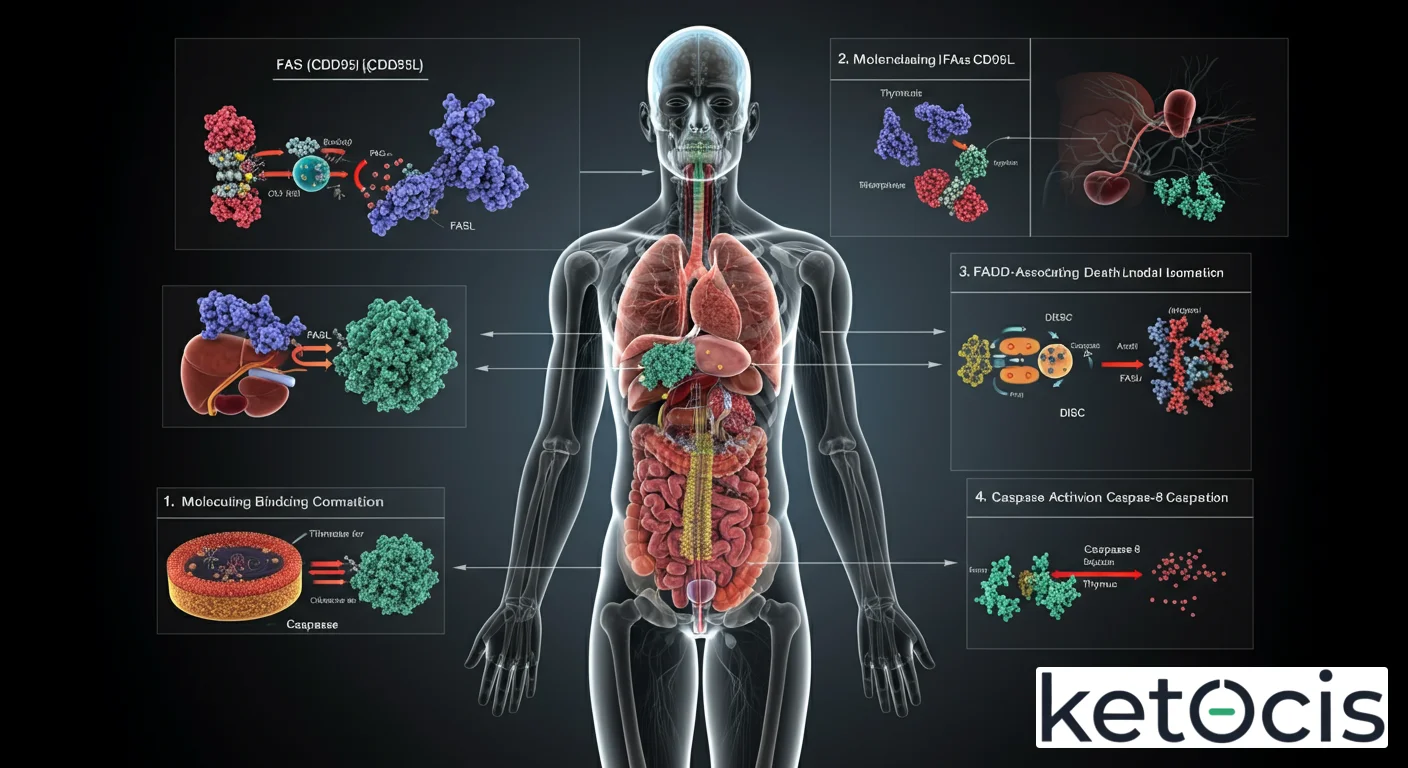
- Unión Ligando-Receptor: El proceso comienza cuando el ligando FASL (FAS Ligand o CD95L), una proteína de membrana expresada en células efectoras (como linfocitos T citotóxicos), se une a la proteína FAS en la superficie de la célula diana. FASL es un trímero, y su unión induce la trimerización de los receptores FAS.
- Formación del DISC: La trimerización de FAS permite que su dominio de muerte intracelular reclute proteínas adaptadoras, como FADD (FAS-Associated Death Domain). FADD, a su vez, recluta pro-caspasa-8 (y/o pro-caspasa-10), una enzima inactiva. Este complejo multiproteico se conoce como DISC (Death-Inducing Signaling Complex).
- Activación de Caspasas Iniciadoras: Dentro del DISC, las moléculas de pro-caspasa-8 se auto-clivan y se activan, formando caspasa-8 activa. La caspasa-8 es una «caspasa iniciadora» crucial.
- Cascada de Caspasas Efectoras: La caspasa-8 activa, a su vez, cliva y activa a las «caspasas efectoras» o ejecutoras, como la caspasa-3, caspasa-6 y caspasa-7. Estas caspasas efectoras son las que llevan a cabo la demolición celular, clivando cientos de proteínas estructurales y funcionales dentro de la célula.
- Muerte Celular: Las caspasas efectoras desmantelan el citoesqueleto, fragmentan el ADN (activando endonucleasas), y alteran la membrana celular, llevando a la formación de cuerpos apoptóticos que son fagocitados por macrófagos, evitando así la liberación de contenido intracelular y la inflamación.
Regulación y Complejidad
La vía de FAS no es un interruptor simple de encendido/apagado; está finamente regulada por diversas proteínas. Por ejemplo, FLIP (FLICE-like inhibitory protein) puede competir con pro-caspasa-8 por la unión a FADD dentro del DISC, inhibiendo la apoptosis. Otras proteínas anti-apoptóticas, como las de la familia Bcl-2, también pueden modular la sensibilidad celular a la muerte inducida por FAS, aunque su papel es más prominente en la vía intrínseca.
Rol en la Salud y la Enfermedad: Un Doble Filo
Dada su función central en la apoptosis, no sorprende que la disfunción de la vía FAS/FASL esté implicada en una amplia gama de patologías.
- Enfermedades Autoinmunes: Mutaciones en los genes FAS o FASL pueden resultar en una incapacidad de eliminar linfocitos T autorreactivos o un exceso de linfocitos T activados, llevando a síndromes linfoproliferativos autoinmunes (ALPS), caracterizados por linfadenopatía, esplenomegalia y autoinmunidad.
- Cáncer: Las células cancerosas a menudo desarrollan resistencia a la apoptosis inducida por FAS como una estrategia de supervivencia. Esto puede ocurrir por la disminución de la expresión de FAS, la sobreexpresión de inhibidores de caspasas como FLIP, o mutaciones en los componentes de la vía. Comprender esta resistencia es clave para desarrollar nuevas terapias oncológicas que reactiven la apoptosis.
- Infecciones Virales: Muchos virus han evolucionado mecanismos para interferir con la vía FAS, ya sea inhibiendo la expresión de FAS en la célula infectada o produciendo análogos de FLIP para bloquear la activación de caspasas, permitiéndoles así persistir y replicarse.
- Enfermedades Neurodegenerativas: Existe evidencia creciente de que la apoptosis mediada por FAS puede contribuir a la pérdida neuronal en enfermedades como el Alzheimer, el Parkinson y la esclerosis lateral amiotrófica. La modulación de esta vía podría ser una estrategia terapéutica futura.
FAS y el Contexto Ketocis: Muerte Celular en el Equilibrio Metabólico
El glosario Ketocis se centra en la intersección de la ciencia médica y la optimización metabólica. ¿Cómo encaja la proteína FAS en este panorama?
La cetosis nutricional y el ayuno intermitente son estados metabólicos que ejercen profundos efectos en la salud celular. Si bien la autofagia (reciclaje celular) es el proceso más comúnmente asociado con el ayuno, la apoptosis también juega un papel crucial en la homeostasis y la eliminación de células senescentes o dañadas.
- Eliminación de Células Senescentes: Las células senescentes son células envejecidas que han dejado de dividirse pero persisten en los tejidos, secretando factores proinflamatorios que contribuyen al envejecimiento y a enfermedades crónicas. Se ha postulado que el ayuno y la cetosis pueden promover la eliminación de estas células. Aunque la autofagia es central, la apoptosis mediada por vías como FAS podría ser un mecanismo complementario para la limpieza celular.
- Impacto en Células Cancerosas: La investigación sugiere que la cetosis puede hacer que las células cancerosas sean más vulnerables a la apoptosis, mientras que protege a las células sanas. Algunos estudios indican que la restricción calórica o la cetosis pueden modular la expresión de proteínas pro-apoptóticas o anti-apoptóticas, afectando la sensibilidad de las células tumorales a vías de muerte como la de FAS. Potenciar la vía FAS en células tumorales, mientras se protege a las sanas, es un área activa de investigación.
- Regulación Inmunológica: Dado el papel de FAS en la homeostasis inmunológica, es plausible que los estados metabólicos como la cetosis, que modulan la función inmunitaria, puedan influir en la actividad de FASL en las células inmunes, afectando la eliminación de linfocitos y la resolución de la inflamación.
Es importante destacar que la relación directa entre la cetosis y la regulación específica de la proteína FAS es un campo de investigación emergente. Sin embargo, la interconexión entre el estado metabólico, la salud celular y los mecanismos de control de calidad como la apoptosis es innegable.
Conclusión: La Elegancia de la Muerte Programada
La proteína FAS (CD95) es mucho más que un simple receptor; es un guardián molecular que asegura la salud y la integridad del organismo a través de la orquestación precisa de la muerte celular programada. Su papel en el desarrollo embrionario, la homeostasis inmunológica y la supresión tumoral subraya su importancia insustituible. Comprender la fisiología de FAS nos ofrece una ventana a la sofisticación de la biología celular y nos equipa con herramientas conceptuales para abordar enfermedades complejas, desde el cáncer hasta las patologías autoinmunes. En el contexto de la optimización metabólica, la investigación futura desvelará cómo estrategias como la cetosis pueden interactuar con esta vía fundamental, abriendo nuevas avenidas para potenciar la salud celular y la longevidad.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.