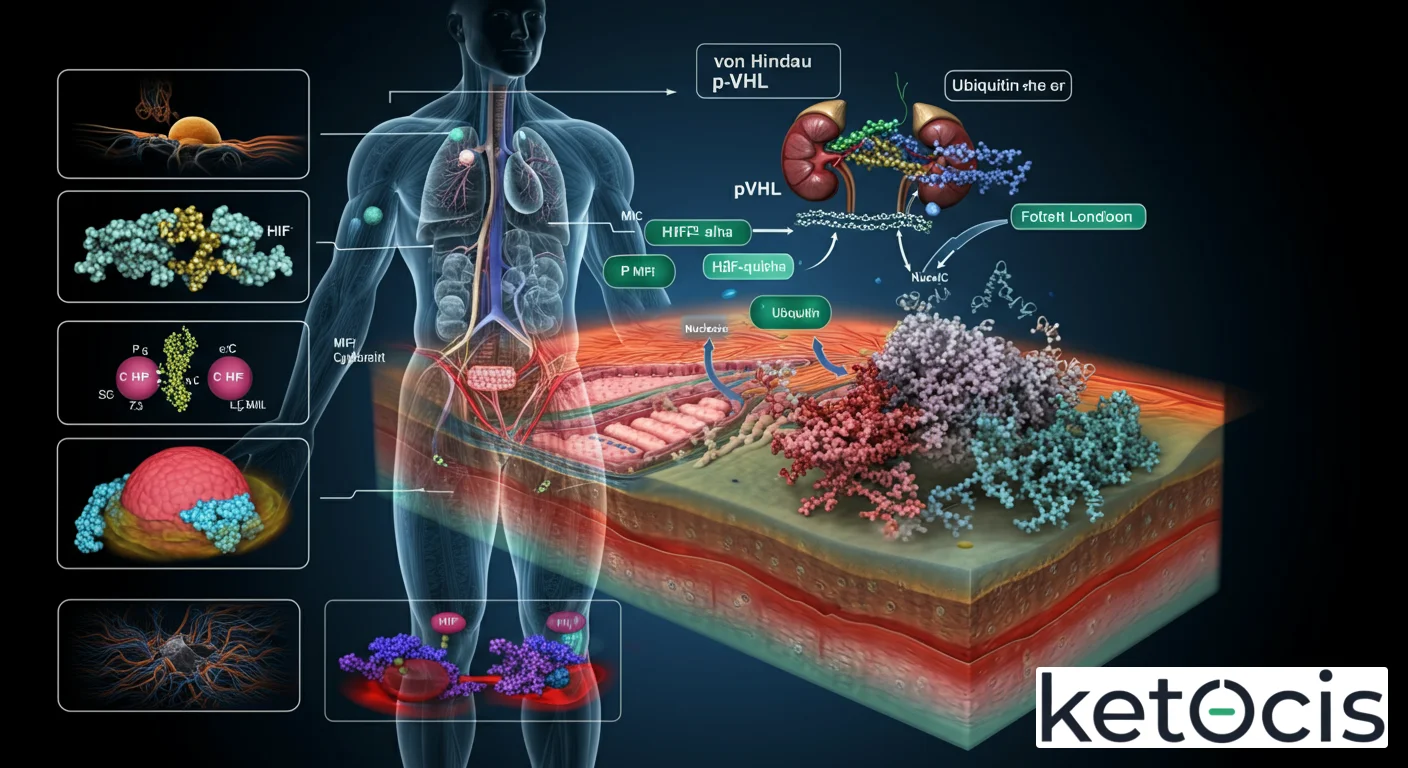
pVHL: La Proteína Supresora de Tumores y Regulador Maestro
Resumen Clínico Rápido
🔬 Clasificación
Proteína supresora de tumores, E3 ubiquitín ligasa
⚙️ Función
Regula la degradación de HIF en normoxia, esencial en la respuesta al oxígeno y la prevención tumoral.
📋 Impacto
Mutaciones causan síndrome de VHL y carcinoma de células renales; afecta angiogénesis y metabolismo.
En el intrincado universo de la biología celular, existen guardianes silenciosos que orquestan procesos vitales, determinando la salud o la enfermedad de un organismo. Entre ellos, la proteína de von Hippel-Lindau, más conocida como pVHL, emerge como una figura central. Lejos de ser una mera molécula, pVHL es un regulador maestro, una centinela molecular cuya función es indispensable para mantener la homeostasis celular y prevenir la progresión de enfermedades devastadoras, incluido el cáncer.
Descubierta inicialmente por su asociación con el síndrome genético de von Hippel-Lindau, una enfermedad hereditaria que predispone a múltiples tumores, pVHL ha revelado ser mucho más que un simple gen defectuoso. Es una proteína supresora de tumores fundamental, crucial en la respuesta celular a la disponibilidad de oxígeno y en la regulación de la expresión génica. Su correcta función es un baluarte contra la proliferación descontrolada y la formación de vasos sanguíneos anómalos, procesos que son sellos distintivos de muchas neoplasias.
Resumen Clínico
- Punto clave 1: pVHL es una proteína supresora de tumores esencial, cuya disfunción está directamente ligada al síndrome de von Hippel-Lindau y a diversas neoplasias malignas, especialmente el carcinoma de células renales.
- Punto clave 2: Actúa como el componente clave del complejo E3 ubiquitín ligasa, marcando proteínas, principalmente los Factores Inducibles por Hipoxia (HIF), para su degradación proteasomal en condiciones normales de oxígeno.
- Punto clave 3: Regula la respuesta celular a la hipoxia, controlando la expresión de genes que promueven la angiogénesis, eritropoyesis y el metabolismo glucolítico, asegurando una adaptación fisiológica adecuada.
Origen y Descubrimiento de pVHL
La historia de pVHL comienza con una enfermedad rara pero devastadora: el síndrome de von Hippel-Lindau (VHL). Descrito por primera vez a finales del siglo XIX y principios del XX por los oftalmólogos Eugen von Hippel y Arvid Lindau, este síndrome se caracteriza por el desarrollo de tumores benignos y malignos en múltiples órganos, como el cerebro, la médula espinal, la retina, los riñones, las glándulas suprarrenales y el páncreas. La naturaleza hereditaria de la enfermedad sugería la existencia de un gen subyacente responsable.
Fue en la década de 1990 cuando se logró identificar y clonar el gen VHL humano, localizado en el cromosoma 3p25-26. Este descubrimiento monumental reveló que las mutaciones germinales en este gen eran la causa principal del síndrome de VHL. El producto de este gen es la proteína pVHL, una proteína de 213 aminoácidos que rápidamente fue clasificada como una proteína supresora de tumores. Su papel inicial se entendió en el contexto de la prevención del cáncer, dado que su inactivación o deleción se observaba comúnmente en los tumores asociados al síndrome, especialmente en el carcinoma de células renales de células claras (ccRCC), la forma más frecuente de cáncer renal.
La comprensión de pVHL como supresor tumoral revolucionó el campo de la oncología, al proporcionar una pieza clave en el rompecabezas de cómo las células controlan su crecimiento y diferenciación. La pérdida de función de pVHL permite que las células escapen de los mecanismos de control, llevando a un crecimiento desregulado y a la formación de tumores.
El síndrome de von Hippel-Lindau es solo una enfermedad que afecta a los riñones.
El síndrome de VHL es una enfermedad multisistémica que afecta a múltiples órganos (cerebro, médula espinal, retina, glándulas suprarrenales, páncreas) y predispone a varios tipos de tumores, no solo renales, debido a la disfunción de la proteína pVHL.
Mecanismo de Acción: El Director de la Orquesta Hipóxica
El mecanismo de acción de pVHL es una obra maestra de la regulación molecular, centrada en la respuesta celular a los niveles de oxígeno. Su función principal es actuar como el componente de reconocimiento de sustrato de un complejo E3 ubiquitín ligasa. Este complejo, conocido como VBC (pVHL-Elongina B-Elongina C), es responsable de marcar proteínas específicas con una pequeña molécula llamada ubiquitina, lo que las etiqueta para su degradación por el proteasoma celular.
Regulación de los Factores Inducibles por Hipoxia (HIF)
El sustrato más crítico y mejor estudiado de pVHL son los Factores Inducibles por Hipoxia (HIF), particularmente las subunidades HIF-1α y HIF-2α. Los HIF son factores de transcripción que desempeñan un papel central en la adaptación celular a la hipoxia (bajos niveles de oxígeno). En condiciones normales de oxígeno (normoxia), pVHL asegura que los HIF sean constantemente degradados, manteniendo sus niveles bajos y, por tanto, silenciando los genes que activan.
El proceso es el siguiente: en normoxia, unas enzimas llamadas prolil hidroxilasas (PHD) hidroxilan residuos de prolina específicos en las subunidades α de HIF. Esta hidroxilación es esencial porque crea un sitio de unión para pVHL. Una vez que pVHL se une al HIF hidroxilado, el complejo VBC lo ubiquitina, dirigiéndolo al proteasoma para su rápida degradación. Este ciclo asegura que, en presencia de oxígeno adecuado, los HIF no se acumulen y no activen la transcripción de sus genes diana.
Sin embargo, en condiciones de hipoxia, las PHD son inactivadas debido a la falta de oxígeno, que es un cofactor esencial para su actividad. Sin hidroxilación, pVHL no puede unirse a HIF, lo que permite que las subunidades α de HIF se estabilicen, se acumulen y se transloquen al núcleo. Allí, se heterodimerizan con la subunidad constitutiva HIF-1β y se unen a secuencias reguladoras de ADN llamadas elementos de respuesta a la hipoxia (HRE), activando la transcripción de cientos de genes. Estos genes promueven procesos vitales para la supervivencia celular en hipoxia, como la angiogénesis (formación de nuevos vasos sanguíneos), la eritropoyesis (producción de glóbulos rojos) y el cambio a un metabolismo más glucolítico.
Otros Sustratos y Funciones
Aunque la regulación de HIF es la función más prominente de pVHL, estudios recientes han revelado que pVHL también interactúa y regula otras proteínas. Por ejemplo, se ha demostrado que pVHL degrada la fibronectina, una proteína de la matriz extracelular, y que participa en la regulación de la polaridad celular a través de la degradación de proteínas quinasas atípicas (aPKC). Estas funciones adicionales sugieren que pVHL tiene un papel más amplio en la homeostasis celular que va más allá de la mera respuesta a la hipoxia, influyendo en la adhesión celular, la migración y la arquitectura tisular, todos ellos procesos críticos en la prevención del cáncer.
Antagonistas y Consecuencias de la Disfunción
pVHL no tiene antagonistas directos en el sentido farmacológico, pero su función puede ser “antagonizada” por mutaciones genéticas o por condiciones ambientales extremas. La principal “antagonista” de pVHL es su propia inactividad, que tiene profundas implicaciones patológicas.
Mutaciones del Gen VHL y el Síndrome VHL
La disfunción más común de pVHL se produce por mutaciones en el gen VHL. Estas mutaciones pueden ser germinales (heredadas) o somáticas (adquiridas). Las mutaciones germinales son la base del síndrome de von Hippel-Lindau, donde la pérdida de una copia funcional del gen VHL predispone a los individuos a desarrollar una serie de tumores benignos y malignos, incluyendo:
- Carcinoma de células renales de células claras (ccRCC): El tipo de cáncer de riñón más común y agresivo. La pérdida de la segunda copia funcional del gen VHL en las células renales (pérdida de heterocigosidad) es un evento clave en la patogénesis de estos tumores.
- Hemangioblastomas: Tumores vasculares benignos que se forman en el cerebro, la médula espinal y la retina.
- Feocromocitomas: Tumores de las glándulas suprarrenales que producen catecolaminas.
- Tumores de sacos endolinfáticos: Tumores del oído interno.
- Cistadenomas papilares del epidídimo y ligamento ancho: Tumores quísticos benignos.
- Tumores neuroendocrinos pancreáticos: Tumores del páncreas.
En todos estos casos, la pérdida de la función de pVHL conduce a una acumulación incontrolada de HIF, incluso en presencia de oxígeno. Esta condición se conoce como pseudo-hipoxia, ya que las células se comportan como si estuvieran en un ambiente de bajos niveles de oxígeno, activando constantemente los genes pro-angiogénicos, pro-proliferativos y pro-metabólicos que impulsan el crecimiento tumoral.
Implicaciones en el Cáncer Esporádico
Más allá del síndrome de VHL, las mutaciones somáticas o la inactivación epigenética del gen VHL se encuentran en un alto porcentaje de carcinomas de células renales esporádicos (no hereditarios), lo que subraya la importancia de pVHL como un supresor tumoral universal en este tipo de cáncer. La comprensión de esta vía ha llevado al desarrollo de terapias dirigidas que buscan inhibir la angiogénesis o directamente las proteínas HIF en pacientes con ccRCC.
Biohacking y Optimización de la Vía pVHL/HIF
Aunque no podemos ‘biohackear’ directamente la expresión de pVHL, podemos influir en el equilibrio de la vía pVHL-HIF a través de la gestión del estrés oxidativo y la función mitocondrial. Compuestos como el sulforafano (en brócoli) o el resveratrol (en uvas rojas) han mostrado modular la actividad de las prolil hidroxilasas (PHD) o influir en la estabilidad de HIF, promoviendo una respuesta adaptativa saludable. Optimizar la salud mitocondrial mediante ejercicio regular y una dieta rica en antioxidantes puede mejorar la sensibilidad al oxígeno celular, asegurando que la vía pVHL-HIF funcione eficientemente para responder a las demandas energéticas sin caer en un estado de pseudo-hipoxia.
Rol en Cetosis, Ayuno y Optimización Metabólica
La conexión entre pVHL, la vía HIF y el metabolismo es profunda y multifacética, con implicaciones significativas en estados metabólicos como la cetosis y el ayuno.
pVHL, HIF y el Metabolismo Celular
La vía HIF es un regulador clave del metabolismo celular. En condiciones de hipoxia (o pseudo-hipoxia debido a la disfunción de pVHL), la activación de HIF-1α promueve la glucólisis anaeróbica (efecto Warburg) y suprime la fosforilación oxidativa mitocondrial. Esto se logra mediante la activación de genes que codifican enzimas glucolíticas (como HK2, PFKFB3) y la piruvato deshidrogenasa quinasa 1 (PDK1), que inhibe la entrada de piruvato en el ciclo de Krebs. Este cambio metabólico es una adaptación para generar ATP rápidamente en ausencia de oxígeno, pero puede ser perjudicial a largo plazo.
En contraste, un pVHL funcional asegura la degradación de HIF en normoxia, promoviendo un metabolismo oxidativo eficiente. Este equilibrio es crucial para la salud celular y la prevención de enfermedades metabólicas.
Impacto de la Cetosis y el Ayuno Intermitente
La cetosis nutricional y el ayuno intermitente son estados metabólicos que alteran profundamente la forma en que las células generan energía. Al reducir la disponibilidad de glucosa y aumentar la oxidación de ácidos grasos y cuerpos cetónicos, estos estados pueden influir en la vía pVHL-HIF de varias maneras:
- Estrés Oxidativo y Función Mitocondrial: Aunque el ayuno y la cetosis pueden inducir un ligero estrés oxidativo inicial, a largo plazo suelen mejorar la función mitocondrial y reducir la producción de especies reactivas de oxígeno (ROS). Una reducción del ROS puede influir en la actividad de las PHD y, por ende, en la estabilidad de HIF. Algunas evidencias sugieren que la cetosis podría modular la actividad de HIF-1α, aunque la relación exacta es compleja y dependiente del contexto celular.
- Disponibilidad de Nutrientes: La actividad de las PHD, que son cruciales para la interacción pVHL-HIF, depende de cofactores como el hierro y el α-cetoglutarato. La disponibilidad de estos metabolitos puede verse alterada por el estado nutricional. El ayuno, al modificar la disponibilidad de sustratos, podría modular indirectamente la actividad de la vía.
- Autofagia: El ayuno y la cetosis son potentes inductores de la autofagia, un proceso de reciclaje celular que elimina componentes dañados. Una autofagia eficiente es vital para mantener la salud mitocondrial y reducir el estrés celular, lo que indirectamente apoya la función óptima de pVHL y previene la acumulación patológica de HIF.
Mantener una función pVHL óptima a través de un estilo de vida saludable que promueva la salud metabólica es clave. Esto incluye una dieta rica en nutrientes, ejercicio regular y evitar toxinas ambientales que puedan generar estrés oxidativo excesivo, factores que pueden comprometer la integridad de las vías de señalización celular.
Alerta Médica: El Peligro de la Pseudo-Hipoxia Crónica
La disfunción de pVHL, ya sea por mutación genética o por factores ambientales que inducen un estado de pseudo-hipoxia, conlleva un riesgo significativo. La activación crónica e incontrolada de los Factores Inducibles por Hipoxia (HIF) no solo impulsa el crecimiento tumoral al promover la angiogénesis y la proliferación, sino que también reprograma el metabolismo celular hacia la glucólisis, incluso en presencia de oxígeno. Esta dependencia glucolítica puede hacer a las células más vulnerables a las fluctuaciones de glucosa y más resistentes a las terapias. Es crucial reconocer que la pseudo-hipoxia no es un estado benigno; es un motor de patología que demanda atención médica y estrategias de intervención para mitigar sus efectos.
Conclusión: pVHL, un Centinela de la Vida Celular
La proteína de von Hippel-Lindau (pVHL) es mucho más que un supresor de tumores; es un centinela molecular, un director de orquesta que afina la respuesta celular a uno de los parámetros más fundamentales para la vida: la disponibilidad de oxígeno. Su descubrimiento no solo desentrañó el misterio de una rara enfermedad genética, sino que también abrió nuevas avenidas en la comprensión del cáncer y la fisiología metabólica.
Desde su papel central en la degradación de los Factores Inducibles por Hipoxia (HIF) en normoxia, hasta su implicación en la polaridad celular y la matriz extracelular, pVHL ejerce una influencia profunda en la homeostasis. Su disfunción, ya sea por mutaciones genéticas o por factores ambientales, desencadena una cascada de eventos que pueden conducir a la pseudo-hipoxia, la proliferación celular descontrolada y la formación de tumores con características metabólicas adaptadas a la supervivencia en condiciones adversas.
La investigación continua sobre pVHL y sus vías asociadas promete nuevas estrategias terapéuticas, no solo para el cáncer renal y el síndrome de VHL, sino también para una gama más amplia de enfermedades donde la desregulación de la respuesta a la hipoxia juega un papel. Comprender y optimizar la función de pVHL es, en esencia, comprender y optimizar una de las bases de la salud celular, abriendo caminos hacia una medicina más precisa y preventiva.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.