Fosfolipasa C Épsilon: Enzima Clave en Señalización Celular
Resumen Clínico Rápido
🔬 Clasificación
Fosfolipasa C, isoforma épsilon
⚙️ Función
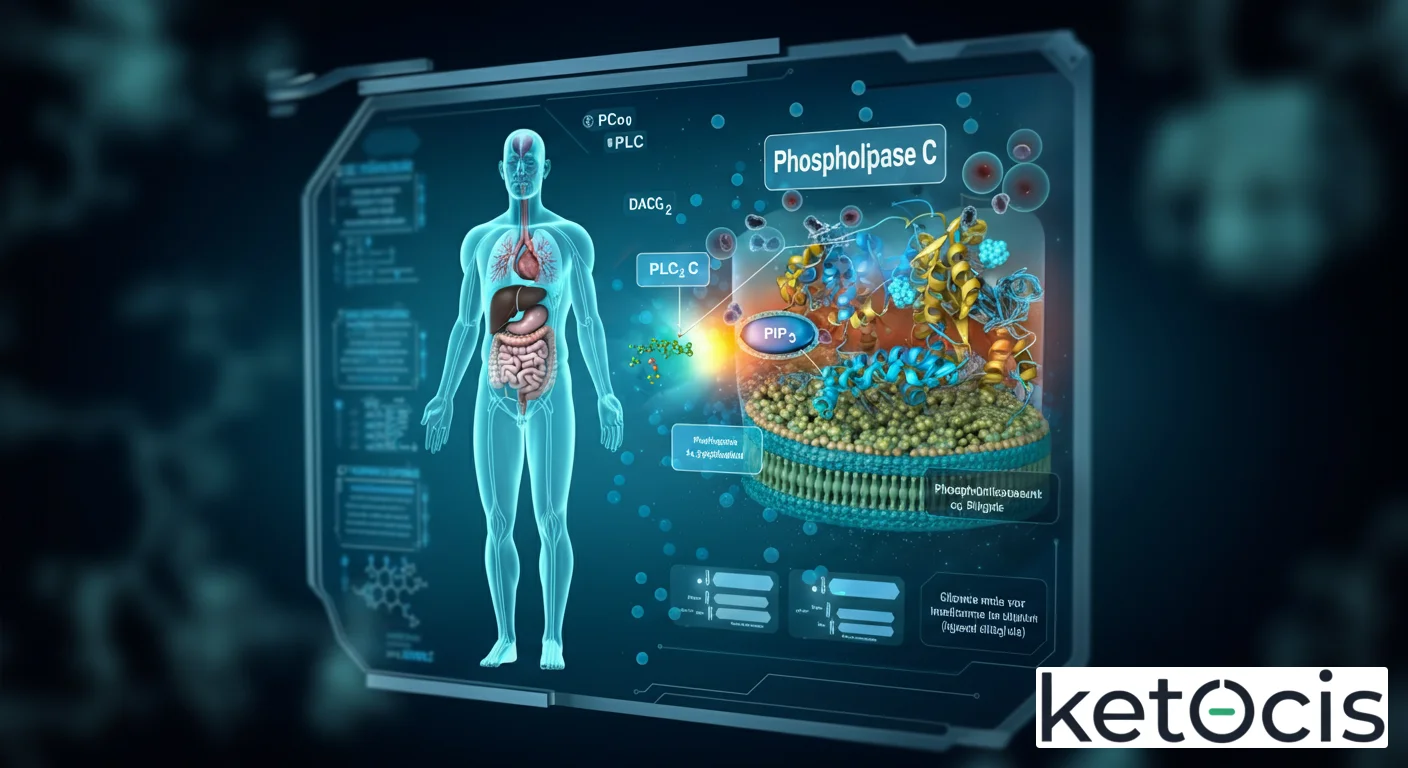
Hidrólisis de PIP2 a DAG e IP3; mediador de calcio y PKC
📋 Impacto
Regula crecimiento, diferenciación, contractilidad; implicada en cáncer, enfermedad cardíaca y renal
¿Qué es la Fosfolipasa C Épsilon? Una Guía Definitiva para el Glosario Ketocis
En el vasto y complejo universo de la biología celular, donde miles de proteínas orquestan una sinfonía de señales para mantener la vida, la fosfolipasa C épsilon (PLC-ε) emerge como una protagonista de particular interés. Esta enzima, miembro de la extensa familia de las fosfolipasas C, se distingue por su arquitectura molecular única y sus roles multifacéticos en la transducción de señales. Comprender su función no solo desentraña misterios fundamentales de la fisiología celular, sino que también abre puertas a nuevas estrategias terapéuticas para diversas patologías, desde enfermedades cardiovasculares hasta el cáncer.
La fosfolipasa C épsilon es mucho más que una simple enzima; es un nodo de integración crucial que conecta diversas vías de señalización, incluyendo aquellas activadas por pequeños GTPasas de la familia Ras y los receptores acoplados a proteínas G (GPCRs). Su capacidad para hidrolizar fosfatidilinositol 4,5-bisfosfato (PIP2) en diacilglicerol (DAG) e inositol 1,4,5-trifosfato (IP3) la posiciona en el epicentro de la generación de segundos mensajeros que regulan procesos tan vitales como la proliferación celular, la diferenciación, la migración y la contracción muscular. En el contexto de la salud metabólica y las intervenciones como la cetosis, comprender cómo enzimas como PLC-ε responden y modulan las señales intracelulares es fundamental para apreciar la adaptabilidad y resiliencia del organismo.
El mito popular es que todas las fosfolipasas C son intercambiables y responden a los mismos estímulos, lo que simplifica excesivamente su función.
La ciencia demuestra que, aunque comparten la hidrólisis de PIP2, las isoformas de PLC (como PLC-ε) tienen estructuras únicas, mecanismos de activación específicos (Ras/Rap, cAMP para PLC-ε) y roles fisiológicos distintos, haciendo que no sean intercambiables y requieran una comprensión detallada para terapias.
Origen y Descubrimiento de una Enzima Multifacética
La historia de las fosfolipasas C se remonta a varias décadas, con la identificación de diversas isoformas que compartían la capacidad de hidrolizar fosfolípidos. Sin embargo, la fosfolipasa C épsilon (PLC-ε) fue una de las últimas adiciones a esta familia, descubierta a finales de los años 90. Su identificación fue un hito debido a su estructura única, que la distingue de otras fosfolipasas C. A diferencia de las isoformas beta (β), gamma (γ) y delta (δ), PLC-ε posee dominios adicionales que le confieren una capacidad de integración de señales sin precedentes.
Estos dominios incluyen un dominio de homología a Ras/Rap-GEF (GEF-like), un dominio de homología a Ras (RA) y un dominio C2 en su región N-terminal, además de los dominios catalíticos X e Y característicos de todas las PLCs. La presencia de estos dominios vincula directamente a PLC-ε con la señalización de pequeñas GTPasas, como Ras y Rap, lo que la convierte en un puente molecular entre estas vías y la cascada de los segundos mensajeros de fosfoinosítidos. Este descubrimiento no solo amplió nuestra comprensión de la diversidad de las PLCs, sino que también reveló una nueva capa de complejidad en la transducción de señales intracelulares.
Mecanismo de Acción: La Orquestación de Segundos Mensajeros
El núcleo de la función de PLC-ε reside en su capacidad enzimática para hidrolizar el fosfatidilinositol 4,5-bisfosfato (PIP2), un fosfolípido de membrana fundamental. Esta hidrólisis genera dos segundos mensajeros vitales: el diacilglicerol (DAG) y el inositol 1,4,5-trifosfato (IP3). Cada uno de estos mensajeros desencadena una serie de eventos intracelulares que modulan la actividad celular de manera profunda y específica.
El IP3, una vez liberado en el citoplasma, se une a receptores específicos en la membrana del retículo endoplasmático, provocando la liberación de iones calcio (Ca2+) almacenados. Este aumento transitorio del calcio intracelular es un evento crucial que regula una miríada de procesos, desde la contracción muscular y la secreción hormonal hasta la expresión génica y la plasticidad sináptica. Por otro lado, el DAG permanece anclado a la membrana plasmática, donde ejerce su función principal como activador de las proteínas quinasas C (PKC). Las PKC son una familia de enzimas que fosforilan diversas proteínas diana, modulando así su actividad y participando en la regulación de la proliferación celular, la diferenciación y la respuesta inflamatoria.
Lo que distingue a PLC-ε de otras isoformas es su modo de activación. A diferencia de las PLCs-β, que son activadas principalmente por proteínas G heterotriméricas, o las PLCs-γ, que responden a tirosina quinasas, PLC-ε es activada de manera robusta por pequeñas GTPasas de la familia Ras, como Ras y Rap. Estas GTPasas, conocidas como interruptores moleculares, se activan en respuesta a factores de crecimiento, hormonas y otros estímulos externos. La interacción directa de los dominios RA y GEF-like de PLC-ε con Ras o Rap en su estado activo (unido a GTP) recluta la enzima a la membrana plasmática y estimula su actividad catalítica. Además, PLC-ε también puede ser activada por GPCRs, lo que subraya su papel como punto de convergencia para múltiples vías de señalización.
Un aspecto fascinante y aún en investigación es la interacción de PLC-ε con la vía del cAMP (adenosín monofosfato cíclico), otro segundo mensajero crucial. A diferencia de otras PLCs, PLC-ε contiene un dominio de unión a cAMP, lo que sugiere una modulación directa por esta vía. Esta característica posiciona a PLC-ε como un integrador clave entre las vías de Ras/Rap, GPCRs y cAMP, permitiendo una señalización intracelular altamente coordinada y contextualmente dependiente. Esta complejidad en su mecanismo de acción le confiere una versatilidad funcional que es explotada en una amplia gama de procesos fisiológicos.
Antagonistas y Regulación: El Control Fino de la Actividad Enzimática
La actividad de PLC-ε no es un proceso descontrolado; está sujeta a una regulación estricta para asegurar una respuesta celular apropiada y evitar la señalización aberrante. Esta regulación se produce a múltiples niveles, desde la modulación de su expresión génica hasta la fosforilación post-traduccional y la interacción con proteínas inhibidoras o coactivadoras.
Los principales ‘antagonistas’ o, más precisamente, reguladores negativos de PLC-ε incluyen proteínas que inactivan sus activadores aguas arriba. Por ejemplo, las proteínas activadoras de GTPasa (GAPs) para Ras y Rap promueven la hidrólisis de GTP a GDP, inactivando estas pequeñas GTPasas y, por ende, reduciendo la activación de PLC-ε. De manera similar, fosfatasas específicas pueden desfosforilar sitios clave en PLC-ε, alterando su conformación y actividad.
Además, la propia maquinaria de señalización de fosfoinosítidos tiene mecanismos de retroalimentación. Las quinasas de lípidos, como la fosfatidilinositol 3-quinasa (PI3K), y las fosfatasas de lípidos, como PTEN, regulan los niveles de PIP2 en la membrana. Una disminución en la disponibilidad de PIP2, el sustrato de PLC-ε, limitará su actividad. La compartimentalización celular también juega un papel crucial; la localización de PLC-ε en microdominios específicos de la membrana puede influir en su acceso a sustratos y activadores.
La modulación por la vía del cAMP es particularmente interesante. Aunque el cAMP generalmente se asocia con la activación de la proteína quinasa A (PKA), su interacción con PLC-ε sugiere una posible modulación cruzada. En algunos contextos, un aumento en cAMP podría potenciar la actividad de PLC-ε, mientras que en otros podría tener un efecto inhibitorio, dependiendo de la célula y el estímulo. Esta complejidad subraya la sofisticación de las redes de señalización intracelular, donde los ‘antagonistas’ no son meros inhibidores, sino parte de un sistema de equilibrio dinámico.
Roles Fisiológicos y Patológicos: Impacto en la Salud y la Enfermedad
La amplia distribución de PLC-ε en diversos tejidos y su capacidad para integrar múltiples señales la convierten en un actor clave en una variedad de procesos fisiológicos. Sin embargo, su desregulación también está implicada en la patogénesis de numerosas enfermedades.
Sistema Cardiovascular
En el corazón, PLC-ε desempeña un papel crítico en la regulación de la contractilidad y en la respuesta al estrés. Se ha demostrado que su activación contribuye a la hipertrofia cardíaca patológica, una condición en la que el músculo cardíaco se agranda en respuesta a una sobrecarga de trabajo. La señalización a través de PLC-ε y sus segundos mensajeros, DAG y IP3, puede activar vías pro-hipertróficas, lo que la convierte en un objetivo potencial para el tratamiento de enfermedades cardíacas.
Sistema Nervioso
En el cerebro, PLC-ε participa en el desarrollo neuronal, la plasticidad sináptica y la memoria. Su activación es importante para la consolidación de la memoria a largo plazo y la formación de nuevas conexiones neuronales. La disfunción de PLC-ε podría contribuir a trastornos neurológicos, aunque la investigación en esta área aún está en sus primeras etapas.
Sistema Inmune
PLC-ε también influye en la función de las células inmunitarias. Se ha implicado en la activación de células T y la degranulación de mastocitos, procesos cruciales para la respuesta inmune y las reacciones alérgicas. La modulación de PLC-ε podría ofrecer nuevas vías para el tratamiento de enfermedades autoinmunes o alérgicas.
Función Renal
En los riñones, PLC-ε es esencial para el mantenimiento de la barrera de filtración glomerular, particularmente en los podocitos. Mutaciones en genes que regulan la vía de PLC-ε o su propia expresión pueden llevar a enfermedades renales, como la glomeruloesclerosis focal y segmentaria, lo que subraya su importancia en la homeostasis renal.
Cáncer
Quizás uno de los roles patológicos más estudiados de PLC-ε es su contribución a la progresión del cáncer. Dada su activación por las vías de Ras, que son frecuentemente mutadas y activas en muchos tipos de cáncer, PLC-ε puede actuar como un oncogén. Se ha encontrado su sobreexpresión o activación aberrante en diversos tumores, incluyendo cáncer de colon, pulmón, mama y vejiga, donde promueve la proliferación, supervivencia y migración de células cancerosas. Su inhibición selectiva podría representar una estrategia terapéutica prometedora en la oncología.
PLC-ε y el Contexto Metabólico: ¿Relevancia para la Cetosis?
La relación directa entre PLC-ε y estados metabólicos específicos como la cetosis no ha sido extensamente dilucidada. Sin embargo, su papel central en la transducción de señales que regulan el crecimiento, la supervivencia y la respuesta celular al estrés sugiere una relevancia indirecta y fundamental.
La cetosis, un estado metabólico inducido por dietas bajas en carbohidratos o el ayuno, implica profundos cambios en el metabolismo energético, la inflamación y la señalización celular. Las vías activadas por Ras y Rap, que son potentes activadores de PLC-ε, están intrínsecamente ligadas a la detección de nutrientes, el crecimiento celular y la respuesta al estrés oxidativo. Por ejemplo, en un estado de cetosis, donde hay una reducción en la señalización de insulina y una mayor dependencia de las grasas como fuente de energía, las vías de crecimiento y proliferación celular pueden ser moduladas a la baja. Dado que PLC-ε es un mediador clave de estas vías, es plausible que su actividad sea indirectamente influenciada por los cambios metabólicos asociados con la cetosis.
Además, la cetosis se asocia con una reducción de la inflamación y un aumento de la resiliencia celular. PLC-ε, al participar en la señalización de células inmunes y en la respuesta al estrés oxidativo a través de la activación de PKC, podría ser un modulador de estos efectos. Por ejemplo, la modulación de los niveles de DAG y IP3 por PLC-ε puede influir en la activación de vías pro-inflamatorias o anti-inflamatorias, dependiendo del contexto celular.
Aunque no existe un ‘biohacking’ directo para PLC-ε en el contexto de la cetosis, el mantenimiento de un ambiente metabólico saludable a través de la dieta y el estilo de vida puede optimizar la función de las vías de señalización en las que PLC-ε participa. La reducción del estrés oxidativo, la mejora de la sensibilidad a la insulina y la modulación de la inflamación, todos ellos beneficios asociados con la cetosis, pueden crear un entorno celular más propicio para una señalización equilibrada y funcional de enzimas como PLC-ε.
Perspectivas Futuras y Conclusión
La fosfolipasa C épsilon es una enzima de señalización fascinante, cuya complejidad estructural y funcional la posiciona como un integrador crucial de múltiples vías de señalización intracelular. Desde su descubrimiento, la investigación ha revelado sus roles esenciales en la fisiología de sistemas tan diversos como el cardiovascular, renal, nervioso e inmune, así como su implicación en la patogénesis de enfermedades graves como el cáncer y la hipertrofia cardíaca.
El continuo estudio de PLC-ε no solo profundiza nuestra comprensión de la biología celular fundamental, sino que también abre nuevas avenidas para el desarrollo de terapias dirigidas. La capacidad de modular selectivamente la actividad de PLC-ε, sin afectar a otras isoformas de PLC, representa un desafío farmacológico significativo pero prometedor. Dada su intrincada conexión con la señalización de Ras/Rap y su potencial interacción con la vía del cAMP, PLC-ε sigue siendo un área activa de investigación con el potencial de desvelar nuevos mecanismos de regulación celular y de ofrecer soluciones innovadoras a problemas de salud complejos.
Para aquellos interesados en la optimización de la salud y el rendimiento a través de enfoques como la cetosis, comprender la maquinaria molecular subyacente, como PLC-ε, es esencial. Aunque la conexión directa pueda ser sutil, la salud de estas vías de señalización fundamentales es la base de la resiliencia y la adaptabilidad celular, elementos clave para maximizar los beneficios de cualquier intervención metabólica. La fosfolipasa C épsilon, por lo tanto, no es solo una enzima; es un testimonio de la intrincada belleza y precisión de la vida a nivel molecular.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.