¿Qué es el transportador de metales divalentes 1 (DMT1)? – Análisis Completo y Beneficios
Resumen Clínico Rápido
🔬 Clasificación
Proteína transmembrana, simportador protón-metal (Familia SLC11A2)
⚙️ Función
Absorción y transporte intracelular de metales divalentes (Fe2+, Zn2+, Mn2+)
📋 Impacto
Crucial para homeostasis de hierro, riesgo de toxicidad por metales pesados
¿Qué es el Transportador de Metales Divalentes 1 (DMT1)?
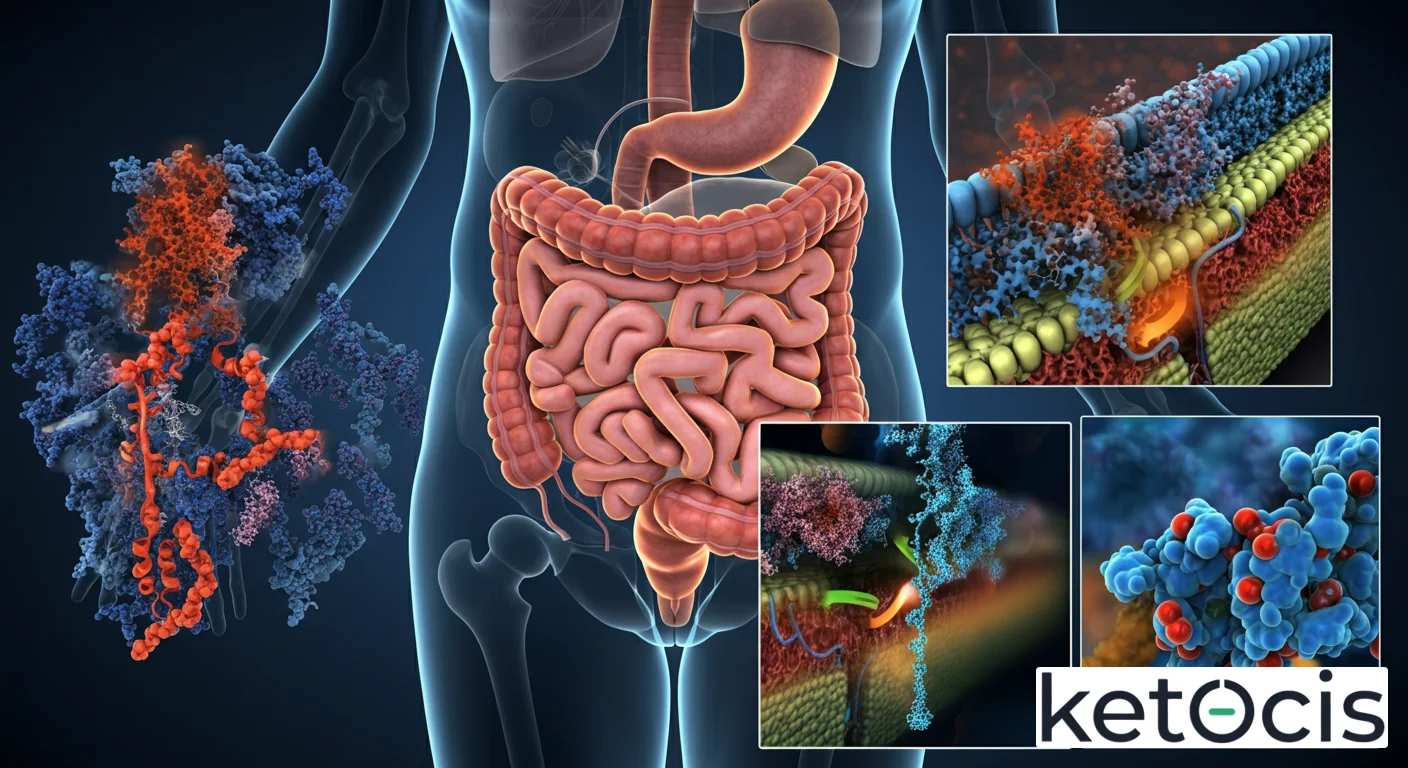
En el vasto y complejo universo de la fisiología humana, cada proteína, cada enzima, cada transportador cumple una función específica, orquestando una sinfonía molecular que sostiene la vida. Entre estos componentes vitales, el Transportador de Metales Divalentes 1 (DMT1) emerge como una figura central, un guardián molecular encargado de la importación de iones metálicos esenciales y, a veces, tóxicos, hacia el interior de nuestras células. Conocido también por su designación genética como SLC11A2 o su nombre histórico Nramp2 (Natural Resistance-Associated Macrophage Protein 2), el DMT1 es una proteína transmembrana fundamental para la homeostasis de metales, particularmente el hierro, un elemento indispensable para la vida.
Desde la absorción de nutrientes en el intestino hasta la función neuronal en el cerebro, el DMT1 ejerce su influencia, asegurando que las células obtengan los metales que necesitan para procesos enzimáticos, transporte de oxígeno y señalización, al tiempo que modula la entrada de aquellos que podrían ser perjudiciales. Su comprensión es clave no solo para la investigación biomédica, sino también para optimizar la salud metabólica, especialmente en contextos dietéticos específicos como la cetosis, donde la regulación de micronutrientes adquiere una relevancia particular.
Resumen Clínico
- El DMT1 es una proteína transmembrana esencial para la absorción y distribución de metales divalentes, especialmente hierro.
- Actúa como un simportador protón-metal, utilizando el gradiente de pH para introducir iones metálicos en la célula.
- Su disfunción está ligada a anemias, hemocromatosis y enfermedades neurodegenerativas, subrayando su papel crítico en la salud humana.
Origen y Naturaleza Molecular del DMT1
El DMT1 es una proteína integral de membrana perteneciente a la familia de transportadores de solutos (SLC, por sus siglas en inglés), específicamente a la subfamilia 11. Su estructura consta de múltiples dominios transmembrana que atraviesan la bicapa lipídica, creando un canal o poro a través del cual los iones metálicos pueden cruzar la membrana celular. La identificación de DMT1 fue un hito en la comprensión de la absorción de hierro, revelando un mecanismo molecular clave para este proceso vital. Su expresión es ubicua, encontrándose en una amplia variedad de tejidos, incluyendo el intestino delgado, el riñón, el hígado, la médula ósea, el bazo y, de manera crucial, el cerebro.
Existen varias isoformas del DMT1, generadas por splicing alternativo, que difieren principalmente en sus extremos C-terminales y en la presencia o ausencia de un elemento de respuesta al hierro (IRE) en su región 3′ no traducida (3’UTR). Estas isoformas exhiben distintas localizaciones subcelulares y patrones de regulación, lo que permite al organismo afinar la captación de metales según las necesidades del tejido y las condiciones fisiológicas. Por ejemplo, la isoforma con el IRE es sensible a los niveles de hierro intracelular y es crucial para la regulación de la absorción intestinal.
Mito: El hierro de las plantas se absorbe tan eficientemente como el de la carne.
Realidad: El hierro hemo de origen animal se absorbe de 2 a 3 veces más eficientemente que el hierro no hemo de las plantas. El DMT1 transporta solo hierro no hemo (Fe2+), cuya absorción es más susceptible a inhibidores dietéticos y requiere reducción previa por Dcytb.
El Mecanismo de Acción del DMT1: Un Simportador de Protones y Metales
La función principal del DMT1 es transportar iones metálicos divalentes desde el exterior al interior de la célula. Lo hace mediante un mecanismo de simporte protón-metal, lo que significa que el transporte del metal está acoplado al movimiento de un protón (H+) a favor de su gradiente electroquímico. Este gradiente de protones, mantenido por las bombas de protones (ATPases) en la membrana, proporciona la energía necesaria para mover los metales contra su propio gradiente de concentración.
En el intestino, por ejemplo, el ambiente ácido del lumen (pH bajo) y la actividad de la ATPasa de protón en la membrana apical de los enterocitos crean un gradiente favorable para el simporte de H+ junto con el hierro. El DMT1 tiene una alta afinidad por el hierro ferroso (Fe2+), la forma reducida del hierro, que es más soluble y biodisponible que el hierro férrico (Fe3+). Antes de ser transportado por DMT1, el hierro férrico dietético debe ser reducido a hierro ferroso por una ferrireductasa, como el citocromo b duodenal (Dcytb), presente en la membrana apical de los enterocitos.
DMT1 en la Absorción de Hierro: La Puerta de Entrada Duodenal
La absorción de hierro es un proceso meticulosamente regulado, ya que el hierro es esencial pero tóxico en exceso. El intestino delgado, específicamente el duodeno, es el sitio principal de absorción de hierro dietético. Aquí, el DMT1 se expresa abundantemente en la membrana apical (luminal) de los enterocitos duodenales. Su papel es crítico: es la principal puerta de entrada para el hierro no hemo (el hierro presente en alimentos vegetales y fortificados) desde el lumen intestinal hacia el interior de la célula.
Una vez dentro del enterocito, el hierro puede ser almacenado temporalmente en la ferritina o transportado a través de la membrana basolateral (hacia la sangre) por el transportador de hierro ferroportina (FPN1). La regulación coordinada de DMT1 y FPN1, junto con la ferrireductasa Dcytb y la ferroxidasa hefaestina, asegura que la cantidad adecuada de hierro sea absorbida y liberada al torrente sanguíneo, donde se unirá a la transferrina para su distribución. Este sistema es vital para prevenir tanto la deficiencia de hierro (anemia) como la sobrecarga (hemocromatosis).
Más Allá del Hierro: El DMT1 como Transportador de Metales Divalentes Múltiples
Aunque el hierro es su sustrato más conocido y fisiológicamente relevante, el DMT1 no es exclusivamente un transportador de hierro. Su nombre, Transportador de Metales Divalentes 1, refleja su capacidad para transportar una variedad de iones metálicos con una valencia de +2. Entre ellos se incluyen:
- Zinc (Zn2+): Un micronutriente esencial para cientos de enzimas y funciones celulares.
- Manganeso (Mn2+): Importante para enzimas antioxidantes y el metabolismo.
- Cobre (Cu2+): Crucial para la función enzimática y la formación de glóbulos rojos.
- Cobalto (Co2+): Componente de la vitamina B12.
Esta promiscuidad en el transporte, si bien ventajosa para la absorción de múltiples nutrientes, también presenta un riesgo. El DMT1 puede introducir metales pesados tóxicos, como el cadmio (Cd2+), el plomo (Pb2+) y el níquel (Ni2+), en las células. Esta capacidad subraya la importancia de controlar la exposición a estos contaminantes ambientales, ya que el DMT1 puede facilitar su acumulación en el organismo, contribuyendo a su toxicidad.
Biohacking
Para optimizar la absorción de hierro en el contexto de una dieta metabólicamente flexible o cetogénica, considera consumir fuentes de hierro hemo (carne roja, hígado) junto con alimentos ricos en vitamina C (pimientos, brócoli, bayas). La vitamina C potencia la reducción del hierro férrico a ferroso, facilitando su captación por DMT1 en el intestino, mejorando así la biodisponibilidad del hierro no hemo.
Regulación Fisiológica del DMT1: Una Danza Molecular de Homeostasis
La expresión y actividad del DMT1 están finamente reguladas para mantener la homeostasis de metales en el cuerpo. La regulación más estudiada es la del hierro, que se produce principalmente a través del sistema IRE/IRP (Elementos de Respuesta al Hierro/Proteínas Reguladoras del Hierro). Cuando los niveles de hierro intracelular son bajos, las IRPs se unen a los IREs presentes en el ARNm de proteínas como el DMT1 (en su isoforma con IRE) y la ferritina.
- En el caso del DMT1, la unión de IRP a su IRE en la región 3’UTR estabiliza el ARNm, aumentando la síntesis de la proteína y, por ende, la absorción de hierro.
- Por el contrario, cuando los niveles de hierro son altos, las IRPs se disocian de los IREs, lo que lleva a la degradación del ARNm del DMT1 y a una disminución de su expresión.
Además del sistema IRE/IRP, otros factores regulan el DMT1. La hepcidina, una hormona peptídica clave en la homeostasis del hierro, aunque actúa principalmente sobre la ferroportina, puede influir indirectamente en el DMT1. La hipoxia (bajos niveles de oxígeno) también puede aumentar la expresión de DMT1 a través del factor inducible por hipoxia (HIF), lo que sugiere un mecanismo para aumentar la captación de hierro en condiciones de baja disponibilidad de oxígeno.
Implicaciones Clínicas y Patologías Asociadas al DMT1
Dada su función central, no sorprende que las disfunciones del DMT1 estén asociadas con diversas patologías:
- Anemia por Deficiencia de Hierro: Mutaciones genéticas en el gen SLC11A2 que reducen la función del DMT1 pueden impedir una absorción adecuada de hierro, llevando a una anemia microcítica hipocrómica congénita refractaria a la terapia oral con hierro. Estos casos son raros, pero ilustran la importancia crítica del transportador.
- Hemocromatosis Tipo 4 (Enfermedad de la Ferroportina): Aunque no es una mutación directa del DMT1, las alteraciones en la ferroportina pueden afectar indirectamente la homeostasis del hierro, con la sobreexpresión compensatoria de DMT1 en algunos contextos.
- Enfermedades Neurodegenerativas: El DMT1 se expresa en el cerebro, particularmente en neuronas y células gliales. Se ha implicado en la patogénesis de enfermedades como el Parkinson y el Alzheimer, donde la desregulación del hierro y el estrés oxidativo son características prominentes. La sobreexpresión de DMT1 puede contribuir a la acumulación de hierro en ciertas regiones cerebrales, exacerbando el daño neuronal.
- Toxicidad por Metales Pesados: Como se mencionó, la capacidad del DMT1 para transportar metales tóxicos como el manganeso, plomo y cadmio, lo convierte en un punto de entrada para estos elementos en las células. La exposición crónica a estos metales puede llevar a su acumulación en órganos como el cerebro, riñones e hígado, causando disfunción y enfermedad. La toxicidad por manganeso, por ejemplo, puede causar un síndrome neurológico similar al Parkinson, en parte facilitado por la entrada de Mn2+ a través del DMT1.
Alerta Clínica
La suplementación excesiva de hierro sin una deficiencia confirmada puede ser peligrosa. Dado que DMT1 transporta hierro y otros metales, un exceso de hierro puede saturar los sistemas de transporte, alterar la homeostasis de otros metales esenciales como el zinc y el manganeso, y promover el estrés oxidativo. Siempre consulta a un profesional de la salud antes de iniciar suplementos de hierro para evitar riesgos metabólicos.
DMT1 y el Metabolismo en Contextos de Cetosis y Ayuno
En el contexto de dietas cetogénicas y ayuno intermitente, el cuerpo experimenta profundos cambios metabólicos, incluyendo la optimización del uso de grasas como combustible y una mayor flexibilidad metabólica. Si bien no hay una conexión directa y exclusiva que vincule el DMT1 con el estado de cetosis en sí mismo, la homeostasis de los metales que regula es fundamental para el funcionamiento celular en cualquier estado metabólico.
La producción de cuerpos cetónicos, la autofagia y la biogénesis mitocondrial, procesos clave en la cetosis y el ayuno, requieren un suministro adecuado de micronutrientes, incluyendo metales como el hierro, el zinc y el manganeso, todos ellos sustratos del DMT1. Por ejemplo, el hierro es crucial para la cadena de transporte de electrones en las mitocondrias, vital para la producción de ATP. El manganeso es un cofactor para la superóxido dismutasa de manganeso (MnSOD), una enzima antioxidante clave en la matriz mitocondrial. El zinc es esencial para la función de numerosas enzimas y para la integridad del ADN.
En un estado de cetosis, donde el cuerpo se vuelve más eficiente en el uso de energía y la reparación celular, mantener un equilibrio óptimo de estos metales es más importante que nunca. Una absorción deficiente o excesiva, mediada en parte por el DMT1, podría comprometer la eficacia de estos procesos adaptativos. Aunque la regulación directa del DMT1 por cuerpos cetónicos o vías de ayuno no ha sido extensamente dilucidada, es plausible que los cambios en el pH intracelular o en el estado redox celular durante estos estados metabólicos puedan influir indirectamente en la actividad del transportador.
Optimización y Estrategias para una Homeostasis Metálica Saludable
Para apoyar la función óptima del DMT1 y, por extensión, una homeostasis metálica saludable, se pueden considerar varias estrategias:
- Dieta Equilibrada: Consumir una variedad de alimentos ricos en micronutrientes, incluyendo fuentes de hierro hemo y no hemo, zinc, manganeso y cobre. La combinación de hierro no hemo con vitamina C puede mejorar su absorción.
- Evitar Inhibidores: Algunos compuestos dietéticos, como los fitatos (en cereales integrales y legumbres) y los taninos (en té y café), pueden quelar metales divalentes y reducir su absorción intestinal. Su consumo debe ser moderado o separado de las comidas ricas en hierro.
- Salud Intestinal: Un intestino sano, con una microbiota equilibrada y una barrera intestinal íntegra, es fundamental para una absorción eficiente y regulada de nutrientes. La inflamación intestinal puede afectar negativamente la función de DMT1 y otros transportadores.
- Minimizar Exposición a Metales Pesados: Reducir la exposición a fuentes de plomo, cadmio y mercurio en el ambiente (agua, alimentos, aire) es crucial, ya que el DMT1 puede facilitar su entrada al organismo.
El monitoreo de los niveles de micronutrientes, especialmente en individuos siguiendo dietas restrictivas o con condiciones de salud específicas, puede ser útil para asegurar un equilibrio adecuado.
Conclusión
El Transportador de Metales Divalentes 1 (DMT1) es una proteína de membrana de importancia incalculable. Desde su papel como la principal puerta de entrada para el hierro en el intestino hasta su participación en la captación de otros metales esenciales y tóxicos en diversos tejidos, el DMT1 es un actor clave en la homeostasis metálica. Su regulación precisa es vital para prevenir enfermedades relacionadas con la deficiencia o el exceso de metales, incluyendo anemias, trastornos neurodegenerativos y toxicidad por metales pesados.
Comprender el DMT1 no solo enriquece nuestro conocimiento de la fisiología fundamental, sino que también ofrece vías para la intervención clínica y estrategias de biohacking para optimizar la salud. En un mundo donde la nutrición y el metabolismo son cada vez más objeto de estudio y personalización, el DMT1 representa un recordatorio de la intrincada red molecular que sustenta nuestra salud y bienestar.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.