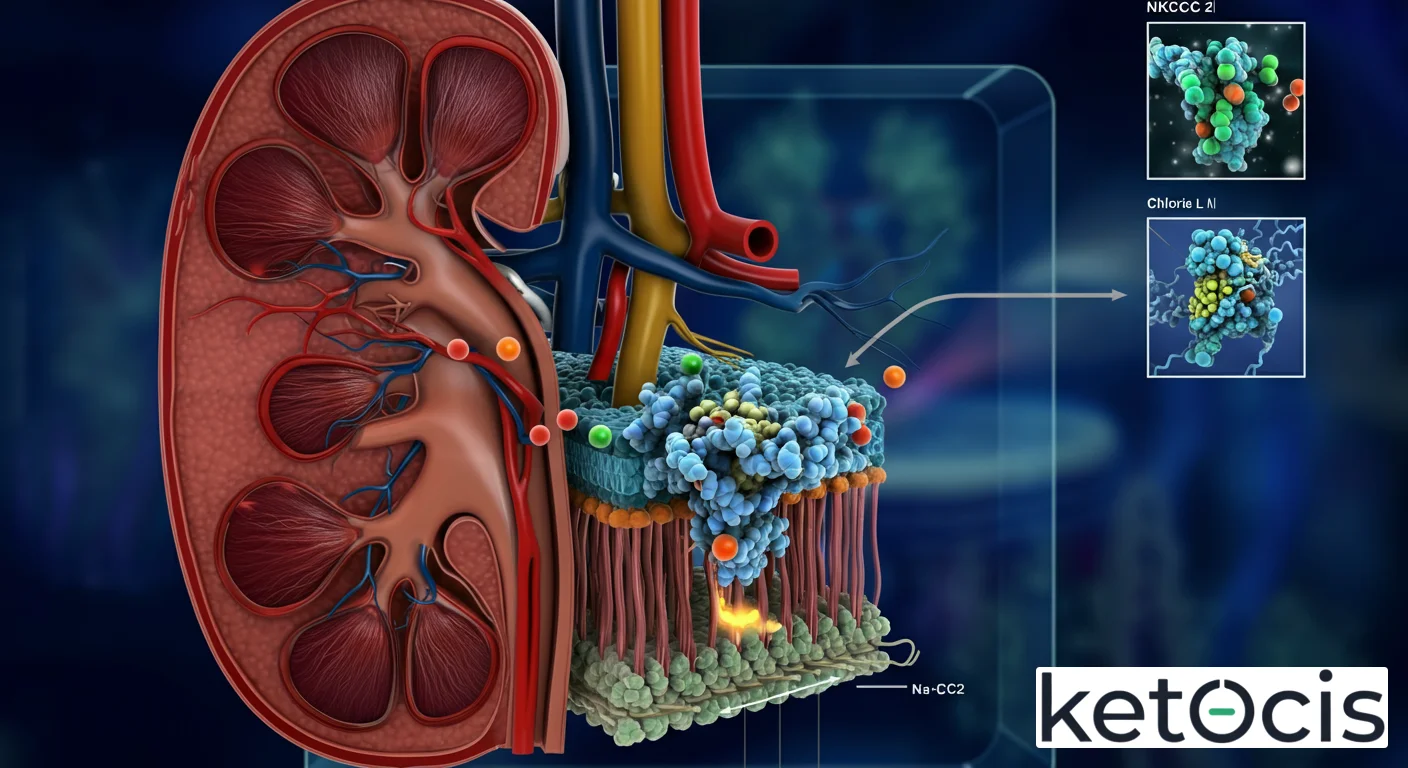
NKCC2: El Simportador Clave en Equilibrio Renal y Cetosis
Resumen Clínico Rápido
🔬 Clasificación
Simportador transmembrana (SLC12A1)
⚙️ Función
Reabsorción de Na+, K+, 2Cl- en el Asa de Henle
📋 Impacto
Regulación de volumen, presión arterial y concentración de orina
El Simportador Na-K-2Cl (NKCC2): Pilar de la Fisiología Renal y Equilibrio Metabólico
En el vasto y complejo universo de la fisiología humana, existen proteínas y transportadores moleculares que, aunque a menudo pasan desapercibidos, son absolutamente fundamentales para nuestra supervivencia y bienestar. Uno de estos héroes silenciosos es el simportador Na-K-2Cl, conocido comúnmente como NKCC2. Ubicado estratégicamente en los riñones, este transportador desempeña un papel crucial en la regulación del volumen de fluidos corporales, la presión arterial y el equilibrio de electrolitos, funciones que adquieren una relevancia aún mayor en estados metabólicos como la cetosis y el ayuno.
Como investigador médico con un profundo interés en la intersección entre la bioquímica, la fisiología y las estrategias de optimización de la salud, mi objetivo es desentrañar la complejidad del NKCC2. Esta guía exhaustiva, diseñada para el «Glosario Ketocis», explorará su estructura, mecanismo de acción, regulación y las implicaciones clínicas y metabólicas que lo convierten en un objeto de estudio fascinante y una diana terapéutica vital. Comprender el NKCC2 no es solo adentrarse en la mecánica renal, sino también entender cómo nuestro cuerpo gestiona los recursos hídricos y salinos bajo diferentes escenarios dietéticos y de estrés.
Resumen Clínico
- El NKCC2 es un cotransportador de sodio, potasio y dos iones cloro, esencial para la reabsorción de electrolitos en el riñón.
- Su actividad es fundamental para la capacidad del riñón de concentrar la orina y mantener el volumen sanguíneo y la presión arterial.
- Es la diana farmacológica de los diuréticos de asa, medicamentos potentes utilizados para tratar la retención de líquidos y la hipertensión.
Origen y Ubicación: El Corazón del Asa de Henle
El simportador Na-K-2Cl tipo 2, o NKCC2, es una proteína integral de membrana perteneciente a la familia de transportadores SLC12. Fue identificado y caracterizado por su papel predominante en el riñón, específicamente en el segmento grueso ascendente del asa de Henle (TAL, por sus siglas en inglés). Esta región del nefrón es crítica para la reabsorción de una porción significativa de los electrolitos filtrados, constituyendo aproximadamente el 25% del sodio y cloro que pasa por los glomérulos.
La presencia del NKCC2 en la membrana apical de las células del TAL le permite acceder directamente al filtrado glomerular. Su función allí es la de un cotransportador electroneutro, lo que significa que no genera un cambio neto en la carga eléctrica a través de la membrana, aunque sí mueve iones. La expresión de NKCC2 es regulada por diversas hormonas y factores, lo que subraya su importancia en la homeostasis renal y sistémica. Existen varias isoformas de NKCC2 (A, B y F), que se diferencian ligeramente en su cinética y localización subcelular, permitiendo una adaptación fina a las necesidades fisiológicas del organismo.
Los diuréticos de asa solo eliminan agua, sin afectar otros electrolitos.
Los diuréticos de asa, al inhibir el NKCC2, bloquean activamente la reabsorción de sodio, potasio y cloro, lo que lleva a una pérdida significativa de estos electrolitos junto con el agua, pudiendo causar desequilibrios graves como hipopotasemia e hiponatremia.
Fisiología Molecular: El Mecanismo de Acción del NKCC2
El mecanismo de acción del NKCC2 es un ballet molecular de alta precisión. Este transportador utiliza el gradiente electroquímico del sodio, generado por la bomba Na+/K+-ATPasa en la membrana basolateral de las células del TAL, para mover activamente sodio (Na+), potasio (K+) y dos iones de cloro (2Cl-) desde la luz tubular hacia el interior de la célula. Es crucial entender que, aunque el potasio se cotransporta, gran parte de él regresa a la luz tubular a través de canales de potasio (ROMK), creando un potencial positivo en la luz que impulsa la reabsorción paracelular de otros cationes como calcio y magnesio.
La reabsorción masiva de electrolitos mediada por el NKCC2 en el TAL tiene consecuencias profundas. Primero, es fundamental para la capacidad del riñón de generar un intersticio medular hipertónico. Este gradiente de osmolaridad es indispensable para que el conducto colector, bajo la influencia de la vasopresina (hormona antidiurética), reabsorba agua y produzca una orina concentrada. Sin la función adecuada del NKCC2, la capacidad de concentrar la orina se ve gravemente comprometida, resultando en una diuresis acuosa y la pérdida de electrolitos.
En segundo lugar, la reabsorción de sodio es un determinante clave del volumen extracelular y, por ende, de la presión arterial. Cualquier alteración en la actividad del NKCC2 puede tener un impacto directo en estos parámetros vitales. La comprensión de este mecanismo es la base para el diseño y uso de medicamentos que modulan la función renal.
Regulación Hormonal y Farmacológica
La actividad del NKCC2 no es estática; está finamente regulada por una compleja red de señales hormonales y factores paracrinos para adaptarse a las necesidades cambiantes del cuerpo. La vasopresina, también conocida como hormona antidiurética (ADH), es uno de los principales moduladores. Cuando los niveles de vasopresina aumentan (por ejemplo, debido a la deshidratación), esta hormona estimula la inserción de NKCC2 en la membrana apical y aumenta su actividad, potenciando la reabsorción de solutos y agua, lo que resulta en una orina más concentrada y la conservación de líquidos.
Otras hormonas como la angiotensina II, las prostaglandinas y el péptido natriurético atrial también influyen en la función del NKCC2, modulando su expresión o actividad para ajustar el equilibrio de sodio y el volumen sanguíneo. Por ejemplo, la angiotensina II tiende a aumentar la actividad del NKCC2, mientras que las prostaglandinas pueden inhibirla.
Desde una perspectiva farmacológica, el NKCC2 es la diana de una clase de medicamentos extremadamente potentes: los diuréticos de asa. Fármacos como la furosemida, la bumetanida y el ácido etacrínico actúan bloqueando competitivamente el sitio de unión del cloro en el NKCC2. Al inhibir este transportador, impiden la reabsorción de sodio, potasio y cloro, lo que lleva a una excreción masiva de estos electrolitos y, consecuentemente, de agua. Esta acción los convierte en herramientas vitales para el tratamiento de la insuficiencia cardíaca congestiva, la hipertensión y otras condiciones asociadas con la retención de líquidos.
El riñón, a través del NKCC2, es un maestro en la conservación de agua. En situaciones de deshidratación, la vasopresina puede aumentar la expresión de NKCC2 hasta en un 300% en minutos, permitiendo que tus riñones reabsorban una cantidad masiva de sal y, por ende, de agua, concentrando la orina hasta 10 veces más. ¡Un biohack natural de supervivencia!
NKCC2 en el Contexto de la Cetosis y el Ayuno
Para aquellos inmersos en el mundo de la cetosis y el ayuno intermitente o prolongado, la función del NKCC2 adquiere una relevancia particular. Al iniciar una dieta cetogénica o un período de ayuno, el cuerpo experimenta cambios significativos en el metabolismo y el equilibrio hidroelectrolítico. Una de las primeras adaptaciones es la depleción de glucógeno. Cada gramo de glucógeno se almacena con aproximadamente 3-4 gramos de agua. Al agotar estas reservas, se produce una diuresis inicial que lleva a una pérdida considerable de agua y electrolitos.
Durante esta fase, y a medida que el cuerpo se adapta a quemar grasas como fuente principal de energía, la demanda sobre los mecanismos de conservación de electrolitos del riñón puede aumentar. Si bien el NKCC2 no es directamente regulado por los cuerpos cetónicos, su actividad es crucial para mitigar la pérdida de sodio y potasio. Un funcionamiento óptimo del NKCC2 es esencial para prevenir la deshidratación y el desequilibrio electrolítico que a menudo contribuyen a la temida «gripe keto».
Además, la producción de cuerpos cetónicos, como el beta-hidroxibutirato y el acetoacetato, puede influir indirectamente en la función renal. Estos ácidos orgánicos se filtran y pueden actuar como aniones no reabsorbibles, lo que podría aumentar la excreción de sodio y potasio si no se compensa adecuadamente. La capacidad del NKCC2 para reabsorber una gran cantidad de sodio y potasio se vuelve un mecanismo de protección vital en este escenario, ayudando a mantener la homeostasis.
La hidratación adecuada y la suplementación estratégica de electrolitos son, por tanto, pilares fundamentales en la gestión de una dieta cetogénica o un protocolo de ayuno, en parte para apoyar el trabajo incansable del NKCC2 y otros transportadores renales.
Implicaciones Clínicas y Patológicas
Las disfunciones del NKCC2 pueden tener consecuencias clínicas graves. Un ejemplo paradigmático es el Síndrome de Bartter, un grupo de trastornos genéticos raros caracterizados por mutaciones en los genes que codifican el NKCC2 o proteínas asociadas. Los pacientes con Síndrome de Bartter presentan una pérdida renal de sal severa, hipopotasemia (niveles bajos de potasio), alcalosis metabólica e hipercalciuria (exceso de calcio en la orina). Esto se debe a que el NKCC2 defectuoso no puede reabsorber adecuadamente los electrolitos, imitando el efecto de los diuréticos de asa.
En el otro extremo del espectro, la hiperactividad del NKCC2 no es una patología común por sí misma, pero su modulación es clave en enfermedades como la hipertensión arterial. Los diuréticos de asa, al inhibir el NKCC2, reducen el volumen sanguíneo y la presión arterial, siendo tratamientos de primera línea en crisis hipertensivas o edemas agudos. Sin embargo, su uso debe ser monitorizado de cerca debido al riesgo de desequilibrios electrolíticos severos.
Alerta Médica: Uso de Diuréticos de Asa
El uso indiscriminado o no supervisado de diuréticos de asa (como la furosemida), que inhiben potentemente el NKCC2, puede llevar a una pérdida severa de electrolitos (sodio, potasio, cloro, calcio, magnesio) y agua. Esto puede provocar deshidratación grave, arritmias cardíacas, debilidad muscular y, en casos extremos, compromiso renal agudo. Nunca uses diuréticos sin la indicación y supervisión de un profesional de la salud, especialmente si sigues una dieta cetogénica o ayunas, donde el equilibrio electrolítico ya es delicado.
Optimización y Salud Renal en el Contexto del NKCC2
Mantener una función renal saludable es fundamental para la actividad óptima del NKCC2 y, por extensión, para el equilibrio general del cuerpo. Aquí hay algunas consideraciones clave:
- Hidratación Adecuada: Beber suficiente agua es crucial para el riñón. La deshidratación crónica puede estresar los mecanismos de conservación de agua, incluido el NKCC2.
- Equilibrio Electrolítico: Asegurar una ingesta adecuada de sodio, potasio y magnesio a través de la dieta es vital. En dietas cetogénicas, esto es aún más crítico debido a la mayor excreción inicial de estos iones.
- Evitar el Exceso de Sal y Azúcar: Un consumo excesivo de sodio puede aumentar la presión arterial y forzar al riñón a trabajar más para excretar el exceso. El azúcar, por otro lado, puede contribuir a la diabetes, una de las principales causas de enfermedad renal crónica.
- Control de la Presión Arterial: La hipertensión crónica daña los vasos sanguíneos renales, afectando la capacidad de los nefrones para funcionar correctamente, incluido el TAL y el NKCC2.
- Ejercicio Regular: La actividad física mejora la salud cardiovascular y renal en general, lo que indirectamente apoya la función de transportadores como el NKCC2.
El monitoreo regular de la función renal y los electrolitos es especialmente importante para individuos con condiciones preexistentes o aquellos que utilizan estrategias dietéticas que pueden influir en el equilibrio hídrico y salino. Entender cómo el NKCC2 contribuye a estos procesos empodera a las personas para tomar decisiones más informadas sobre su salud.
Conclusión: Un Transportador Esencial para la Vida
El simportador Na-K-2Cl (NKCC2) es mucho más que una simple proteína de membrana; es un componente crítico de la maquinaria renal que orquesta el equilibrio de fluidos y electrolitos, la concentración de orina y la regulación de la presión arterial. Su intrincada fisiología molecular, su regulación hormonal y su rol como diana farmacológica lo sitúan en el centro de la investigación médica y la práctica clínica.
Desde la perspectiva del “Glosario Ketocis”, comprender el NKCC2 nos ilumina sobre los desafíos y adaptaciones que el cuerpo humano experimenta durante la cetosis y el ayuno. Reconocer la importancia de este transportador nos impulsa a adoptar estrategias de biohacking conscientes, como la gestión meticulosa de electrolitos e hidratación, para optimizar la salud metabólica y renal. El NKCC2 es, sin duda, un testimonio de la elegancia y eficiencia con la que nuestro organismo mantiene la homeostasis frente a un entorno interno y externo en constante cambio.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.