TfR1: El Receptor de Transferrina 1 y el Metabolismo del Hierro
Resumen Clínico Rápido
🔬 Clasificación
Glicoproteína transmembrana tipo II, Homodímero
⚙️ Función
Principal receptor para la captación de hierro (Fe³⁺) mediada por transferrina
📋 Impacto
Esencial para eritropoyesis, proliferación celular, desarrollo cerebral; biomarcador y objetivo terapéutico
El Receptor de Transferrina 1 (TfR1): Guardián Molecular del Hierro Celular
En el intrincado universo de la biología celular, donde cada molécula desempeña un papel coreográfico para mantener la homeostasis, el Receptor de Transferrina 1 (TfR1) emerge como una figura central. Este receptor de superficie celular no es meramente una puerta de entrada; es el principal regulador de la captación de hierro en la mayoría de las células de mamíferos, un elemento indispensable para procesos biológicos tan fundamentales como la respiración celular, la síntesis de ADN y la proliferación. Su comprensión es clave no solo para desentrañar los mecanismos de la vida, sino también para abordar patologías que van desde la anemia ferropénica hasta el cáncer y las enfermedades neurodegenerativas.
El hierro es un metal de transición esencial, pero su naturaleza redox lo convierte en un arma de doble filo. Si bien es vital para la función enzimática y el transporte de oxígeno, su acumulación excesiva puede generar especies reactivas de oxígeno (ROS) y daño celular. Por lo tanto, el organismo ha desarrollado sistemas altamente sofisticados para su absorción, transporte, almacenamiento y utilización. El TfR1 se sitúa en el epicentro de esta compleja red, dictando el ritmo al que las células adquieren el hierro del torrente sanguíneo para satisfacer sus demandas metabólicas.
Esta guía enciclopédica, diseñada para el exigente Glosario Ketocis, explorará en profundidad la naturaleza, el mecanismo de acción, las funciones fisiológicas y las implicaciones clínicas del TfR1, ofreciendo una perspectiva autoritativa y fascinante sobre su rol insustituible en la salud y la enfermedad.
Resumen Clínico
- El Receptor de Transferrina 1 (TfR1) es la principal puerta de entrada para el hierro en la mayoría de las células, crucial para su supervivencia y proliferación.
- Su expresión está finamente regulada por los niveles de hierro intracelular a través de las Proteínas Reguladoras de Hierro (IRPs), asegurando una homeostasis precisa.
- Más allá del metabolismo del hierro, TfR1 desempeña roles críticos en la eritropoyesis, la respuesta inmunitaria, el desarrollo neuronal y puede ser un objetivo terapéutico en el cáncer y otras enfermedades.
Más hierro siempre es mejor para la energía y la salud.
El exceso de hierro es tóxico. Puede generar estrés oxidativo, dañar órganos y aumentar el riesgo de enfermedades crónicas. La homeostasis del hierro es crucial, y la suplementación solo debe realizarse bajo supervisión médica y tras confirmar una deficiencia.
Origen y Naturaleza Molecular del Receptor de Transferrina 1
El TfR1, codificado por el gen TFRC en humanos, es una glicoproteína transmembrana tipo II que existe como un homodímero en la superficie celular. Cada monómero tiene una masa molecular de aproximadamente 90-95 kDa y consta de tres dominios principales: un pequeño dominio citoplasmático N-terminal, un dominio transmembrana y un gran dominio extracelular C-terminal. Este último es el sitio de unión para su ligando principal, la transferrina.
La transferrina es una glicoproteína sérica que transporta el hierro férrico (Fe³⁺) de forma segura y soluble en el plasma. Cada molécula de transferrina puede unir dos iones de hierro. Es esta forma de transferrina, saturada con hierro (diferric transferrin), la que es reconocida con alta afinidad por el TfR1. La ubicuidad del TfR1 en la mayoría de los tejidos, con una expresión particularmente alta en células que requieren grandes cantidades de hierro como los eritroblastos (precursores de glóbulos rojos) y las células proliferativas (incluidas las cancerosas), subraya su importancia fundamental.
La investigación sobre el TfR1 comenzó a cobrar fuerza en la década de 1980, revelando su estructura y función esenciales en el transporte de hierro. Desde entonces, ha sido objeto de estudio intensivo debido a su papel multifacético en la fisiología y la patología.
Mecanismo de Acción: La Danza Molecular del Hierro Celular
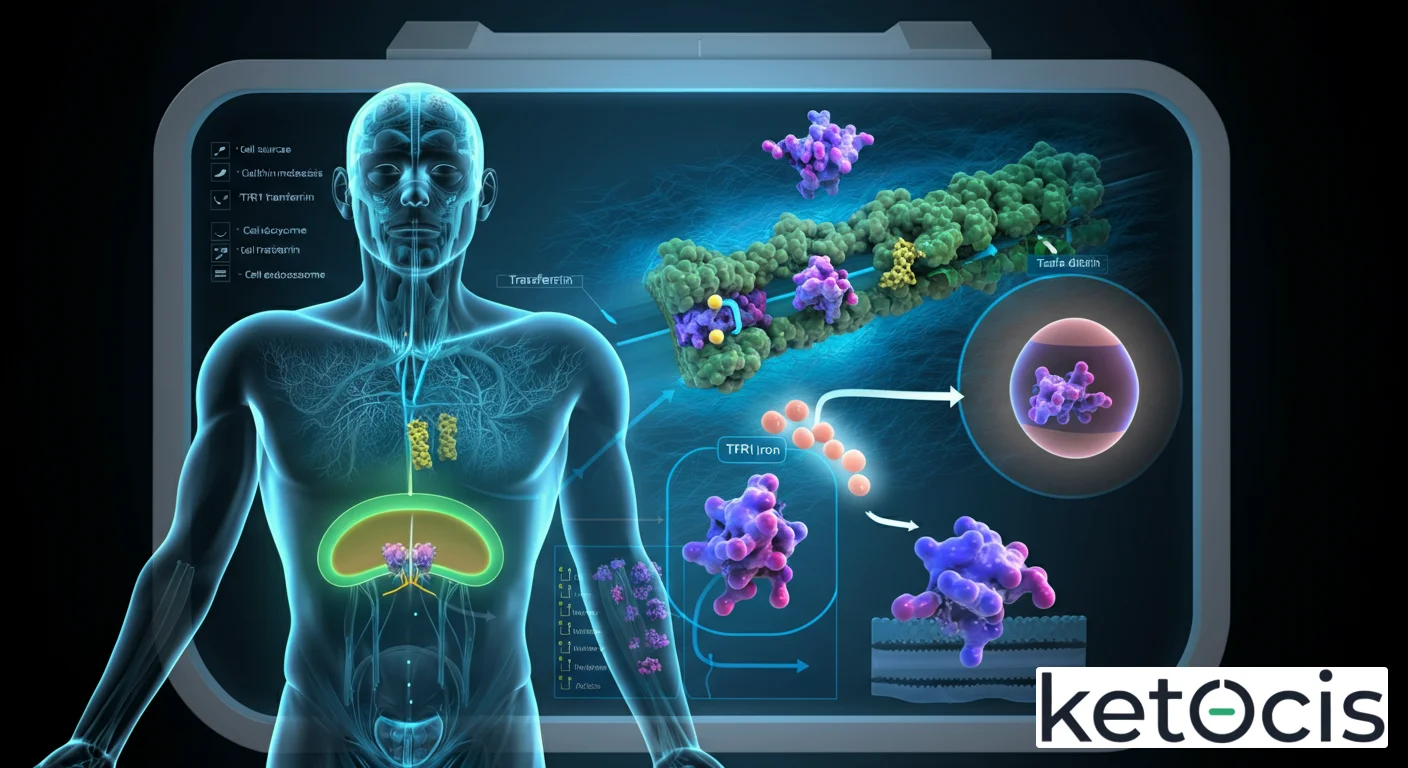
El proceso por el cual el TfR1 facilita la entrada de hierro a la célula es un ejemplo elegante de endocitosis mediada por receptor. Este mecanismo se puede desglosar en varios pasos clave:
- Unión Ligando-Receptor: La transferrina diferrica (con dos átomos de hierro) en el plasma se une con alta afinidad al dominio extracelular del TfR1 en la superficie celular.
- Endocitosis: El complejo TfR1-transferrina-hierro es internalizado en la célula a través de vesículas recubiertas de clatrina, formando un endosoma temprano.
- Acidificación del Endosoma: Las bombas de protones (ATPases de tipo V) en la membrana del endosoma acidifican el lumen, reduciendo el pH de aproximadamente 7.4 a 5.5-6.0. Este ambiente ácido induce un cambio conformacional en la transferrina, lo que disminuye su afinidad por el hierro.
- Liberación del Hierro: En este entorno ácido, los dos iones de Fe³⁺ se disocian de la transferrina. Una vez liberado, el Fe³⁺ es reducido a Fe²⁺ por una ferrireductasa endosomal (como STEAP3) y luego transportado al citosol a través del transportador de metales divalentes DMT1 (SLC11A2) en la membrana del endosoma.
- Reciclaje del Receptor: Una vez que el hierro es liberado, la transferrina ahora sin hierro (apotransferrina) permanece unida al TfR1 en el ambiente ácido. El complejo TfR1-apotransferrina es reciclado rápidamente de vuelta a la superficie celular. Al alcanzar el pH neutro extracelular, la apotransferrina se disocia del TfR1 y es liberada al plasma para volver a cargar hierro, mientras que el TfR1 queda disponible para iniciar un nuevo ciclo de captación de hierro.
Este ciclo eficiente asegura un suministro constante de hierro a la célula sin la acumulación de transferrina o TfR1 en el interior, manteniendo la homeostasis del hierro.
Funciones Fisiológicas Más Allá de la Captación de Hierro
Aunque su función principal es la captación de hierro, la omnipresencia y la regulación precisa del TfR1 sugieren roles más amplios en la fisiología celular:
- Eritropoyesis: Las células precursoras de los glóbulos rojos (eritroblastos) tienen una demanda excepcionalmente alta de hierro para la síntesis de hemoglobina. La alta expresión de TfR1 en estas células es fundamental para la producción de glóbulos rojos funcionales. Una deficiencia en TfR1 o en el suministro de hierro puede llevar a anemias.
- Proliferación Celular y Cáncer: Las células en rápida división, como las células cancerosas, tienen una necesidad elevada de hierro para la replicación del ADN y la producción de energía. Consecuentemente, muchas células tumorales sobreexpresan TfR1, lo que las convierte en un objetivo atractivo para terapias dirigidas que buscan privarlas de hierro.
- Sistema Inmune: Las células inmunes, especialmente los linfocitos T activados, aumentan su expresión de TfR1 para satisfacer sus necesidades metabólicas durante la proliferación y diferenciación, destacando el papel del hierro en la respuesta inmunitaria.
- Neurodesarrollo y Función Cerebral: El cerebro es particularmente vulnerable a las alteraciones en la homeostasis del hierro. TfR1 es crucial para el suministro de hierro a las neuronas y otras células cerebrales, siendo esencial para el desarrollo neuronal, la mielinización y la función cognitiva. Su disfunción se ha relacionado con enfermedades neurodegenerativas como el Alzheimer y el Parkinson.
- Entrada Viral: Sorprendentemente, TfR1 también actúa como receptor de entrada para ciertos virus, incluyendo el virus de la coriomeningitis linfocítica (LCMV) y algunos retrovirus, lo que añade otra capa de complejidad a sus funciones.
Regulación y Antagonistas del TfR1: Manteniendo el Equilibrio
La expresión de TfR1 está finamente regulada para asegurar que las células obtengan la cantidad justa de hierro, ni demasiado ni muy poco. Los principales orquestadores de esta regulación son las Proteínas Reguladoras de Hierro (IRPs), IRP1 e IRP2, que detectan los niveles de hierro intracelular y modulan la traducción de ARNm o la estabilidad de ARNm de genes relacionados con el metabolismo del hierro.
Cuando los niveles de hierro son bajos, las IRPs se unen a secuencias específicas en los ARNm llamadas Elementos de Respuesta al Hierro (IREs). El ARNm del TfR1 contiene IREs en su región 3′ no traducida (3′ UTR). La unión de las IRPs a estas IREs estabiliza el ARNm del TfR1, lo que lleva a un aumento en la síntesis de la proteína TfR1 y, por ende, a una mayor captación de hierro.
Por el contrario, cuando los niveles de hierro son altos, las IRPs se disocian de los IREs del ARNm del TfR1, lo que resulta en la degradación del ARNm y una disminución de la expresión de TfR1, reduciendo así la captación de hierro.
Además de esta regulación post-transcripcional, la expresión de TfR1 puede ser influenciada por factores como la hipoxia, los factores de crecimiento y las citoquinas. La forma soluble del receptor de transferrina (sTfR), que se genera por el corte proteolítico del dominio extracelular de TfR1, circula en la sangre y es un biomarcador útil para evaluar el estado del hierro y la eritropoyesis, especialmente en la diferenciación entre anemia ferropénica y anemia de enfermedad crónica.
TfR1 en el Contexto Metabólico: Cetosis y Ayuno
La relación entre el TfR1 y estados metabólicos como la cetosis o el ayuno es un área de investigación emergente y fascinante. Tanto la dieta cetogénica como el ayuno intermitente inducen cambios profundos en el metabolismo energético celular, afectando vías de señalización clave como mTOR y AMPK, y alterando la disponibilidad de nutrientes.
El hierro es un cofactor esencial para numerosas enzimas mitocondriales involucradas en la cadena de transporte de electrones y, por lo tanto, es crítico para la producción eficiente de ATP. En estados de cetosis, donde las mitocondrias se adaptan para quemar grasas como principal fuente de combustible, un suministro adecuado de hierro es imperativo para mantener la función mitocondrial óptima. Si bien no hay evidencia directa y masiva que vincule la dieta cetogénica o el ayuno con una alteración drástica en la expresión general de TfR1 en individuos sanos, se pueden inferir algunas interacciones:
- Demanda de Hierro en Proliferación: Si la dieta cetogénica o el ayuno tienen un efecto antiproliferativo en ciertos tejidos (como se sugiere en algunos modelos de cáncer), esto podría teóricamente reducir la demanda de hierro y, por ende, la expresión de TfR1 en esas células.
- Inflamación y Homeostasis del Hierro: La cetosis y el ayuno pueden modular la inflamación. La inflamación crónica a menudo conduce a la “anemia de la enfermedad crónica”, donde el hierro se secuestra en los macrófagos y la expresión de TfR1 puede ser alterada en un intento de conservar hierro. Si la cetosis reduce la inflamación, podría indirectamente influir en la biodisponibilidad del hierro y la regulación del TfR1.
- Señalización Celular: Vías como AMPK, activada durante el ayuno, pueden influir en la expresión génica y proteica. Se ha demostrado que AMPK regula la expresión de genes de metabolismo del hierro en algunas condiciones, sugiriendo un posible enlace indirecto con TfR1.
Es importante destacar que cualquier intervención dietética debe considerar el estado individual del hierro. Una persona con deficiencia de hierro podría experimentar un impacto diferente en la regulación del TfR1 en comparación con alguien con reservas adecuadas. La investigación futura probablemente arrojará más luz sobre estas interacciones complejas.
Implicaciones Clínicas: Biomarcador y Objetivo Terapéutico
La importancia del TfR1 se extiende al ámbito clínico, donde sirve tanto como biomarcador como objetivo terapéutico potencial:
- Diagnóstico de Deficiencia de Hierro: Los niveles séricos de sTfR son un indicador sensible de la deficiencia de hierro funcional y la eritropoyesis. A diferencia de la ferritina (que puede elevarse en la inflamación), el sTfR no se ve afectado por la inflamación, lo que lo convierte en una herramienta valiosa para distinguir la anemia ferropénica de la anemia de enfermedad crónica.
- Cáncer: La sobreexpresión de TfR1 en muchas células cancerosas lo convierte en un blanco atractivo. Estrategias que buscan bloquear la captación de hierro a través de TfR1, ya sea con anticuerpos monoclonales o pequeñas moléculas, están siendo investigadas como terapias anticáncer. La privación de hierro puede inducir estrés oxidativo y apoptosis en células tumorales.
- Enfermedades Neurodegenerativas: La desregulación del hierro en el cerebro es un sello distintico de varias enfermedades neurodegenerativas. La modulación de la actividad de TfR1 podría ser una estrategia para restaurar la homeostasis del hierro cerebral y mitigar el daño neuronal.
- Trastornos de Sobrecarga de Hierro: En condiciones como la hemocromatosis hereditaria, donde hay una absorción excesiva de hierro, la comprensión de cómo se regula TfR1 es vital para desarrollar terapias que puedan reducir la carga de hierro.
Alerta Metabólica
La suplementación con hierro, aunque vital para la deficiencia, no debe tomarse a la ligera. La creencia de que «más hierro siempre es mejor» es un mito peligroso. Un exceso de hierro puede ser altamente tóxico, promoviendo el estrés oxidativo, dañando órganos como el hígado y el corazón, e incluso aumentando el riesgo de ciertas enfermedades crónicas, incluido el cáncer. Antes de considerar cualquier suplemento de hierro, es crucial realizar análisis de sangre para confirmar una deficiencia. La automedicación puede llevar a una sobrecarga de hierro, una condición silenciosa pero potencialmente devastadora para la salud metabólica.
Conclusión: El TfR1 como Eje de la Vida Celular
El Receptor de Transferrina 1 es mucho más que un simple canal para el hierro. Es un sensor dinámico y un regulador maestro de uno de los nutrientes más vitales, orquestando su entrada en las células para apoyar una miríada de procesos fisiológicos. Desde la formación de glóbulos rojos hasta la intrincada maquinaria de la división celular y la función cerebral, el TfR1 es un actor indispensable.
Su compleja regulación por los niveles de hierro y su papel en diversas patologías lo convierten en un foco continuo de investigación. A medida que profundizamos en la interacción entre el TfR1 y estados metabólicos como la cetosis, se abren nuevas vías para comprender la salud y la enfermedad, y para desarrollar estrategias terapéuticas y de biohacking más inteligentes. La historia del TfR1 es un testimonio de la elegancia y la interconexión de la biología molecular, recordándonos que incluso las proteínas más pequeñas pueden tener un impacto monumental en la gran sinfonía de la vida.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.