HIF: Factor Inducible por Hipoxia | Glosario Ketocis
Resumen Clínico Rápido
🔬 Clasificación
Factor de transcripción
⚙️ Función
Regulación de la homeostasis del oxígeno
📋 Impacto
Supervivencia celular, cáncer, enfermedades metabólicas
¿Qué es el Factor Inducible por Hipoxia (HIF)? Un Pilar de la Adaptación Celular
En el intrincado universo de la biología celular, donde la vida se aferra a un equilibrio precario, el Factor Inducible por Hipoxia (HIF) emerge como un protagonista fundamental. Este complejo proteico no es solo un sensor de oxígeno, sino el maestro director de una orquesta molecular que permite a nuestras células y, por extensión, a todo el organismo, adaptarse y sobrevivir en condiciones de baja disponibilidad de oxígeno, un estado conocido como hipoxia. Desde la cima de una montaña hasta el corazón de un tumor, la capacidad de detectar y responder a los cambios en los niveles de oxígeno es crucial para la homeostasis y la supervivencia.
La hipoxia es una condición común que enfrentan las células en diversas situaciones fisiológicas y patológicas, desde el desarrollo embrionario y el ejercicio intenso hasta enfermedades como la isquemia, el cáncer y las enfermedades respiratorias crónicas. La respuesta celular a la hipoxia debe ser rápida y coordinada, reconfigurando el metabolismo, promoviendo la formación de nuevos vasos sanguíneos y ajustando la producción de glóbulos rojos. HIF es el eje central de esta respuesta adaptativa, orquestando la expresión de cientos de genes que facilitan la supervivencia y la función celular bajo estrés hipóxico. Su estudio no solo desvela secretos de la fisiología fundamental, sino que también abre avenidas prometedoras para el tratamiento de una vasta gama de enfermedades.
Resumen Clínico
- Sensor de Oxígeno: HIF es el principal regulador de la respuesta celular a la hipoxia, detectando variaciones en los niveles de oxígeno.
- Maestro de Transcripción: Activa la expresión de cientos de genes involucrados en metabolismo, angiogénesis, eritropoyesis y supervivencia celular.
- Relevancia Biomédica: Crucial en fisiología (ejercicio, altitud) y patología (cáncer, isquemia, enfermedades metabólicas), siendo una diana terapéutica clave.
Propósito Evolutivo: La Supervivencia en un Mundo Variable
El Oxígeno como Impulsor y Limitante
La Tierra primitiva, con su atmósfera anóxica, dio paso a un planeta rico en oxígeno gracias a la actividad fotosintética. Este cambio revolucionario, la Gran Oxidación, no solo permitió el florecimiento de la vida compleja, sino que también impuso una nueva presión selectiva. El oxígeno, aunque esencial para la respiración aeróbica y la producción eficiente de energía, es también una molécula reactiva que puede generar especies dañinas. Además, su disponibilidad no es constante; fluctúa con la altitud, la actividad física y el estado fisiológico o patológico de los tejidos. La evolución, por tanto, tuvo que dotar a los organismos de mecanismos sofisticados para gestionar el oxígeno de manera óptima, evitando tanto su escasez como su exceso.
En este contexto, la capacidad de las células para percibir y responder a la disponibilidad de oxígeno se convirtió en una ventaja evolutiva inmensa. Los organismos que podían ajustar su metabolismo y fisiología para adaptarse a la hipoxia tenían mayores probabilidades de sobrevivir y reproducirse. Este proceso de adaptación no es trivial; implica una reconfiguración energética profunda, priorizando vías que no dependen de oxígeno o que lo utilizan de manera más eficiente. El HIF representa la culminación de millones de años de evolución en la gestión del oxígeno, un sistema de alarma y respuesta que ha sido conservado a lo largo de las especies.
Orígenes de la Adaptación
Desde organismos unicelulares hasta mamíferos complejos, la señalización por oxígeno es un proceso fundamental. Las primeras formas de vida desarrollaron vías metabólicas anaeróbicas para sobrevivir en ambientes con poco o ningún oxígeno. Con la aparición del oxígeno, surgieron las vías aeróbicas, mucho más eficientes energéticamente. Sin embargo, la necesidad de alternar o complementar estas vías persistió. Se cree que los precursores del sistema HIF evolucionaron para mediar esta transición, permitiendo a las células cambiar su estrategia metabólica en función de la disponibilidad de oxígeno.
El sistema HIF es un ejemplo paradigmático de cómo la evolución reutiliza y refina módulos moleculares para nuevas funciones. En su esencia, HIF es un factor de transcripción, una proteína que se une al ADN para controlar la expresión génica. Su particularidad radica en que su estabilidad y actividad están directamente ligadas a la presencia de oxígeno. Esta maquinaria molecular altamente conservada subraya la importancia crítica de la homeostasis del oxígeno para la vida tal como la conocemos, conectando directamente la disponibilidad de este gas vital con el destino y la función celular.
Conexión con el Metabolismo
Una de las funciones más críticas de HIF es su capacidad para reprogramar el metabolismo celular. En condiciones de normoxia (niveles normales de oxígeno), las células prefieren la fosforilación oxidativa, una vía altamente eficiente que produce grandes cantidades de ATP utilizando oxígeno. Sin embargo, cuando el oxígeno es escaso, HIF induce un cambio hacia la glucólisis anaeróbica, una vía menos eficiente pero que no requiere oxígeno. Este fenómeno, conocido en el contexto del cáncer como el efecto Warburg, permite a las células generar ATP rápidamente, aunque a costa de una menor eficiencia energética.
La inducción de genes glucolíticos como GLUT1 (transportador de glucosa) y diversas enzimas glucolíticas por HIF asegura que la célula pueda captar más glucosa y procesarla para obtener energía, incluso en ausencia de oxígeno. Este cambio metabólico es vital no solo para la supervivencia en la hipoxia aguda, sino también para procesos fisiológicos como el desarrollo y la adaptación al ejercicio, donde la demanda de energía puede exceder momentáneamente el suministro de oxígeno.
La activación de HIF siempre es beneficiosa para la salud.
Aunque esencial para la adaptación a la hipoxia fisiológica, la activación descontrolada o crónica de HIF puede promover el crecimiento tumoral, la angiogénesis patológica y la progresión de enfermedades crónicas, demostrando su naturaleza de doble filo.
Fisiología Molecular: El Intrincado Mecanismo de HIF
Estructura y Subunidades
El Factor Inducible por Hipoxia es un heterodímero, lo que significa que está compuesto por dos subunidades diferentes: una subunidad alfa (HIF-α) y una subunidad beta (HIF-β). Existen tres isoformas de HIF-α: HIF-1α, HIF-2α y HIF-3α. De estas, HIF-1α y HIF-2α son las más estudiadas y funcionalmente relevantes. La subunidad HIF-β, también conocida como ARNT (aryl hydrocarbon receptor nuclear translocator), es constitutiva, es decir, está presente de forma constante en la célula, independientemente de los niveles de oxígeno. La clave de la regulación de HIF reside en la subunidad alfa, que es altamente sensible a la disponibilidad de oxígeno.
HIF-1α y HIF-2α comparten similitudes estructurales, incluyendo dominios de unión al ADN y dominios de transactivación, pero difieren en su patrón de expresión y en los genes diana que regulan, confiriendo especificidad a la respuesta hipóxica. HIF-1α es el principal mediador de la respuesta general a la hipoxia, mientras que HIF-2α a menudo media respuestas más específicas, como la eritropoyesis y la vasculogénesis en ciertos tejidos.
Regulación por Oxígeno
La magia de HIF reside en su sofisticada regulación dependiente del oxígeno. Este mecanismo asegura que HIF solo esté activo cuando el oxígeno es escaso, evitando una activación innecesaria y potencialmente dañina.
-
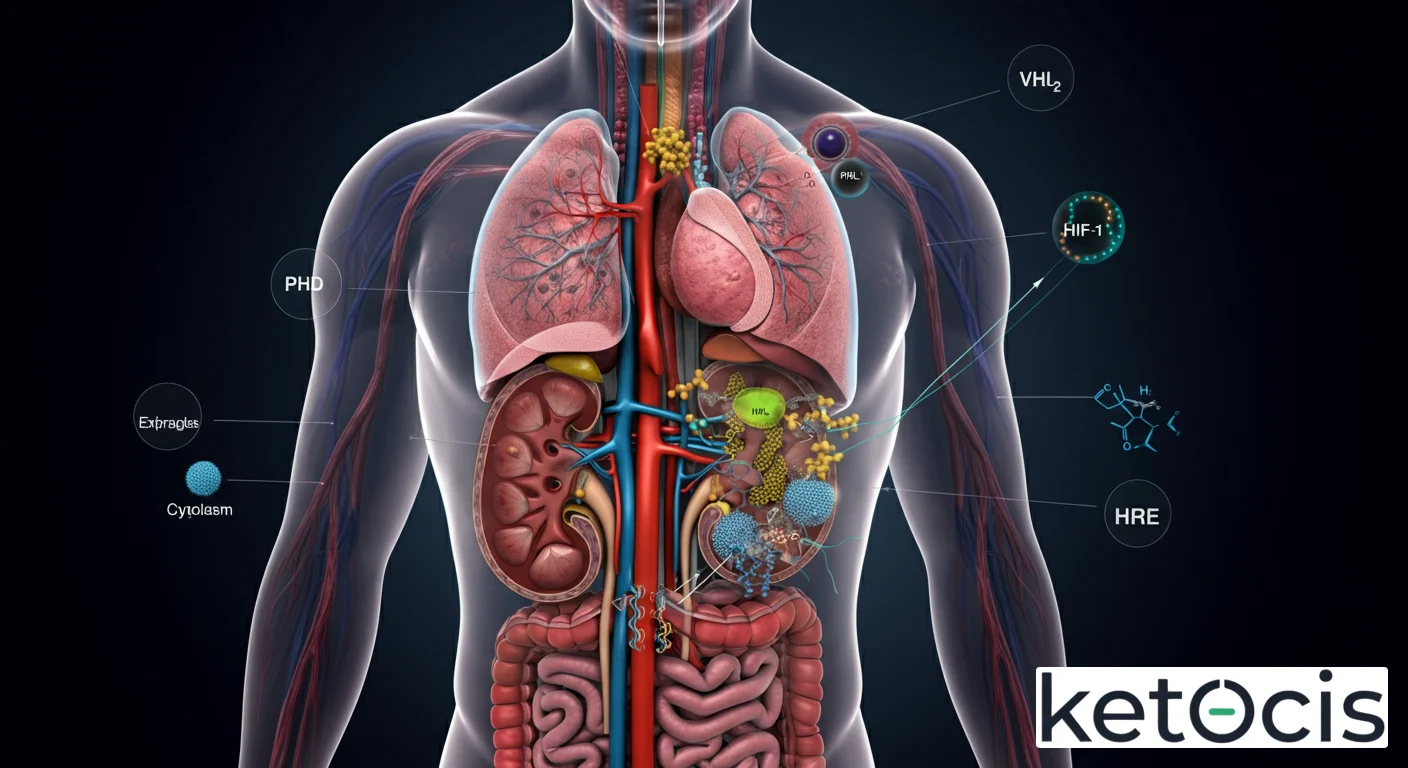
En Normoxia (Oxígeno Normal): Bajo condiciones de oxígeno abundante, la subunidad HIF-α es hidroxilada rápidamente. Esta hidroxilación ocurre en residuos de prolina específicos dentro de HIF-α y es catalizada por una familia de enzimas llamadas prolil hidroxilasas (PHDs). Las PHDs requieren oxígeno como cosustrato, lo que las convierte en los sensores moleculares clave. Una vez hidroxilada, HIF-α es reconocida por la proteína VHL (von Hippel-Lindau), que forma parte de un complejo ubiquitina ligasa. VHL marca a HIF-α para su degradación por el proteasoma, un complejo proteico que descompone proteínas no deseadas o dañadas. Como resultado, en normoxia, los niveles de HIF-α son extremadamente bajos y el factor de transcripción permanece inactivo.
-
En Hipoxia (Bajo Oxígeno): Cuando los niveles de oxígeno disminuyen, la actividad de las PHDs se inhibe drásticamente debido a la falta de sustrato. Sin hidroxilación, HIF-α ya no es reconocida por VHL y, por lo tanto, escapa a la degradación proteasomal. Esto lleva a una rápida acumulación y estabilización de HIF-α en el citoplasma. Una vez estabilizada, HIF-α se trasloca al núcleo, donde se heterodimeriza con la subunidad constitutiva HIF-β (ARNT). El complejo HIF-α/HIF-β se une entonces a secuencias específicas de ADN conocidas como Elementos de Respuesta a Hipoxia (HREs), localizadas en las regiones promotoras de sus genes diana. Esta unión recluta coactivadores transcripcionales, iniciando la expresión de una amplia variedad de genes.
Genes Diana de HIF
La activación de HIF desencadena una cascada de eventos que altera profundamente la fisiología celular. Los genes diana de HIF son increíblemente diversos y abarcan funciones críticas para la adaptación a la hipoxia:
-
Angiogénesis: HIF induce la expresión del factor de crecimiento endotelial vascular (VEGF), una proteína clave que estimula la formación de nuevos vasos sanguíneos para restaurar el suministro de oxígeno a los tejidos hipóxicos.
-
Eritropoyesis: HIF promueve la síntesis de eritropoyetina (EPO), una hormona que estimula la producción de glóbulos rojos en la médula ósea, aumentando la capacidad de transporte de oxígeno de la sangre.
-
Metabolismo de la Glucosa: HIF activa genes que facilitan la captación de glucosa (ej., GLUT1) y enzimas glucolíticas (ej., hexoquinasa, fosfofructoquinasa-1), desviando el metabolismo hacia la glucólisis anaeróbica.
-
Transporte de Hierro: HIF regula genes implicados en la homeostasis del hierro, un componente esencial para el transporte de oxígeno.
-
Proliferación y Supervivencia Celular: HIF puede activar genes que promueven la supervivencia celular bajo estrés, así como aquellos involucrados en la proliferación celular.
Dato de Biohacking: Optimización de la Respuesta a la Hipoxia
Estudios sugieren que la exposición intermitente a la hipoxia (como el entrenamiento en altitud o cámaras hipóxicas) puede activar el sistema HIF, mejorando la eficiencia mitocondrial, la resistencia y la capacidad de transporte de oxígeno. Ciertos compuestos naturales, como los flavonoides presentes en frutas y verduras, o el ácido alfa-lipoico, se investigan por su potencial para modular sutilmente la actividad de las PHDs, influyendo en la estabilización de HIF y ofreciendo vías para optimizar la respuesta adaptativa celular en contextos de salud y rendimiento.
Beneficios y Roles Fisiológicos de HIF
La importancia fisiológica de HIF es inmensa, abarcando desde el desarrollo embrionario hasta la adaptación del adulto a condiciones extremas.
Angiogénesis y Flujo Sanguíneo
La formación de nuevos vasos sanguíneos, o angiogénesis, es una respuesta crucial a la hipoxia. HIF es el principal inductor de este proceso, principalmente a través de la activación de VEGF. En tejidos isquémicos (con flujo sanguíneo reducido), como en el corazón después de un infarto, la activación de HIF intenta restaurar el suministro de oxígeno y nutrientes mediante la creación de una nueva red vascular. Este mecanismo es vital para la curación de heridas y la regeneración tisular.
Eritropoyesis
La capacidad de la sangre para transportar oxígeno depende en gran medida del número de glóbulos rojos y su contenido de hemoglobina. HIF juega un papel central en la eritropoyesis al estimular la producción de EPO en los riñones y el hígado. La EPO, a su vez, actúa sobre la médula ósea para aumentar la producción de glóbulos rojos. Este es el mecanismo detrás de la adaptación a la altitud, donde la menor presión parcial de oxígeno induce un aumento en los niveles de EPO y, consecuentemente, en la masa de glóbulos rojos.
Adaptación Metabólica
Como se mencionó, HIF es un maestro en la reprogramación metabólica. Al promover la glucólisis anaeróbica y suprimir la fosforilación oxidativa, permite que las células generen ATP en entornos con bajo oxígeno. Además, HIF también puede influir en el metabolismo de los lípidos y los aminoácidos, asegurando que la célula tenga acceso a fuentes de energía alternativas y precursores biosintéticos bajo estrés. Este cambio es particularmente relevante en el desarrollo de órganos, donde las regiones hipóxicas son comunes y requieren un metabolismo adaptado.
Reparación Tisular y Cicatrización
La hipoxia es una característica común en las heridas y en los sitios de daño tisular. HIF contribuye a la reparación tisular al promover la angiogénesis, la migración de células inmunes y la producción de factores de crecimiento que facilitan la regeneración. En la cicatrización de heridas, la activación de HIF es esencial para la formación de tejido de granulación y la posterior reepitelialización, demostrando su papel protector y reparador.
Papel en el Ejercicio y la Altitud
Para los atletas y las personas que viven en altitudes elevadas, HIF es un aliado clave. El entrenamiento en altitud, que somete al cuerpo a hipoxia leve, activa HIF, lo que lleva a un aumento en la producción de EPO, más glóbulos rojos y una mejora en la capacidad aeróbica. Además, HIF optimiza la función mitocondrial y la eficiencia del uso de oxígeno, lo que se traduce en una mayor resistencia y un mejor rendimiento físico. Es un mecanismo de adaptación natural que el cuerpo utiliza para maximizar el suministro y la utilización de oxígeno bajo demanda.
HIF en la Salud y la Enfermedad
Aunque HIF es un protector esencial en muchas circunstancias, su desregulación puede ser un factor clave en la patogénesis de numerosas enfermedades.
Cáncer
El cáncer es quizás el campo donde la dualidad de HIF es más evidente. Los tumores a menudo crecen rápidamente, superando el suministro de oxígeno de los vasos sanguíneos existentes, lo que crea un microambiente hipóxico. En este entorno, la activación sostenida de HIF es fundamental para la supervivencia y progresión del tumor. HIF promueve la angiogénesis tumoral (formación de vasos sanguíneos que alimentan el tumor), el cambio metabólico hacia la glucólisis (efecto Warburg) para sustentar el rápido crecimiento, y la metástasis al inducir factores que facilitan la invasión y la migración celular. Por estas razones, HIF es una diana terapéutica muy atractiva en la investigación oncológica, con fármacos que buscan inhibir su actividad para frenar el crecimiento tumoral.
Enfermedades Cardiovasculares
En condiciones como el infarto de miocardio o el accidente cerebrovascular, donde el flujo sanguíneo se interrumpe y los tejidos sufren de isquemia e hipoxia, HIF juega un papel complejo. Inicialmente, la activación de HIF es protectora, promoviendo la angiogénesis para restaurar el flujo sanguíneo y cambiando el metabolismo para mantener la viabilidad celular. Sin embargo, la activación prolongada o excesiva de HIF puede contribuir al daño por reperfusión y otros efectos deletéreos. El equilibrio entre los efectos protectores y perjudiciales de HIF en estas enfermedades es un área activa de investigación.
Enfermedades Renales
Enfermedades como la enfermedad renal crónica y la anemia asociada a esta, están intrínsecamente ligadas a la disfunción de HIF. Los riñones son el principal sitio de producción de EPO, y la hipoxia renal crónica puede alterar esta producción. Los activadores de HIF, que estabilizan HIF-α, están siendo desarrollados como tratamientos para la anemia renal, ofreciendo una alternativa a la administración exógena de EPO.
Inflamación y Enfermedades Autoinmunes
HIF también está involucrado en la regulación de la respuesta inflamatoria. Las células inmunes, como los macrófagos, activan HIF en condiciones hipóxicas encontradas en sitios de inflamación o infección. Esta activación modula la producción de citoquinas y la función inmune, lo que sugiere un papel en enfermedades autoinmunes y en la resolución de la inflamación. Su papel es complejo, pudiendo ser tanto pro-inflamatorio como anti-inflamatorio dependiendo del contexto.
Mitos y Realidades del HIF
Alerta Médica: La Doble Cara de la Activación de HIF
Existe la percepción errónea de que activar HIF es siempre beneficioso para la salud, dada su asociación con la adaptación y el rendimiento. Sin embargo, la activación sostenida o descontrolada de HIF, como ocurre en el microambiente tumoral, es un motor clave para el crecimiento del cáncer, la metástasis y la angiogénesis patológica. Intervenir en el sistema HIF sin una comprensión profunda de su contexto fisiológico y las posibles consecuencias a largo plazo puede tener efectos perjudiciales, transformando un mecanismo de supervivencia en una vía de enfermedad.
¿Es HIF Siempre Beneficioso?
Uno de los mitos más persistentes es que la activación de HIF es inherentemente buena. Si bien es cierto que HIF es un componente vital para la supervivencia y la adaptación en situaciones de hipoxia aguda y fisiológica (como el ejercicio o la vida en altitud), su activación crónica o desregulada es un sello distintivo de muchas patologías. En el cáncer, por ejemplo, HIF es un promotor clave del crecimiento tumoral, la resistencia a la terapia y la metástasis. También se ha implicado en la fibrosis y la progresión de enfermedades inflamatorias crónicas. La clave, como en muchos sistemas biológicos, reside en el equilibrio y la temporalidad de su activación.
Manipulación de HIF: ¿Una Solución Universal?
La promesa de manipular HIF para tratar enfermedades es enorme, pero también conlleva riesgos. Los activadores farmacológicos de HIF, como los inhibidores de PHD, son prometedores para el tratamiento de la anemia renal. Sin embargo, la activación sistémica y prolongada de HIF podría tener efectos secundarios indeseados, como el aumento del riesgo de tumores, la promoción de la angiogénesis no deseada o cambios metabólicos adversos. La investigación se centra ahora en desarrollar terapias que puedan modular HIF de manera específica para el tejido o la enfermedad, minimizando los efectos fuera de objetivo y aprovechando sus beneficios sin incurrir en sus riesgos.
La complejidad de HIF subraya que la biología es raramente una cuestión de blanco o negro. Comprender los matices de su regulación y sus interacciones con otras vías celulares es esencial para diseñar estrategias terapéuticas seguras y efectivas que aprovechen el poder de este maestro regulador sin desencadenar sus facetas más oscuras.
Conclusión: El Maestro de la Adaptación Celular
El Factor Inducible por Hipoxia (HIF) es mucho más que una simple proteína; es un centinela molecular, un estratega evolutivo y un pilar fundamental de la homeostasis celular. Su capacidad para orquestar una respuesta adaptativa integral a la escasez de oxígeno subraya la sofisticación de los sistemas biológicos. Desde la reprogramación metabólica que permite a una célula sobrevivir sin oxígeno, hasta la inducción de nuevos vasos sanguíneos para restaurar el flujo vital, HIF es un testimonio de la increíble resiliencia de la vida.
La investigación sobre HIF no solo ha profundizado nuestra comprensión de la fisiología básica y la adaptación del organismo, sino que también ha abierto puertas a nuevas intervenciones terapéuticas para una miríada de enfermedades, desde la anemia y las enfermedades cardiovasculares hasta el cáncer. Sin embargo, su poder implica una responsabilidad; la manipulación de HIF debe ser abordada con precisión y cautela, reconociendo su doble naturaleza como protector y promotor de la enfermedad. En última instancia, HIF nos recuerda que en el delicado equilibrio de la vida, la capacidad de adaptarse es la clave de la supervivencia.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.