¿Qué es el complejo de glicoproteínas asociado a distrofina (DAGC)? – Análisis Completo y Beneficios
Resumen Clínico Rápido
🔬 Clasificación
Complejo multiproteico transmembrana
⚙️ Función
Estabilidad estructural y transducción de señales en el sarcolema
📋 Impacto
Defectos causan distrofias musculares (DMD, LGMD)
En el vasto y fascinante universo de la biología molecular, la integridad y función de cada célula, especialmente aquellas con roles mecánicos críticos como las fibras musculares, dependen de una intrincada red de proteínas. Entre estas estructuras fundamentales, el Complejo de Glicoproteínas Asociado a Distrofina (DAGC) emerge como un pilar esencial, actuando como el puente vital entre el citoesqueleto intracelular de una célula muscular y la matriz extracelular que la rodea. Su descubrimiento y la comprensión de su papel han revolucionado nuestra visión de las enfermedades neuromusculares, particularmente las distrofias musculares.
Este complejo molecular no es meramente un andamiaje; es una máquina molecular multifuncional que integra señales mecánicas y bioquímicas, crucial para la estabilidad estructural del sarcolema —la membrana plasmática de la célula muscular— y para la transducción de señales que regulan el desarrollo, la función y la reparación muscular. Cuando este complejo falla, las consecuencias son devastadoras, conduciendo a la degeneración progresiva del tejido muscular que caracteriza a enfermedades como la distrofia muscular de Duchenne (DMD) y Becker (BMD), así como a otras miopatías menos comunes. Comprender el DAGC es adentrarse en la esencia de la fisiología muscular y la patogénesis de algunas de las enfermedades genéticas más desafiantes para la medicina moderna.
Resumen Clínico
- El DAGC es un complejo multiproteico crucial para la estabilidad y función de las fibras musculares esqueléticas y cardíacas.
- Actúa como un enlace mecánico entre el citoesqueleto de actina y la matriz extracelular, protegiendo al sarcolema del estrés mecánico durante la contracción muscular.
- Defectos en cualquiera de sus componentes pueden causar diversas formas de distrofias musculares, con la distrofina siendo la proteína clave en la distrofia muscular de Duchenne.
El Propósito Evolutivo del DAGC: Anclaje y Protección
Desde una perspectiva evolutiva, la aparición de sistemas contráctiles altamente especializados en organismos multicelulares requirió mecanismos robustos para salvaguardar la integridad celular ante las fuerzas generadas. El propósito evolutivo del DAGC es precisamente ese: proporcionar un sistema de anclaje mecánico y señalización que blinde la célula muscular contra el daño inducido por el estrés contráctil repetitivo. Imaginen una cuerda que une el interior de una tienda de campaña a sus estacas exteriores, permitiéndole resistir vientos fuertes; el DAGC cumple una función análoga, anclando el andamiaje interno de la célula muscular (el citoesqueleto) a su entorno externo (la matriz extracelular).
Esta función es vital para la supervivencia y el rendimiento de los músculos. Sin un DAGC funcional, cada contracción muscular, cada movimiento, se convierte en un evento potencialmente destructivo para el sarcolema. La capacidad de los vertebrados para realizar movimientos vigorosos y sostenidos, desde la carrera hasta el bombeo cardíaco constante, depende íntimamente de la robustez que este complejo confiere a sus fibras musculares. Su evolución subraya la presión selectiva para desarrollar sistemas que minimicen el daño tisular y mantengan la homeostasis celular bajo condiciones de alto estrés mecánico.
Fisiología Molecular: Los Componentes del Complejo y su Orquestación
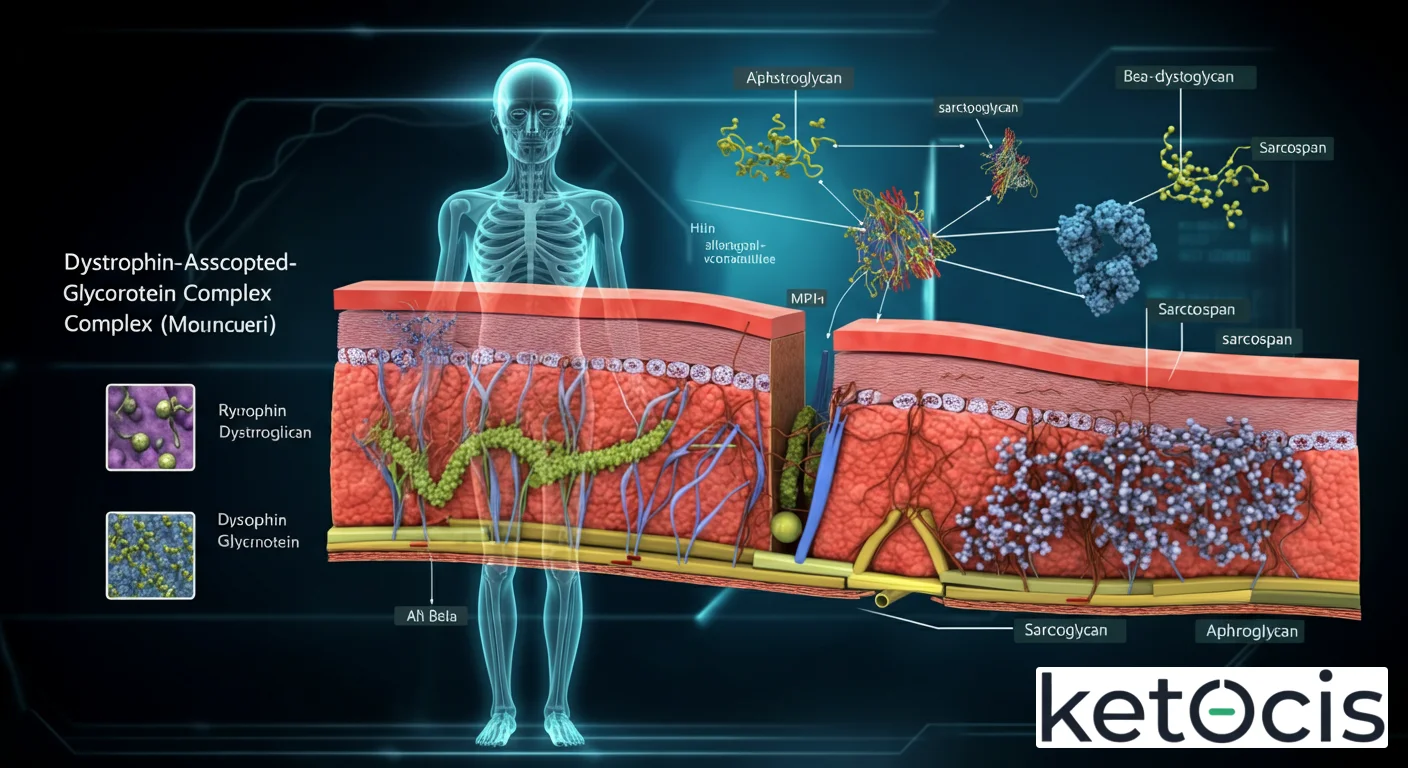
El DAGC es una obra maestra de la ingeniería molecular, compuesto por una serie de proteínas interconectadas que se extienden desde el citoplasma hasta el espacio extracelular. Su arquitectura es jerárquica y modular, con cada componente desempeñando un rol específico pero coordinado. Los principales componentes pueden agruparse en subcomplejos:
1. La Distrofina: El Ancla Citoesquelética
La distrofina es la proteína central y más grande del DAGC, un gigante de 427 kDa codificado por uno de los genes más grandes conocidos en el genoma humano. Se localiza en la cara citoplasmática del sarcolema, donde se une directamente a los filamentos de actina del citoesqueleto a través de su dominio N-terminal. Su dominio central, rico en repeticiones de espectrina, proporciona una estructura flexible y elástica, mientras que su dominio C-terminal se une al resto del DAGC. La ausencia o disfunción de la distrofina, como ocurre en la distrofia muscular de Duchenne, es catastrófica para la fibra muscular, comprometiendo la integridad del complejo y la estabilidad del sarcolema.
2. El Subcomplejo de Distroglicanos: El Enlace Transmembrana
Este subcomplejo está formado por dos proteínas derivadas de un único precursor genético: alfa-distroglicano (α-DG) y beta-distroglicano (β-DG). El α-DG es una glicoproteína periférica extracelular que se une a componentes de la matriz extracelular como la laminina-2 (merosin). El β-DG es una proteína transmembrana que atraviesa el sarcolema y se une directamente a la distrofina en el lado citoplasmático y a α-DG en el lado extracelular. Esta unión α-DG/β-DG es crucial para establecer la conexión entre el citoesqueleto y la matriz extracelular. La glicosilación adecuada de α-DG es esencial para su función, y defectos en este proceso pueden llevar a distrofias musculares congénitas.
3. El Subcomplejo de Sarcoglicanos: Estabilidad Adicional
El subcomplejo de sarcoglicanos consta de cuatro proteínas transmembrana: alfa-, beta-, gamma- y delta-sarcoglicano (α-, β-, γ-, δ-SG). Estas proteínas interactúan entre sí para formar un complejo estable dentro de la membrana plasmática, uniéndose al β-distroglicano. Su función principal es proporcionar estabilidad adicional al sarcolema y participar en la transducción de señales. Las mutaciones en cualquiera de los genes que codifican los sarcoglicanos son responsables de las sarcoglicanopatías, un grupo de distrofias musculares de las cinturas (LGMD) clínicamente similares a la DMD.
4. Otras Proteínas Asociadas: Moduladores y Señalizadores
Además de los componentes principales, el DAGC incluye otras proteínas importantes como las sintrofinas, que se unen a la distrofina y a otras proteínas de señalización como la óxido nítrico sintasa neuronal (nNOS), modulando la señalización intracelular. Las distrobrevinas, proteínas relacionadas con la distrofina, también se asocian al complejo. La sarcospan es otra proteína transmembrana que se asocia con los sarcoglicanos y puede modular su estabilidad y función. Estas proteínas accesorias resaltan la naturaleza multifuncional del DAGC, que no solo es un ancla estructural sino también una plataforma de señalización.
Beneficios de un DAGC Funcional: Más Allá de la Estabilidad Mecánica
Un DAGC intacto y funcional ofrece beneficios que van más allá de la mera estabilidad mecánica:
- Protección contra el Daño por Estrés: Es el amortiguador principal que absorbe y distribuye las fuerzas generadas durante la contracción y relajación muscular, previniendo microdesgarros y la lisis celular.
- Integridad de la Membrana Plasmática: Mantiene la barrera del sarcolema, crucial para regular el flujo de iones y moléculas y evitar la entrada de sustancias nocivas.
- Transducción de Señales: Funciona como un centro de señalización, conectando el exterior celular con el interior. Por ejemplo, la unión de nNOS al DAGC permite la producción de óxido nítrico, un vasodilatador que mejora el flujo sanguíneo durante el ejercicio, y un modulador de la función contráctil.
- Regulación de la Homeostasis del Calcio: Indirectamente, un DAGC intacto ayuda a mantener la homeostasis del calcio intracelular, cuya desregulación es un evento clave en la patogénesis de las distrofias musculares.
- Reparación y Regeneración Muscular: Un sarcolema estable es fundamental para la activación adecuada de las células satélite y los procesos de reparación muscular después del daño.
Biohacking del Músculo: La Conexión Entre Estrés Mecánico y Señalización Celular
¿Sabías que la tensión mecánica ejercida sobre tus músculos durante el ejercicio no solo los fortalece, sino que activa directamente vías de señalización que promueven la reparación y el crecimiento? El DAGC es un sensor clave en este proceso. Cuando los músculos se contraen y estiran, el DAGC transmite estas fuerzas al interior de la célula, desencadenando cascadas bioquímicas que incluyen la activación de mTOR, crucial para la síntesis de proteínas. Optimizar la intensidad y el tipo de ejercicio puede potenciar estas señales, fomentando una mejor adaptación muscular y, potencialmente, una mayor resistencia al daño, incluso en ausencia de patología.
La Patología del DAGC: Las Distrofias Musculares
La disfunción del DAGC es el sello distintivo de un grupo de enfermedades genéticas progresivas conocidas como distrofias musculares. Cada componente del complejo puede ser el sitio de una mutación, llevando a una forma específica de distrofia:
- Distrofia Muscular de Duchenne (DMD) y Becker (BMD): Causadas por mutaciones en el gen DMD, que codifica la distrofina. La DMD es la forma más severa, con ausencia casi completa de distrofina, resultando en degeneración muscular severa, debilidad progresiva y muerte prematura. La BMD es una forma más leve, con distrofina truncada o reducida pero parcialmente funcional.
- Distrofias Musculares de las Cinturas (LGMD): Un grupo heterogéneo de distrofias que afectan predominantemente los músculos de los hombros y la pelvis. Muchas formas de LGMD son causadas por mutaciones en los genes que codifican los sarcoglicanos (sarcoglicanopatías), llevando a la inestabilidad del subcomplejo de sarcoglicanos y, secundariamente, a la disfunción del DAGC.
- Distrofias Musculares Congénitas (CMD): Algunas formas, como las causadas por defectos en la glicosilación del alfa-distroglicano (distroglicanopatías), resultan en una conexión deficiente entre la célula muscular y la matriz extracelular, con afectación muscular severa y, a menudo, implicación cerebral.
En todas estas condiciones, la falla del DAGC conduce a una cascada de eventos patológicos: el sarcolema se vuelve frágil y susceptible a la ruptura, lo que permite la entrada de calcio extracelular en la célula. Este influjo de calcio desregulado activa proteasas y otras enzimas degradativas, lo que conduce a la necrosis de las fibras musculares. Con el tiempo, la capacidad de regeneración muscular se agota, y el tejido muscular es reemplazado por tejido conectivo y adiposo, un proceso conocido como fibrosis y pseudohipertrofia.
Investigación y Terapias Emergentes
La comprensión detallada del DAGC ha abierto vías emocionantes para el desarrollo de terapias. En la DMD, por ejemplo, las estrategias incluyen:
- Terapia de Exón Skipping: Utiliza oligonucleótidos antisentido para omitir exones mutados en el ARN mensajero, permitiendo la producción de una proteína distrofina más corta pero funcional, similar a la que se encuentra en la BMD.
- Terapia Génica: Consiste en introducir una copia funcional del gen DMD en las células musculares, a menudo utilizando vectores virales como los virus adenoasociados (AAVs). El desafío es el gran tamaño del gen DMD, lo que ha llevado al desarrollo de microdistrofinas más pequeñas.
- Edición Genómica (CRISPR/Cas9): Busca corregir la mutación directamente en el ADN del paciente, ofreciendo la posibilidad de una cura más permanente.
- Terapias Farmacológicas: Se dirigen a reducir la inflamación, la fibrosis o mejorar la regeneración muscular, como los corticosteroides o moduladores de la vía TGF-β.
Para las sarcoglicanopatías y distroglicanopatías, las estrategias también se centran en la terapia génica y en enfoques que restauran la función de las proteínas afectadas o mitigan las consecuencias de su disfunción.
ALERTA MÉDICA: No Subestimes la Fatiga Crónica y la Debilidad Muscular
Es crucial no ignorar la fatiga muscular persistente, la debilidad progresiva o la dificultad para realizar tareas cotidianas que antes eran fáciles. Aunque muchas causas son benignas, estos síntomas pueden ser indicadores tempranos de enfermedades neuromusculares graves, incluidas las distrofias asociadas al DAGC. La automedicación o la dependencia de suplementos no probados pueden retrasar un diagnóstico vital y la intervención médica adecuada. Siempre consulta a un profesional de la salud ante cualquier cambio significativo en tu fuerza o resistencia muscular. Un diagnóstico temprano es fundamental para el manejo y la planificación terapéutica.
Mitos y Realidades del DAGC y la Salud Muscular
Existe un mito persistente de que la simple ingesta de proteínas o suplementos ‘constructores de músculo’ puede compensar o incluso prevenir las distrofias musculares. La realidad es que, si bien una nutrición adecuada es vital para la salud muscular general, las distrofias musculares son enfermedades genéticas causadas por defectos específicos en proteínas clave como las del DAGC. Ningún suplemento dietético puede corregir una mutación genética o restaurar una proteína ausente o disfuncional.
El Futuro del DAGC en la Medicina
El estudio del DAGC sigue siendo un campo vibrante de investigación. Los avances en tecnologías de imagen, genómica y proteómica están permitiendo una comprensión aún más profunda de su estructura, sus interacciones dinámicas y su papel en diversas enfermedades. La identificación de nuevos componentes asociados al DAGC o la elucidación de vías de señalización previamente desconocidas podría revelar nuevos objetivos terapéuticos. Además, la exploración de cómo el DAGC interactúa con otros complejos moleculares y su papel en tejidos no musculares, como el cerebro o el corazón, está ampliando nuestro conocimiento y ofreciendo nuevas perspectivas sobre la complejidad de la fisiología humana.
En resumen, el Complejo de Glicoproteínas Asociado a Distrofina no es solo un componente de la célula muscular; es un guardián de su integridad, un sensor de su entorno y un integrador de señales vitales. Su estudio nos recuerda la asombrosa complejidad de la vida a nivel molecular y la promesa de la ciencia para desentrañar los misterios de las enfermedades más desafiantes.
La distrofia muscular se puede curar con una dieta rica en proteínas o suplementos milagrosos.
Las distrofias musculares son enfermedades genéticas causadas por mutaciones en genes que codifican proteínas estructurales o funcionales clave, como las del DAGC. Ningún suplemento dietético puede corregir estas mutaciones o restaurar la función proteica perdida. Las terapias actuales se centran en enfoques genéticos y farmacológicos para mitigar los síntomas o corregir el defecto subyacente.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.