ARN Interferente: Silenciamiento Génico y Terapia Revolucionaria
Resumen Clínico Rápido
🔬 Clasificación
ARN no codificante
⚙️ Función
Regulación génica post-transcripcional
📋 Impacto
Herramienta de investigación y potencial terapéutico
En el vasto y complejo universo de la biología molecular, donde la información genética fluye desde el ADN hasta las proteínas que construyen y operan nuestros cuerpos, existe un mecanismo de control sofisticado y de una elegancia asombrosa: el ARN interferente. Este proceso biológico, presente en prácticamente todos los eucariotas, representa una de las formas más fundamentales y potentes de regulación génica. No se trata simplemente de una curiosidad académica, sino de una maquinaria molecular que defiende la integridad del genoma, orquesta el desarrollo y, cada vez más, se perfila como una herramienta terapéutica de vanguardia con el potencial de transformar la medicina moderna.
Desde su descubrimiento, que valió un Premio Nobel, el concepto de ARN interferente (ARNi) ha redefinido nuestra comprensión de cómo los genes son silenciados o activados. Lejos de ser un mero intermediario en la síntesis de proteínas, ciertas moléculas de ARN no codificante poseen la capacidad intrínseca de identificar y neutralizar mensajes genéticos específicos, impidiendo que se traduzcan en proteínas. Este silenciamiento génico post-transcripcional es crucial para mantener la homeostasis celular, protegerse contra invasores virales y regular la expresión génica durante el desarrollo y la diferenciación. Adentrarse en el estudio del ARNi es explorar una dimensión oculta de la biología, donde pequeñas moléculas ejercen un control monumental sobre el destino de la célula y, por extensión, del organismo.
Resumen Clínico
- Punto clave 1: El ARN interferente (ARNi) es un mecanismo biológico de silenciamiento génico post-transcripcional, crucial para la regulación de la expresión genética y la defensa celular.
- Punto clave 2: Involucra ARN de doble cadena (ARNd) pequeños, como los microARN (miRNA) y los ARN de interferencia pequeños (siRNA), que guían complejos proteicos para degradar o inhibir la traducción de ARNm específicos.
- Punto clave 3: Su capacidad para silenciar genes con alta especificidad lo convierte en una poderosa herramienta de investigación y una prometedora plataforma para el desarrollo de nuevas terapias génicas contra enfermedades como el cáncer, infecciones virales y trastornos genéticos.
El ARN interferente es una técnica de edición genética que altera permanentemente el ADN.
Falso. El ARNi actúa a nivel post-transcripcional, silenciando temporalmente la expresión de genes al degradar ARNm específicos o inhibir su traducción, sin modificar la secuencia de ADN.
El Propósito Evolutivo del ARN Interferente: Un Guardián del Genoma
La existencia del ARN interferente no es un capricho de la evolución, sino una estrategia vital forjada a lo largo de miles de millones de años para proteger y regular la vida. Su propósito evolutivo principal se manifiesta en dos roles fundamentales: la defensa antiviral y la regulación de la expresión génica endógena. En esencia, el ARNi actúa como un sistema inmune molecular innato a nivel genético.
Desde una perspectiva defensiva, el ARNi se desarrolló como una barrera formidable contra elementos genéticos invasores. Los virus, en particular aquellos con genomas de ARN o que replican a través de intermediarios de ARN de doble cadena (ARNd), son objetivos primarios. Cuando un virus infecta una célula, a menudo produce ARNd como parte de su ciclo de replicación. El sistema ARNi de la célula huésped reconoce este ARNd foráneo como una señal de peligro y lo procesa para activar una respuesta de silenciamiento, degradando el ARNm viral y deteniendo la infección. Este mecanismo no solo protege contra virus, sino también contra los elementos transponibles, secuencias de ADN móviles que pueden insertarse aleatoriamente en el genoma y causar mutaciones dañinas. Al silenciar la expresión de estos ‘genes saltarines’, el ARNi ayuda a mantener la estabilidad e integridad del genoma.
Paralelamente a su función defensiva, el ARNi desempeña un papel indispensable en la regulación de la expresión de los propios genes de un organismo. Los microARN (miRNA), una clase clave de moléculas de ARNi, son transcritos a partir de regiones específicas del genoma y actúan como reguladores maestros. Están implicados en casi todos los procesos biológicos conocidos: desde el desarrollo embrionario y la diferenciación celular hasta el metabolismo, la respuesta inmune y la homeostasis tisular. Un único miRNA puede regular cientos de ARNm diferentes, y la expresión de muchos genes está bajo el control de múltiples miRNA. Esta intrincada red de regulación permite a las células responder dinámicamente a los cambios ambientales y mantener su identidad y función específicas. La interrupción de este delicado equilibrio puede conducir a una amplia gama de patologías, subrayando la importancia crítica del ARNi para la salud.
La Fisiología Molecular del Silenciamiento Génico: Una Maquinaria de Precisión
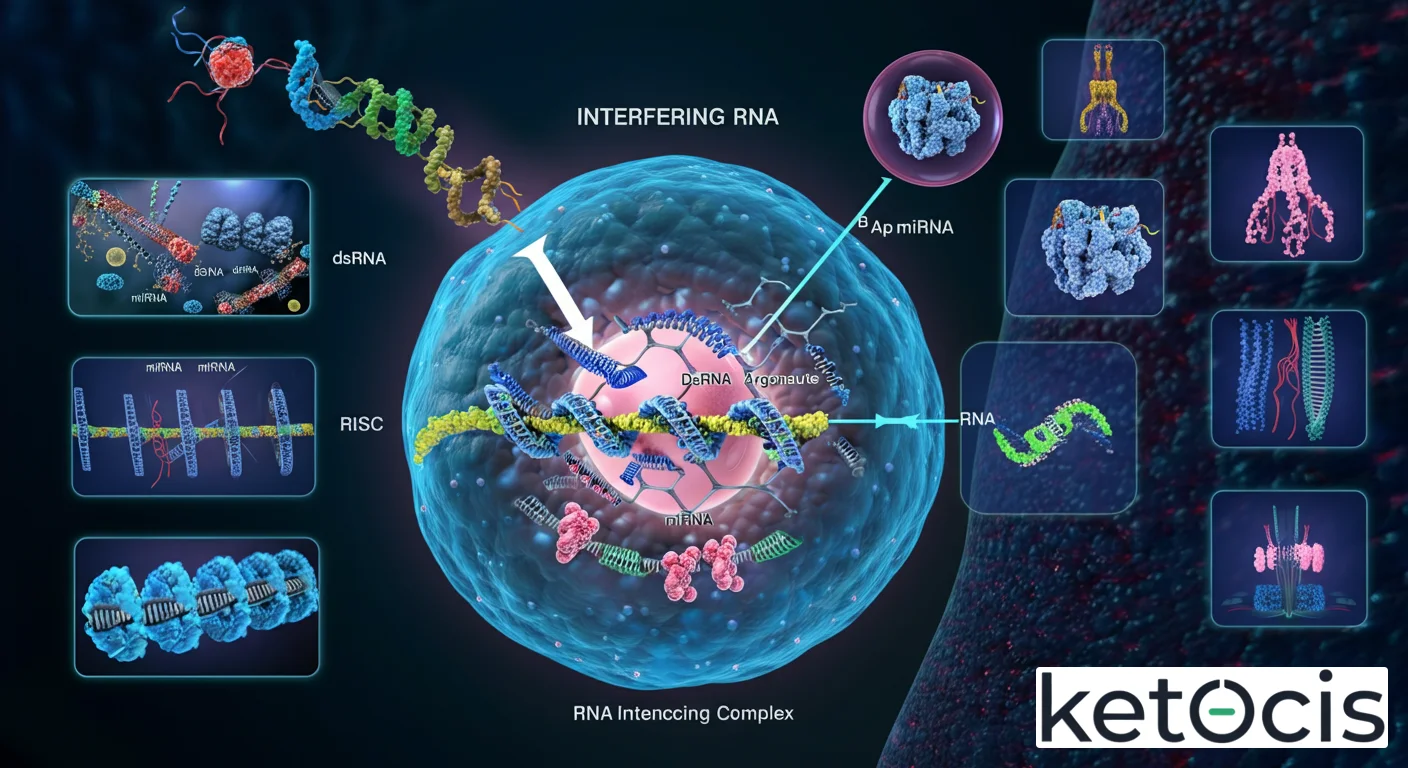
El mecanismo del ARN interferente es una danza molecular intrincada que involucra varias proteínas y tipos de ARN no codificante. Aunque existen diferentes vías (siRNA, miRNA, piRNA), el principio subyacente es el reconocimiento de ARN de doble cadena y su uso como guía para silenciar ARNm específicos. Nos centraremos en los mecanismos de siRNA (ARN de interferencia pequeño) y miRNA, que son los más estudiados y terapéuticamente relevantes.
ARN de Interferencia Pequeño (siRNA)
La vía del siRNA es típicamente desencadenada por ARNd exógeno (como el de virus) o por ARNd endógeno largo. Una enzima clave, la Dicer, una RNasa III, juega un papel central. Dicer procesa estos ARNd largos en fragmentos más pequeños, de aproximadamente 21-23 nucleótidos de longitud, conocidos como siRNA. Estos siRNA tienen extremos sobresalientes de dos nucleótidos en el 3′ y grupos fosfato en el 5′.
Una vez generados, los siRNA se asocian con un complejo multiproteico llamado Complejo de Silenciamiento Inducido por ARN (RISC, por sus siglas en inglés). En este complejo, una de las dos hebras del siRNA (la hebra guía) se retiene, mientras que la otra (la hebra pasajera) se degrada. La hebra guía dirige el complejo RISC hacia un ARNm diana que posee una secuencia complementaria. La proteína central del RISC es la familia de proteínas Argonaute, que contiene la actividad catalítica para escindir el ARNm diana. Una vez que el RISC, guiado por el siRNA, encuentra su ARNm complementario, Argonaute lo corta, lo que lleva a la rápida degradación del ARNm y, consecuentemente, a la interrupción de la síntesis de la proteína correspondiente.
MicroARN (miRNA)
La vía del miRNA es similar pero comienza de manera diferente y tiene matices importantes en su mecanismo de acción. Los miRNA se transcriben inicialmente como moléculas de ARN largas, conocidas como pri-miRNA, a menudo con estructuras de horquilla. Estas pri-miRNA son procesadas en el núcleo por un complejo proteico que incluye la RNasa III nuclear Drosha y su cofactor Pasha (DGCR8). Este procesamiento genera precursores de miRNA de aproximadamente 70 nucleótidos, conocidos como pre-miRNA, que aún conservan la estructura de horquilla.
Los pre-miRNA son exportados del núcleo al citoplasma por el transportador Exportina-5. Una vez en el citoplasma, la enzima Dicer vuelve a entrar en acción, procesando los pre-miRNA en miRNA maduros de doble cadena, de aproximadamente 21-23 nucleótidos, similares a los siRNA. Al igual que los siRNA, estos miRNA maduros se cargan en el complejo RISC. Sin embargo, a diferencia de los siRNA que suelen tener una complementariedad perfecta con su ARNm diana, los miRNA a menudo forman apareamientos imperfectos, típicamente en la región 3′ no traducida (3′ UTR) del ARNm. Esta complementariedad imperfecta no suele conducir a la escisión directa del ARNm, sino que resulta en la inhibición de la traducción de la proteína o en la desadenilación y posterior degradación del ARNm. Esta sutil diferencia permite que un solo miRNA regule múltiples ARNm, lo que lo convierte en un regulador génico más pleiotrópico.
Dato de Biohacking: Potenciando la Regulación Epigenética con Nutrientes
La expresión de los microARN (miRNA) puede ser influenciada por factores dietéticos. Por ejemplo, se ha demostrado que ciertos compuestos bioactivos presentes en alimentos como el sulforafano (en brócoli) o el resveratrol (en uvas) pueden modular la expresión de miRNA específicos que, a su vez, regulan vías metabólicas clave o la respuesta al estrés. Optimizar la ingesta de estos fitonutrientes podría, teóricamente, ‘biohackear’ tu maquinaria de ARNi, afinando la expresión génica para una mejor salud celular y metabólica.
Beneficios y Aplicaciones Terapéuticas del ARN Interferente
La comprensión detallada del ARN interferente ha abierto puertas a una plétora de aplicaciones, tanto en la investigación biomédica como en el desarrollo de terapias innovadoras. Su capacidad para silenciar genes específicos con alta precisión lo convierte en una herramienta invaluable para desentrañar las funciones génicas y para abordar enfermedades a nivel molecular.
Herramienta de Investigación
En el laboratorio, el ARNi se ha convertido en una técnica estándar para el silenciamiento génico. Los investigadores pueden diseñar siRNA o miRNA sintéticos que se dirijan específicamente a cualquier ARNm de interés. Al introducir estas moléculas en células o modelos animales, pueden silenciar la expresión de un gen particular y observar las consecuencias fenotípicas. Esto permite determinar la función de genes desconocidos, validar dianas farmacológicas y estudiar vías biológicas complejas. La capacidad de ‘apagar’ genes de forma selectiva ha revolucionado la genómica funcional y el descubrimiento de fármacos.
Potencial Terapéutico
El verdadero impacto del ARNi reside en su promesa como una nueva clase de medicamentos. La idea es simple pero poderosa: si una enfermedad es causada por la expresión excesiva o inapropiada de un gen (por ejemplo, un oncogén en el cáncer o un gen viral en una infección), el ARNi puede diseñarse para silenciar ese gen y revertir la patología. Las áreas de aplicación son vastas:
- Cáncer: Muchos tipos de cáncer se caracterizan por la sobreexpresión de oncogenes o la subexpresión de genes supresores de tumores. Los ARNi pueden diseñarse para silenciar oncogenes clave o para modular la expresión de miRNA que promueven el crecimiento tumoral o la metástasis.
- Enfermedades Virales: El ARNi es una defensa natural contra los virus. Los siRNA pueden diseñarse para atacar secuencias de ARN viral esenciales, como en el caso del VIH, la Hepatitis B y C, o el virus sincitial respiratorio (VSR).
- Enfermedades Neurodegenerativas: Trastornos como la enfermedad de Huntington o la esclerosis lateral amiotrófica (ELA) son causados por la acumulación de proteínas tóxicas resultantes de mutaciones génicas. El ARNi puede silenciar los genes mutados que producen estas proteínas.
- Trastornos Genéticos Hereditarios: Muchas enfermedades monogénicas (causadas por un solo gen defectuoso) podrían beneficiarse del ARNi. Un ejemplo notable es la amiloidosis por transtiretina (ATTR), donde el ARNi ya ha dado lugar a terapias aprobadas que silencia el gen de la transtiretina mutada, reduciendo la producción de proteínas amiloidogénicas.
- Enfermedades Cardiovasculares y Metabólicas: La modulación de genes implicados en el metabolismo del colesterol, la aterosclerosis o la diabetes es otra área activa de investigación.
A pesar de su inmenso potencial, la aplicación terapéutica del ARNi enfrenta desafíos significativos, principalmente relacionados con la entrega in vivo de las moléculas de ARN a las células diana. El ARN es una molécula lábil y es fácilmente degradado por las nucleasas en el cuerpo. Además, su carga negativa dificulta su entrada a través de las membranas celulares. Las estrategias para superar estos obstáculos incluyen el uso de nanopartículas lipídicas, conjugados de N-acetilgalactosamina (GalNAc) para la entrega hepática, y modificaciones químicas para aumentar la estabilidad y reducir los efectos fuera de objetivo.
Alerta Médica: El Riesgo de los Efectos Fuera de Objetivo
Aunque el ARN interferente es notablemente específico, existe un riesgo inherente de ‘efectos fuera de objetivo’ (off-target effects). Esto ocurre cuando un siRNA o miRNA diseñado para silenciar un gen específico se une y silencia inadvertidamente otros ARNm con secuencias parcialmente complementarias. Esto puede llevar a efectos secundarios no deseados o toxicidad inesperada en un contexto terapéutico. La investigación actual se centra en el diseño de moléculas de ARNi más selectivas y en el desarrollo de sistemas de entrega que minimicen la exposición a células no diana para mitigar este riesgo.
Mitos y Realidades del ARN Interferente
Como cualquier tecnología emergente con un alto perfil en la investigación y la medicina, el ARNi no está exento de malentendidos y mitos. Es crucial diferenciar la ciencia de la especulación.
Mito Popular Falso:
“El ARN interferente es una forma de edición genética que modifica permanentemente el ADN de una persona, con riesgos impredecibles a largo plazo.”
Explicación Científica:
Falso. Esta es una confusión común con técnicas como CRISPR-Cas9. El ARNi no es una técnica de edición genética. Su mecanismo de acción es fundamentalmente diferente: opera a nivel post-transcripcional. Esto significa que el ARNi actúa sobre el ARN mensajero (ARNm), la molécula que lleva la información desde el ADN a la maquinaria de síntesis de proteínas, y no directamente sobre el ADN. El ARNi silencia temporalmente la expresión de genes al degradar ARNm específicos o al inhibir su traducción a proteínas, sin modificar la secuencia de ADN del paciente. Por lo tanto, sus efectos son reversibles y no alteran el genoma de forma permanente, lo que en algunos contextos puede ser una ventaja en términos de seguridad, ya que los efectos secundarios indeseados pueden cesar una vez que el tratamiento se interrumpe o se agota.
La distinción entre la edición genética (que altera el ADN) y el silenciamiento génico (que actúa sobre el ARN) es fundamental para comprender la seguridad y el alcance de las terapias basadas en ARNi. Si bien ambas buscan influir en la expresión génica, lo hacen a diferentes niveles y con diferentes implicaciones a largo plazo.
Conclusión: El Futuro Prometedor del Silenciamiento Génico
El ARN interferente representa una de las revoluciones más significativas en la biología molecular de las últimas décadas. Desde su papel como un mecanismo de defensa ancestral hasta su emergencia como una de las plataformas terapéuticas más prometedoras, el ARNi continúa desafiando y expandiendo nuestra comprensión de la vida a nivel molecular. Su capacidad para silenciar genes de manera específica y potente ofrece una vía para abordar enfermedades que antes se consideraban intratables, al permitirnos ‘apagar’ las causas genéticas subyacentes.
Aunque los desafíos en la entrega y la especificidad persisten, la ciencia avanza a pasos agigantados. Con varias terapias basadas en ARNi ya aprobadas y muchas más en ensayos clínicos, estamos presenciando el amanecer de una nueva era en la medicina, donde el conocimiento de estas diminutas moléculas de ARN se traduce en tratamientos que cambian vidas. El ARNi no es solo una parte fascinante de la biología; es una prueba del ingenio de la naturaleza y un faro de esperanza para el futuro de la salud humana.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.