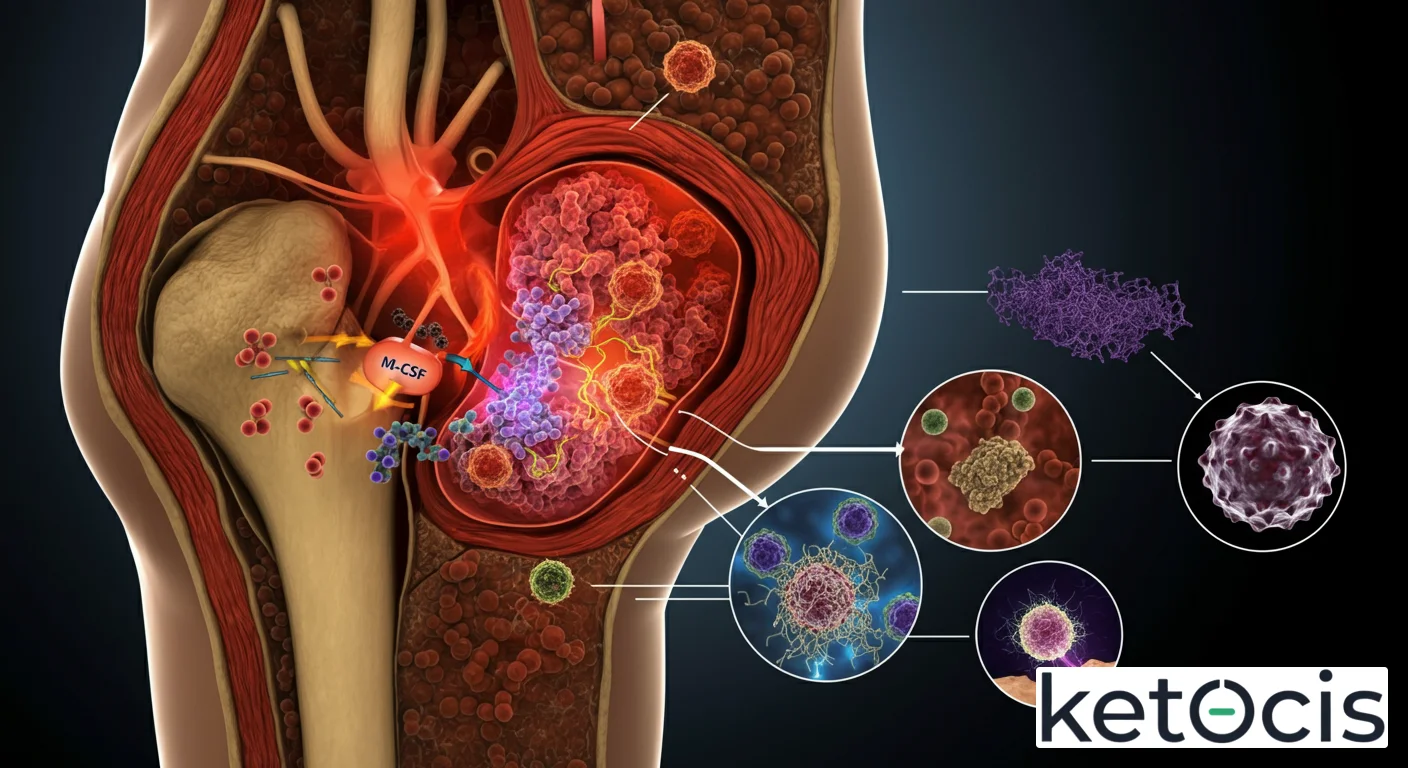
¿Qué es el factor estimulante de colonias de macrófagos (M-CSF)? – Análisis Completo y Beneficios
Resumen Clínico Rápido
🔬 Clasificación
Citocina, Factor de Crecimiento Hematopoyético
⚙️ Función
Proliferación, diferenciación y supervivencia de monocitos/macrófagos
📋 Impacto
Regulación inmune, remodelación ósea, neuroprotección, metabolismo
En el vasto y complejo universo de la biología celular, donde cada molécula juega un papel orquestado en el mantenimiento de la homeostasis y la defensa del organismo, el factor estimulante de colonias de macrófagos (M-CSF, por sus siglas en inglés, Macrophage Colony-Stimulating Factor) emerge como una citocina fundamental. No es meramente un mensajero, sino un director clave en la orquesta del sistema inmune innato, con implicaciones profundas que se extienden mucho más allá de la simple proliferación de células mieloides. Su influencia abarca desde la embriogénesis y la remodelación ósea hasta la neuroprotección y la modulación metabólica, revelando una versatilidad que lo posiciona como un objetivo de estudio y manipulación terapéutica de creciente interés.
Este polipéptido, también conocido como CSF-1, pertenece a una familia de factores de crecimiento hematopoyéticos que dictan el destino de las células progenitoras. Su descubrimiento inicial se centró en su capacidad para estimular la formación de colonias de macrófagos y monocitos in vitro, revelando su papel crucial en la mielopoyesis. Sin embargo, décadas de investigación han desvelado una red de funciones mucho más intrincada, posicionándolo como un regulador maestro de la diferenciación, supervivencia y función de las células del linaje monocítico-macrofágico. Comprender el M-CSF no es solo adentrarse en la inmunología, sino explorar un eje central que conecta la inflamación, la regeneración tisular y, sorprendentemente, las adaptaciones metabólicas que ocurren en estados como la cetosis y el ayuno.
En esta guía enciclopédica, desentrañaremos la naturaleza del M-CSF, desde su origen y estructura molecular hasta su complejo mecanismo de acción y sus diversas funciones fisiológicas. Exploraremos cómo su actividad es finamente regulada y las consecuencias de su desregulación en diversas patologías. Finalmente, nos aventuraremos en las intersecciones entre el M-CSF, el metabolismo y las estrategias de biohacking, proporcionando una perspectiva integral y autoritativa para el Glosario Ketocis, con el rigor científico que demanda la vanguardia de la investigación biomédica.
Resumen Clínico
-
Punto clave 1: M-CSF (CSF-1) es una citocina hematopoyética crucial para la proliferación, diferenciación y supervivencia de monocitos y macrófagos.
-
Punto clave 2: Actúa a través del receptor CSF1R (CD115), desencadenando vías de señalización intracelular vitales para la inmunidad innata y adaptativa.
-
Punto clave 3: Sus funciones se extienden más allá de la inmunidad, influyendo en la remodelación ósea, desarrollo neurológico, reproducción y metabolismo energético.
Origen y Estructura Molecular del M-CSF
El M-CSF es una glicoproteína que se produce como un homodímero, es decir, dos cadenas idénticas unidas. Existen varias isoformas de M-CSF, resultado de un procesamiento alternativo del ARN mensajero del gen CSF1. Estas isoformas pueden ser secretadas, unidas a la membrana o ser un proteoglicano, cada una con implicaciones funcionales distintas en su biodisponibilidad y modo de acción. La forma secretada es la más estudiada y es liberada al torrente sanguíneo y al líquido intersticial, actuando de forma paracrina o endocrina. La forma unida a la membrana permite una señalización yuxtacrina, es decir, entre células adyacentes, lo cual es vital en microambientes tisulares específicos.
La producción de M-CSF es ubicua, con una amplia gama de tipos celulares capaces de sintetizarlo, incluyendo monocitos, macrófagos, fibroblastos, células endoteliales, osteoblastos, células estromales de la médula ósea y células epiteliales. Esta producción generalizada subraya su importancia fundamental en múltiples sistemas orgánicos. La expresión del gen CSF1 está finamente regulada por una variedad de estímulos proinflamatorios y factores de crecimiento, como el factor de necrosis tumoral alfa (TNF-α), la interleucina-1 (IL-1) y el lipopolisacárido (LPS), así como por factores de transcripción como NF-κB y AP-1. Esta regulación permite que los niveles de M-CSF se adapten rápidamente a las necesidades fisiológicas y patológicas del organismo, por ejemplo, aumentando drásticamente durante infecciones o inflamación para movilizar y diferenciar células mieloides.
El M-CSF solo es relevante para el sistema inmune y la defensa contra patógenos.
Falso. Aunque crucial para la inmunidad, el M-CSF tiene funciones vitales en el desarrollo embrionario, remodelación ósea (osteoclastogénesis), neurogénesis y neuroprotección, reproducción y modulación del metabolismo, demostrando una acción pleiotrópica mucho más amplia.
Mecanismo de Acción: La Orquestación Celular del M-CSF
La acción biológica del M-CSF está mediada exclusivamente por su receptor de membrana de alta afinidad, el CSF1R (también conocido como CD115). Este receptor es una tirosina quinasa transmembrana que pertenece a la subfamilia de receptores de tirosina quinasa tipo III, la misma familia que incluye los receptores de PDGF (factor de crecimiento derivado de plaquetas) y Kit. CSF1R se expresa predominantemente en células del linaje monocítico-macrofágico, incluyendo monocitos, macrófagos, osteoclastos y microglía, lo que explica la especificidad de acción del M-CSF.
Cuando el M-CSF se une a su receptor, induce la dimerización del CSF1R y la autofosforilación de residuos de tirosina en el dominio intracelular del receptor. Esta fosforilación crea sitios de acoplamiento para proteínas de señalización intracelular que contienen dominios SH2 (Src Homology 2). Entre las vías de señalización clave activadas por el CSF1R se encuentran la vía de las MAP quinasas (ERK1/2, p38, JNK), la vía de la PI3K/Akt (fosfoinosítido 3-quinasa/proteína quinasa B) y la vía de las STAT (transductores de señal y activadores de la transcripción). Estas vías regulan una miríada de procesos celulares, incluyendo la proliferación, la diferenciación, la supervivencia celular, la migración, la fagocitosis y la producción de otras citocinas y quimiocinas.
Funciones Fisiológicas Diversas del M-CSF
Más allá de su rol canónico en la hematopoyesis, el M-CSF ejerce funciones críticas en múltiples sistemas orgánicos:
-
Sistema Inmune: Es esencial para el desarrollo y la homeostasis de las poblaciones de macrófagos residentes en tejidos, como las células de Kupffer en el hígado, los macrófagos alveolares en los pulmones y la microglía en el cerebro. Regula la polarización de los macrófagos hacia fenotipos pro-inflamatorios (M1) o anti-inflamatorios/reparadores (M2), influyendo en la resolución de la inflamación y la reparación tisular.
-
Remodelación Ósea: El M-CSF es un factor indispensable para la osteoclastogénesis, el proceso de formación de osteoclastos, las células responsables de la resorción ósea. En sinergia con el RANKL (ligando del receptor activador del factor nuclear kappa B), M-CSF promueve la diferenciación de precursores monocíticos en osteoclastos maduros y funcionales, manteniendo el equilibrio dinámico entre la formación y la resorción ósea.
-
Sistema Nervioso: En el cerebro, el M-CSF y su receptor CSF1R son fundamentales para el desarrollo, la supervivencia y la función de la microglía, los macrófagos residentes del sistema nervioso central. Modula la plasticidad sináptica, la neurogénesis y la eliminación de residuos celulares, jugando un papel neuroprotector en condiciones de lesión o enfermedad neurodegenerativa.
-
Reproducción: El M-CSF es crucial para el desarrollo placentario, la implantación del embrión y la gestación. Es producido por las células del trofoblasto y las células estromales uterinas, promoviendo la proliferación y diferenciación de los macrófagos deciduales, que son esenciales para la tolerancia inmunológica materno-fetal y el soporte del embarazo.
-
Metabolismo: En el tejido adiposo, el M-CSF influye en la diferenciación y función de los macrófagos adiposos, que son actores clave en la inflamación crónica asociada a la obesidad y la resistencia a la insulina. Modula el metabolismo lipídico y la sensibilidad a la insulina, sugiriendo un papel en las enfermedades metabólicas.
Regulación y Antagonistas del M-CSF
La actividad del M-CSF está sujeta a una estricta regulación para evitar una activación inmunológica descontrolada o una disfunción tisular. Esta regulación ocurre a múltiples niveles:
-
Regulación de la Expresión Génica: Como se mencionó, la transcripción del gen CSF1 es modulada por factores de transcripción y citocinas pro-inflamatorias y anti-inflamatorias. Por ejemplo, citocinas como la IL-10 y el TGF-β pueden suprimir la producción de M-CSF, actuando como frenos en la respuesta inmune.
-
Disponibilidad del Ligando y del Receptor: La escisión proteolítica del M-CSF unido a la membrana por enzimas como las metaloproteinasas de la matriz (MMPs) puede liberar la forma soluble, alterando su biodisponibilidad. De manera similar, el receptor CSF1R puede ser internalizado tras la unión del ligando o escindido de la superficie celular, reduciendo la señalización.
-
Señalización Negativa Intracelular: Las células poseen mecanismos intrínsecos para atenuar la señalización del CSF1R, como las fosfatasas de tirosina (por ejemplo, PTPN6/SHP-1) que desfosforilan los residuos de tirosina del receptor y de las proteínas de señalización, interrumpiendo las cascadas de transducción. También existen proteínas supresoras de la señalización de citocinas (SOCS) que pueden inhibir las vías STAT activadas por M-CSF.
-
Moléculas Antagonistas o Terapéuticas: En contextos patológicos, se han desarrollado estrategias para modular la actividad del M-CSF. Anticuerpos monoclonales que bloquean el M-CSF o el CSF1R, así como inhibidores de moléculas pequeñas que actúan sobre la actividad tirosina quinasa del CSF1R, se están investigando como terapias para el cáncer, enfermedades autoinmunes y otras condiciones inflamatorias.
M-CSF, Cetosis y Ayuno: Una Conexión Emergente
El interés en la interacción entre el M-CSF y los estados metabólicos como la cetosis y el ayuno ha crecido exponencialmente. Se sabe que tanto la dieta cetogénica como el ayuno intermitente o prolongado inducen cambios significativos en el sistema inmune y en el metabolismo energético.
La cetosis, caracterizada por la producción de cuerpos cetónicos (β-hidroxibutirato, acetoacetato y acetona), tiene potentes efectos antiinflamatorios e inmunomoduladores. El β-hidroxibutirato (BHB), el cuerpo cetónico más abundante, ha demostrado inhibir el inflamasoma NLRP3 y modular la función de los macrófagos. Dado que el M-CSF es un regulador clave de la diferenciación y polarización de los macrófagos, es plausible que los estados de cetosis y ayuno influyan en la vía M-CSF/CSF1R.
Estudios preliminares sugieren que el ayuno puede modular la expresión de M-CSF y CSF1R, afectando la infiltración y polarización de macrófagos en diversos tejidos, incluyendo el tejido adiposo. En la obesidad, los macrófagos en el tejido adiposo a menudo adoptan un fenotipo pro-inflamatorio (M1), contribuyendo a la resistencia a la insulina. La cetosis y el ayuno podrían promover una polarización hacia macrófagos M2, que son anti-inflamatorios y pro-resolutivos, posiblemente a través de la modulación de las vías de señalización dependientes de M-CSF.
Además, el M-CSF está implicado en la función mitocondrial y el metabolismo de lípidos. Los macrófagos, células altamente plásticas, adaptan su metabolismo a su microambiente y estado funcional. Los cuerpos cetónicos podrían influir en la reprogramación metabólica de los macrófagos, alterando su dependencia de la glucólisis o la fosforilación oxidativa, y potencialmente impactando su respuesta a las señales de M-CSF. Esta área de investigación es prometedora para entender cómo las intervenciones dietéticas pueden optimizar la salud inmunometabólica.
Dato Médico de Optimización: La activación controlada de la vía M-CSF/CSF1R, a través de estrategias que modulan la polarización de macrófagos hacia un fenotipo M2 (antiinflamatorio y reparador), podría ser una clave para potenciar la resiliencia metabólica. Ciertos compuestos bioactivos presentes en dietas ricas en polifenoles y ácidos grasos omega-3 han demostrado modular la función macrofágica, lo que sugiere un camino para optimizar la respuesta inflamatoria y la reparación tisular. La modulación de esta vía puede ser esencial para la longevidad y la prevención de enfermedades crónicas, especialmente en el contexto de la autofagia y la mitofagia inducidas por el ayuno.
M-CSF en Patologías: Desde la Inflamación Crónica al Cáncer
La desregulación de la vía M-CSF/CSF1R está implicada en una amplia gama de patologías:
-
Enfermedades Inflamatorias Crónicas y Autoinmunes: Niveles elevados de M-CSF y una mayor expresión de CSF1R se observan en enfermedades como la artritis reumatoide, la esclerosis múltiple y la enfermedad inflamatoria intestinal. En estos contextos, el M-CSF contribuye a la infiltración de macrófagos pro-inflamatorios en los tejidos afectados, perpetuando el ciclo de inflamación y daño tisular.
-
Cáncer: El M-CSF es un factor clave en el microambiente tumoral. Promueve la supervivencia, proliferación y diferenciación de los macrófagos asociados al tumor (TAMs), que a menudo adoptan un fenotipo M2. Los TAMs son notorios por su capacidad para suprimir la respuesta inmune antitumoral, promover la angiogénesis, la metástasis y la resistencia a la quimioterapia. Por ello, la inhibición de la vía M-CSF/CSF1R es una estrategia terapéutica prometedora en oncología.
-
Aterosclerosis: En esta enfermedad cardiovascular, el M-CSF contribuye a la acumulación de monocitos y su diferenciación en macrófagos espumosos dentro de las placas ateroscleróticas. Estos macrófagos fagocitan lípidos modificados y liberan citocinas pro-inflamatorias, exacerbando la progresión de la enfermedad.
-
Osteoporosis: Un desequilibrio en el eje M-CSF/RANKL puede llevar a una excesiva actividad osteoclástica y, consecuentemente, a la pérdida de densidad ósea, como se observa en la osteoporosis y otras enfermedades óseas.
-
Enfermedades Neurodegenerativas: Aunque el M-CSF es neuroprotector en condiciones fisiológicas, su desregulación en enfermedades como el Alzheimer o el Parkinson puede contribuir a la neuroinflamación y a la disfunción microglial, acelerando la progresión de la enfermedad.
Advertencia Médica: La sobreactivación crónica de la vía M-CSF/CSF1R puede ser un motor subyacente de la inflamación sistémica y la progresión de diversas enfermedades crónicas, incluyendo ciertos tipos de cáncer y trastornos autoinmunes. La manipulación de esta vía debe realizarse bajo supervisión médica estricta, ya que un desequilibrio puede tener consecuencias significativas en la función inmunológica y la homeostasis tisular, potencialmente exacerbando condiciones existentes o provocando efectos adversos.
Implicaciones Terapéuticas y Futuras Direcciones
Dada la amplia implicación del M-CSF en la fisiopatología de numerosas enfermedades, su vía de señalización se ha convertido en un objetivo terapéutico atractivo. Los inhibidores del CSF1R, tanto anticuerpos como pequeñas moléculas, están siendo evaluados en ensayos clínicos para el tratamiento de diversos cánceres, con el objetivo de reprogramar los macrófagos asociados al tumor y potenciar las respuestas inmunes antitumorales. También hay interés en su uso para enfermedades autoinmunes y fibrosis, donde la supresión de la actividad macrofágica pro-inflamatoria podría ser beneficiosa.
Sin embargo, la complejidad de la vía M-CSF/CSF1R y sus múltiples funciones fisiológicas presentan desafíos. Una inhibición sistémica y prolongada podría tener efectos secundarios indeseables, como inmunosupresión o alteraciones en la remodelación ósea. Por lo tanto, las futuras estrategias terapéuticas se centran en la modulación más selectiva de la vía, quizás a través de la focalización en isoformas específicas de M-CSF o en subpoblaciones de macrófagos.
La investigación futura también explorará más a fondo la conexión entre el M-CSF y el metabolismo. Comprender cómo los estados nutricionales y las intervenciones dietéticas, como la cetosis, influyen en la expresión y la función del M-CSF podría abrir nuevas vías para el desarrollo de estrategias preventivas y terapéuticas para enfermedades metabólicas e inflamatorias. La plasticidad de los macrófagos y su capacidad para adaptarse a las señales del microambiente ofrecen un terreno fértil para la investigación translacional.
Conclusión
El factor estimulante de colonias de macrófagos (M-CSF) es mucho más que un simple factor de crecimiento hematopoyético. Es un regulador maestro de la biología de monocitos y macrófagos, con funciones esenciales que abarcan desde el desarrollo embrionario y la homeostasis tisular hasta la respuesta inmune y la reparación. Su compleja interacción con el receptor CSF1R orquesta una sinfonía de señales intracelulares que dictan el destino y la función de estas células inmunológicas omnipresentes.
La profunda implicación del M-CSF en la fisiopatología de enfermedades como el cáncer, las enfermedades autoinmunes y los trastornos metabólicos lo convierte en un objetivo terapéutico de alto valor. A medida que nuestra comprensión de su biología molecular y sus intrincadas redes de señalización se profundiza, también lo hace nuestro potencial para desarrollar intervenciones más precisas y efectivas. Para el Glosario Ketocis, la relevancia del M-CSF radica en su potencial rol como modulador de la respuesta inmune y metabólica en estados de cetosis y ayuno, abriendo un emocionante capítulo en la intersección de la inmunometabolismo y las estrategias de optimización de la salud.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.