MicroARN (miARN): Guía Definitiva de Regulación Genética y Salud
Resumen Clínico Rápido
🔬 Clasificación
ARN no codificante pequeño
⚙️ Función
Regulación post-transcripcional
📋 Impacto
Salud, enfermedad, metabolismo
¿Qué es un microARN (miARN)? La Arquitectura Invisible de la Regulación Genética
En el vasto y complejo universo de la biología molecular, donde el ADN es el plano maestro de la vida, existen orquestadores sutiles pero poderosos que afinan la expresión de nuestros genes. Entre ellos, los microARNs (miARNs) emergen como protagonistas silenciosos, pequeñas secuencias de ácido ribonucleico no codificante que, a pesar de su diminuto tamaño, ejercen un control monumental sobre casi todos los procesos celulares. Imagínese una biblioteca inmensa, donde cada libro es un gen. Los miARNs no escriben libros nuevos, pero deciden cuáles se leen, con qué frecuencia y cuándo se guardan en el estante, influyendo así en el destino y la función de cada célula.
Estos enigmáticos reguladores no codificantes fueron descubiertos por primera vez en Caenorhabditis elegans a principios de los años 90, pero no fue hasta principios del nuevo milenio que su omnipresencia y trascendencia en el mundo animal y vegetal se hizo evidente. Desde entonces, la investigación sobre los miARNs ha explotado, revelando su participación en el desarrollo embrionario, la diferenciación celular, la respuesta inmune, la homeostasis metabólica y, lamentablemente, en la progresión de innumerables enfermedades, desde el cáncer hasta las patologías neurodegenerativas. Su estudio es una ventana a la sofisticación de la vida, ofreciéndonos nuevas vías para comprender y, potencialmente, modular nuestra propia biología.
Resumen Clínico: Puntos Clave sobre los microARNs
- Reguladores Maestros: Los microARNs son pequeñas moléculas de ARN no codificante que controlan la expresión génica a nivel post-transcripcional.
- Biogénesis Precisa: Su formación implica un proceso meticuloso que incluye las enzimas Drosha y Dicer, resultando en una molécula madura de aproximadamente 22 nucleótidos.
- Mecanismo de Acción: Se asocian al complejo RISC (RNA-induced silencing complex) para silenciar genes, ya sea degradando el ARNm objetivo o reprimiendo su traducción proteica.
- Impacto Sistémico: Influencian una miríada de procesos biológicos, desde el desarrollo y la diferenciación celular hasta la respuesta inmune y el metabolismo energético.
- Biomarcadores y Terapia: La desregulación de los miARNs está ligada a diversas enfermedades, lo que los convierte en prometedores biomarcadores diagnósticos y en dianas terapéuticas innovadoras.
El Propósito Evolutivo de los miARNs: La Precisión como Ventaja Selectiva
La existencia de los miARNs no es casualidad; es el resultado de millones de años de evolución que han favorecido la eficiencia y la adaptabilidad. Su propósito evolutivo principal radica en la capacidad de afinar y modular la expresión génica con una precisión exquisita. A diferencia de los factores de transcripción que regulan el inicio de la síntesis de ARN, los miARNs actúan a nivel post-transcripcional, proporcionando una capa adicional y rápida de control. Esta capacidad de silenciar genes de forma rápida y reversible es crucial para la plasticidad celular y la respuesta a los cambios ambientales.
Imagínese una célula que necesita cambiar rápidamente su programa genético para adaptarse a un nuevo nutriente o para defenderse de un patógeno. Los miARNs permiten que la célula “apague” ciertos programas y “encienda” otros sin la necesidad de sintetizar nuevas proteínas reguladoras o de degradar completamente los ARNm existentes, lo que sería un proceso más lento y energéticamente costoso. Esta agilidad en la regulación es una ventaja selectiva formidable, permitiendo a los organismos responder de manera más eficiente al estrés, optimizar el uso de recursos y garantizar un desarrollo embrionario sin errores. Son, en esencia, los directores de orquesta que aseguran que cada instrumento genético toque la nota correcta en el momento preciso.
Los microARNs son solo 'ADN basura' sin función biológica relevante.
Los microARNs son secuencias de ARN no codificante que actúan como reguladores maestros de la expresión génica, silenciando o degradando ARNm específicos. Son esenciales para el desarrollo, la homeostasis celular y la respuesta a estímulos, y su desregulación está implicada en múltiples patologías.
Fisiología Molecular: La Intrincada Danza de la Biogénesis y la Función
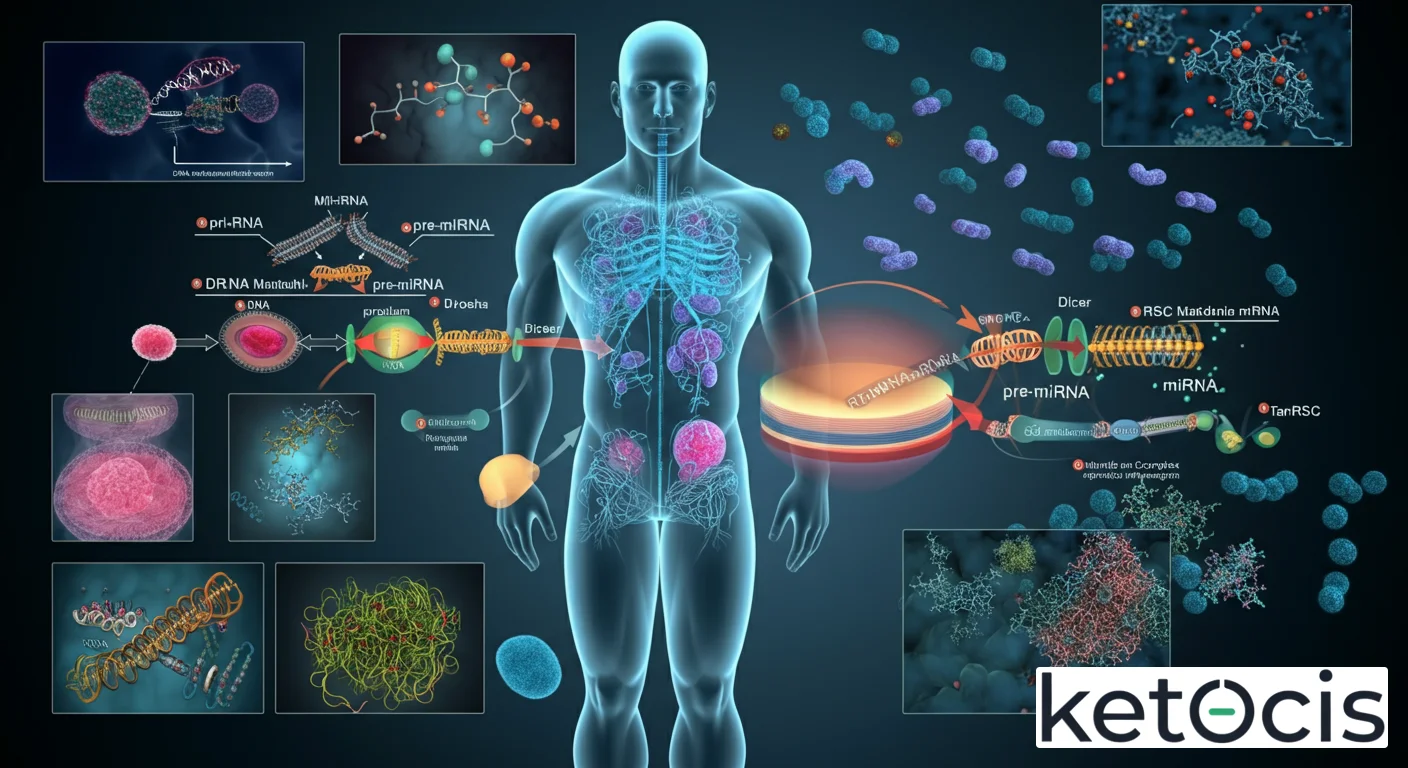
La vida de un miARN es un viaje fascinante de transformación y asociación. Todo comienza en el núcleo, donde los genes de miARN se transcriben en largas moléculas de ARN llamadas pri-miARNs (microARNs primarios). Estas moléculas, que pueden tener varios miles de nucleótidos, contienen estructuras de horquilla que son clave para su procesamiento. Aquí entra en juego un complejo proteico central: la ribonucleasa III nuclear Drosha, asociada a su cofactor DGCR8. Juntos, Drosha y DGCR8, actúan como unas “tijeras moleculares”, cortando el pri-miARN para liberar una horquilla más pequeña de aproximadamente 70 nucleótidos, conocida como pre-miARN (microARN precursor).
Una vez formado, el pre-miARN es exportado del núcleo al citoplasma por la proteína Exportina-5. En el citoplasma, el pre-miARN se encuentra con otra ribonucleasa III, la enzima Dicer. Dicer corta la horquilla del pre-miARN, generando un dúplex de ARN de doble cadena de unos 22 nucleótidos. Este dúplex es el precursor del miARN maduro. Una de las hebras del dúplex (la hebra guía) se incorpora a un complejo multiproteico llamado RISC (RNA-induced silencing complex), mientras que la otra hebra (la hebra pasajera) generalmente se degrada. Es dentro del complejo RISC donde el miARN maduro ejerce su poder regulador.
El mecanismo de acción es elegante en su simplicidad y potente en su efecto. El complejo RISC, guiado por la secuencia del miARN, busca ARNm diana en el citoplasma que tengan secuencias complementarias al miARN. La complementariedad no tiene que ser perfecta, lo que permite a un único miARN regular múltiples ARNm y a un ARNm ser regulado por múltiples miARNs. Una vez que el complejo RISC se une al ARNm diana, puede silenciar la expresión génica de dos maneras principales: 1) Reprimiendo la traducción del ARNm en proteína, impidiendo que los ribosomas sinteticen la proteína; o 2) Promoviendo la degradación del ARNm, eliminándolo de la piscina celular y, por tanto, impidiendo la síntesis de proteínas. Este control post-transcripcional permite una regulación fina y rápida de la expresión génica, esencial para la homeostasis celular y la respuesta a estímulos.
MiARNs y Salud: Desde el Desarrollo hasta la Patología
La ubicuidad de los miARNs en la regulación génica significa que su influencia se extiende a prácticamente todos los aspectos de la salud y la enfermedad. Durante el desarrollo embrionario, los miARNs son cruciales para la diferenciación celular y la formación de tejidos y órganos, asegurando que las células asuman sus identidades y funciones correctas. En el sistema inmune, modulan la respuesta inflamatoria, la activación de linfocitos y la defensa contra patógenos, actuando como interruptores moleculares que pueden amplificar o atenuar las reacciones inmunes.
La desregulación de los miARNs, ya sea por una expresión excesiva o insuficiente, está directamente implicada en una amplia gama de patologías. En el cáncer, los miARNs pueden actuar como oncogenes (promoviendo el crecimiento tumoral) o como supresores tumorales (inhibiendo el crecimiento). Por ejemplo, miR-21 es frecuentemente sobreexpresado en muchos tipos de cáncer, promoviendo la proliferación y la metástasis, mientras que miR-34a, un supresor tumoral, a menudo se encuentra disminuido. En enfermedades cardiovasculares, como la insuficiencia cardíaca y la aterosclerosis, ciertos miARNs regulan la remodelación cardíaca, la inflamación vascular y la formación de placas. Las enfermedades neurodegenerativas, como el Alzheimer y el Parkinson, también muestran perfiles de miARNs alterados, lo que sugiere su papel en la neuroinflamación y la muerte neuronal.
El Rol de los miARNs en Cetosis y Ayuno: Una Perspectiva Metabólica
Para la comunidad de “Glosario Ketocis”, la interacción entre los miARNs y los estados metabólicos como la cetosis y el ayuno es particularmente relevante. Estos pequeños reguladores son actores clave en la adaptación del cuerpo a los cambios en la disponibilidad de nutrientes, orquestando la transición entre el metabolismo de la glucosa y el de los cuerpos cetónicos. Durante el ayuno y la dieta cetogénica, el cuerpo experimenta profundas modificaciones metabólicas, incluyendo la movilización de grasas, la cetogénesis hepática y una mayor eficiencia energética.
Numerosos estudios han revelado que los perfiles de miARNs cambian significativamente en respuesta al ayuno y la restricción calórica. Por ejemplo, miARNs implicados en la regulación del metabolismo lipídico, como miR-33, que regula la biosíntesis de colesterol y el transporte de lípidos, pueden verse modulados. La disminución de miR-33, por ejemplo, podría favorecer una mayor oxidación de ácidos grasos. Otro ejemplo es miR-122, altamente expresado en el hígado, que juega un papel crucial en la homeostasis del colesterol y los ácidos grasos. Su modulación durante el ayuno puede influir en la disponibilidad de sustratos para la cetogénesis.
Además, los miARNs también influyen en procesos celulares clave activados durante el ayuno, como la autofagia y la mitofagia, mecanismos esenciales para la limpieza celular y la renovación de orgánulos. miARNs específicos pueden regular las vías de señalización que controlan estos procesos, optimizando la respuesta celular al estrés nutricional. La modulación de miARNs también se ha asociado con la mejora de la sensibilidad a la insulina y la reducción de la inflamación sistémica, dos beneficios bien documentados de la cetosis y el ayuno intermitente. Comprender cómo estos pequeños reguladores responden a estas intervenciones dietéticas abre nuevas vías para optimizar la salud metabólica.
Biohacking y miARNs: Optimización Metabólica
¿Sabías que tu microbiota intestinal puede influir en tus miARNs? Ciertas bacterias producen metabolitos que pueden modificar la expresión de miARNs en las células del huésped, impactando la absorción de nutrientes, la respuesta inmune y la salud metabólica. Optimizar tu microbiota con una dieta rica en fibra y alimentos fermentados, o incluso con probióticos específicos, podría ser una estrategia de biohacking indirecta para modular tus miARNs y potenciar los beneficios de la cetosis y el ayuno. ¡Es una conexión fascinante entre tu intestino y tu genoma silencioso!
Optimización y Potencial Terapéutico: El Futuro de la Medicina Personalizada
El profundo entendimiento de los miARNs no solo ha revelado su papel fundamental en la biología, sino que también ha desatado una ola de entusiasmo en el campo de la medicina traslacional. Su potencial se extiende en dos grandes vertientes: como biomarcadores diagnósticos y como dianas terapéuticas.
Dado que los miARNs pueden ser detectados en fluidos corporales como la sangre, la orina y la saliva, se están investigando activamente como biomarcadores no invasivos para la detección temprana de enfermedades. Un perfil específico de miARNs circulantes podría indicar la presencia de cáncer, enfermedades cardíacas o neurodegenerativas mucho antes de que aparezcan los síntomas clínicos, permitiendo intervenciones más tempranas y efectivas. Esta “biopsia líquida” a través de miARNs promete revolucionar el diagnóstico.
Desde una perspectiva terapéutica, la capacidad de modular la expresión de miARNs ofrece estrategias innovadoras. Se están desarrollando dos enfoques principales: la administración de miRNA mimetics (análogos sintéticos de miARNs supresores que están disminuidos en una enfermedad) y los antagomiRs (moléculas que secuestran o bloquean la función de miARNs oncogénicos o patogénicos sobreexpresados). Estas terapias están en diversas fases de investigación y ensayos clínicos, con resultados prometedores en áreas como la oncología, las enfermedades hepáticas y las cardiovasculares. La promesa es una medicina de precisión, donde se restaura el equilibrio de los miARNs para corregir la patología subyacente.
Más allá de las intervenciones farmacológicas, nuestro estilo de vida puede ser un modulador natural de los miARNs. La dieta, el ejercicio regular, la calidad del sueño y la gestión del estrés han demostrado influir en los perfiles de miARNs, lo que sugiere que las decisiones diarias pueden tener un impacto epigenético profundo. Adoptar un estilo de vida saludable no solo beneficia los sistemas metabólicos directamente, sino que también puede optimizar la orquestación de la expresión génica a través de estos pequeños pero poderosos reguladores.
Mitos y Realidades sobre los microARNs
Como con cualquier campo de vanguardia, los miARNs no están exentos de malentendidos y exageraciones. Es crucial discernir la ciencia de la especulación.
Alerta Médica: Cuidado con las Promesas Milagrosas
Existe el mito de que una “dieta milagrosa” o un suplemento específico puede “resetear” completamente tus miARNs para curar cualquier enfermedad o revertir el envejecimiento de forma radical. Si bien la dieta y el estilo de vida tienen un impacto innegable en la expresión de miARNs y la salud, las afirmaciones de curas totales o reseteos genéticos son, en la mayoría de los casos, simplificaciones peligrosas y carecen de respaldo científico robusto. La modulación de miARNs es un proceso complejo y multifactorial; se requiere mucha más investigación antes de que cualquier terapia con miARNs esté ampliamente disponible y sea segura para el público general. Siempre consulta a profesionales de la salud antes de adoptar tratamientos no verificados.
Un mito común es la idea de que los microARNs son solo “ADN basura” o “ARN sin importancia” porque no codifican proteínas. La realidad es diametralmente opuesta: son reguladores maestros. Otro mito es la creencia de que un solo miARN es la clave para una enfermedad, lo que lleva a la búsqueda de una “bala mágica” terapéutica. En verdad, la mayoría de las patologías implican una compleja red de miARNs desregulados que interactúan con múltiples vías génicas. La ciencia avanza en la comprensión de estas redes, no en la simplificación excesiva.
Conclusión: Los Silenciosos Arquitectos de la Vida
Los microARNs representan una de las revelaciones más fascinantes de la biología moderna. Estos pequeños fragmentos de ARN no codificante han pasado de ser una curiosidad de laboratorio a ser reconocidos como reguladores esenciales de la expresión génica, con implicaciones profundas para la salud, la enfermedad y la adaptación evolutiva. Su intrincada biogénesis y su mecanismo de acción, que silencian genes con precisión quirúrgica, subraya la elegancia y la eficiencia de la maquinaria molecular de la vida.
Desde el desarrollo embrionario hasta la respuesta a los desafíos metabólicos como la cetosis y el ayuno, los miARNs actúan como guardianes del equilibrio celular. Su desregulación es un sello distintivo de numerosas patologías, lo que los convierte en valiosos biomarcadores y en prometedoras dianas terapéuticas para la medicina del futuro. A medida que continuamos desentrañando la complejidad de estas moléculas, se abre un panorama de posibilidades para la prevención, el diagnóstico y el tratamiento de enfermedades, acercándonos a una era de medicina verdaderamente personalizada y molecularmente informada. Los microARNs nos recuerdan que, a menudo, los jugadores más pequeños son los que ejercen la mayor influencia en el gran teatro de la vida.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.