HFE: Proteína de Hemocromatosis Humana | Glosario Ketocis
Resumen Clínico Rápido
🔬 Clasificación
Proteína MHC Clase I-like
⚙️ Función
Regulación de hepcidina y hierro
📋 Impacto
Hemocromatosis hereditaria
La Proteína de Hemocromatosis Humana (HFE): Guardián del Hierro y Raíz de un Desequilibrio Genético
En el vasto y complejo universo de la bioquímica humana, existen proteínas cuya función es tan vital como sutil. Una de ellas es la proteína HFE, un componente clave en la intrincada danza del metabolismo del hierro. Su nombre, un acrónimo de Human Hemochromatosis Protein, ya nos da una pista de su profunda conexión con una de las enfermedades genéticas más comunes: la hemocromatosis hereditaria. Esta condición, caracterizada por una sobrecarga de hierro en el organismo, puede tener consecuencias devastadoras si no se detecta y gestiona a tiempo.
Como investigadores médicos y expertos en la intersección de la genética, la nutrición y la salud metabólica, nos adentramos en el fascinante mundo de la HFE. Comprender su estructura, su mecanismo de acción y las implicaciones de sus mutaciones es fundamental no solo para el diagnóstico y tratamiento de la hemocromatosis, sino también para apreciar la delicada homeostasis que rige nuestro cuerpo. En este artículo, desgranaremos cada faceta de la HFE, desde su origen molecular hasta su papel en la regulación sistémica del hierro, ofreciendo una guía exhaustiva para el Glosario Ketocis.
Origen y Estructura Molecular de la HFE
La proteína HFE es un miembro atípico de la superfamilia del Complejo Mayor de Histocompatibilidad (MHC) de clase I. A diferencia de sus parientes más conocidos, que presentan péptidos antigénicos a las células T, la HFE ha evolucionado para desempeñar un papel completamente diferente en la fisiología humana. Codificada por el gen HFE, localizado en el brazo corto del cromosoma 6 (6p21.3), esta proteína se expresa en la superficie de diversas células, incluyendo hepatocitos, células de las criptas duodenales y macrófagos.
Estructuralmente, la HFE se compone de una cadena alfa pesada y una cadena ligera no covalente conocida como beta-2 microglobulina (β2m). La asociación con β2m es crucial para el plegamiento correcto y la expresión en la superficie celular de la HFE. Esta estructura dota a la proteína de una configuración tridimensional específica que le permite interactuar con otras moléculas clave en el metabolismo del hierro. La HFE es una proteína transmembrana, con un dominio extracelular que contiene los sitios de interacción, un segmento transmembrana y una cola citoplasmática corta que puede participar en la señalización intracelular.
La historia evolutiva de la HFE sugiere una adaptación para optimizar el manejo del hierro, un elemento esencial pero también potencialmente tóxico. Su origen se remonta a la necesidad de mantener un equilibrio preciso entre la disponibilidad de hierro para funciones vitales como el transporte de oxígeno y la síntesis de ADN, y la prevención de su acumulación excesiva, que genera radicales libres y daño oxidativo. Esta dualidad subraya la importancia crítica de la HFE en la salud humana.
La hemocromatosis es una enfermedad exclusiva de personas mayores o alcohólicas.
La hemocromatosis hereditaria es una condición genética que puede manifestarse a cualquier edad y no está directamente ligada al consumo excesivo de alcohol, aunque el alcohol puede agravar el daño hepático. La mutación más común afecta a la proteína HFE, alterando la homeostasis del hierro desde el nacimiento.
Mecanismo de Acción: La Danza del Hierro y la Hepcidina
El papel central de la proteína HFE reside en su capacidad para regular la homeostasis sistémica del hierro, principalmente a través de su influencia en la producción de hepcidina, una hormona peptídica sintetizada en el hígado y considerada el principal regulador negativo del hierro. La hepcidina controla los niveles de hierro en el plasma actuando sobre la ferroportina, la única proteína exportadora de hierro conocida, presente en enterocitos, macrófagos y hepatocitos.
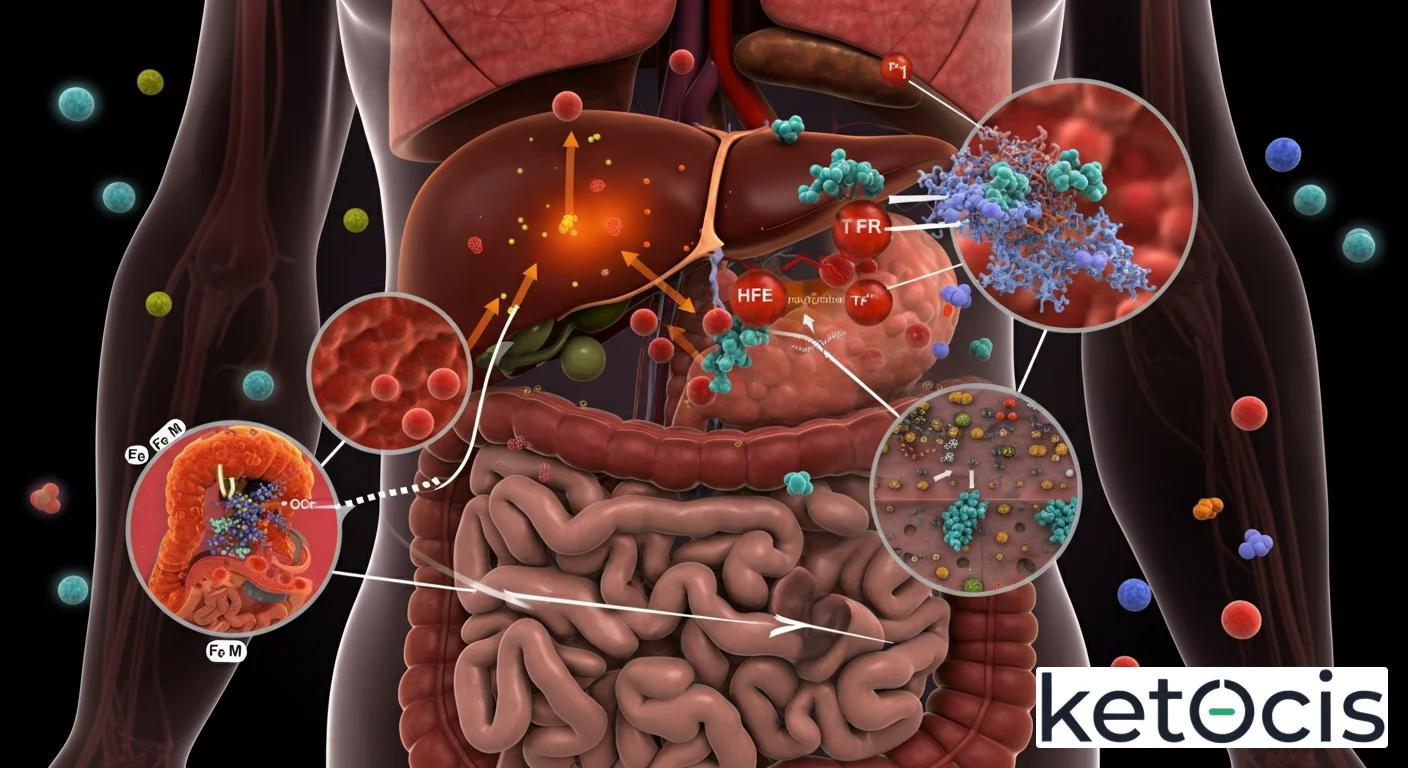
El mecanismo molecular es intrincado. En condiciones normales, la HFE forma un complejo en la superficie celular con el receptor de transferrina 1 (TfR1) y la beta-2 microglobulina. La transferrina, una proteína transportadora de hierro en la sangre, se une al TfR1 para introducir el hierro en las células. Cuando la HFE se une al TfR1, reduce la afinidad de este último por la transferrina cargada de hierro. Sin embargo, el papel más crítico de la HFE es su interacción con otra molécula clave: el receptor de transferrina 2 (TfR2), que también se expresa en los hepatocitos, y con la hemojuvelina (HJV), un correceptor. Este complejo HFE-TfR2-HJV actúa como un sensor de los niveles de hierro circulante, enviando señales al hígado para ajustar la producción de hepcidina.
Cuando los niveles de hierro son altos, este complejo señaliza al hígado para que aumente la producción de hepcidina. La hepcidina, a su vez, se une a la ferroportina, induciendo su internalización y degradación. Esto reduce la liberación de hierro de las células de almacenamiento y la absorción de hierro dietético en el intestino, disminuyendo así los niveles de hierro en el plasma. Por el contrario, cuando los niveles de hierro son bajos, la señalización a través del complejo HFE se atenúa, la producción de hepcidina disminuye, y la ferroportina se mantiene activa, permitiendo la liberación y absorción de hierro.
Las mutaciones más comunes en el gen HFE, como la C282Y y la H63D, alteran esta delicada maquinaria. La mutación C282Y, en particular, impide que la HFE se una a la beta-2 microglobulina y, por lo tanto, que se exprese correctamente en la superficie celular. Sin una HFE funcional, el complejo sensor de hierro en el hígado no puede enviar la señal adecuada para aumentar la producción de hepcidina. El resultado es una deficiencia relativa de hepcidina, lo que lleva a una absorción intestinal de hierro incontrolada y una liberación excesiva de hierro de los macrófagos, culminando en la sobrecarga sistémica característica de la hemocromatosis.
La Hemocromatosis Hereditaria: Cuando el Guardián Falla
La hemocromatosis hereditaria (HH) es una enfermedad genética autosómica recesiva, lo que significa que un individuo debe heredar dos copias mutadas del gen HFE (una de cada progenitor) para desarrollar la forma más común y grave de la enfermedad. La mutación C282Y es la más prevalente y se asocia con la forma clásica de la enfermedad, mientras que la mutación H63D, aunque menos penetrante, también puede contribuir a la sobrecarga de hierro, especialmente en combinación con la C282Y (heterocigoto compuesto).
La consecuencia directa de una HFE defectuosa es la incapacidad del cuerpo para detectar adecuadamente los niveles de hierro. Esto provoca que el intestino delgado continúe absorbiendo hierro de la dieta sin restricciones, y que los macrófagos liberen hierro almacenado, incluso cuando los depósitos corporales ya están repletos. Con el tiempo, este exceso de hierro se acumula progresivamente en diversos órganos, siendo los más afectados el hígado, el corazón, el páncreas, las articulaciones y la hipófisis.
Los síntomas de la hemocromatosis suelen manifestarse en la edad adulta, generalmente entre los 40 y 60 años, aunque el daño comienza mucho antes. Los hombres suelen presentar síntomas más temprano y de forma más severa que las mujeres, debido a las pérdidas menstruales y los embarazos, que actúan como una forma natural de flebotomía. Las manifestaciones clínicas incluyen fatiga crónica, dolor articular, daño hepático (cirrosis, carcinoma hepatocelular), diabetes mellitus (por daño pancreático), arritmias cardíacas y miocardiopatía, hipogonadismo y coloración bronceada de la piel (de ahí el término “diabetes bronceada”).
El diagnóstico precoz es crucial. Se basa en la detección de niveles elevados de ferritina sérica (un marcador de los depósitos de hierro) y un alto porcentaje de saturación de transferrina (la proporción de transferrina unida al hierro). La confirmación se realiza mediante pruebas genéticas para identificar las mutaciones en el gen HFE. El tratamiento principal es la flebotomía terapéutica, que consiste en la extracción regular de sangre para reducir los depósitos de hierro en el cuerpo. Este método es altamente efectivo si se inicia antes de que se produzca un daño orgánico irreversible.
HFE y la Salud Metabólica: Más Allá de la Hemocromatosis
Aunque la HFE es predominantemente conocida por su papel en la hemocromatosis, su influencia se extiende a otros aspectos de la salud metabólica. La sobrecarga de hierro no solo daña órganos directamente, sino que también puede exacerbar condiciones como la resistencia a la insulina y el síndrome metabólico. El exceso de hierro hepático, por ejemplo, ha sido implicado en la patogénesis de la esteatosis hepática no alcohólica (EHNA) y la progresión a esteatohepatitis no alcohólica (EHNA), incluso en ausencia de hemocromatosis clínica.
La relación entre la HFE y el metabolismo del hierro también tiene implicaciones para el contexto de la cetosis y el ayuno. Un metabolismo de hierro bien regulado es fundamental para la función mitocondrial y la producción de energía, procesos clave en estados cetogénicos. Si bien no hay una interacción directa y única entre la HFE y la cetosis, una sobrecarga de hierro no tratada puede comprometer la salud mitocondrial y la capacidad del cuerpo para utilizar grasas eficientemente, afectando indirectamente los beneficios de una dieta cetogénica o el ayuno intermitente. La inflamación crónica asociada con la sobrecarga de hierro puede, además, contrarrestar los efectos antiinflamatorios de la cetosis.
Por otro lado, el ayuno intermitente y las dietas cetogénicas, al reducir la inflamación y mejorar la sensibilidad a la insulina, podrían ofrecer beneficios generales para la salud que, en teoría, podrían mitigar algunos de los efectos sistémicos de la sobrecarga de hierro, aunque nunca sustituirán la flebotomía como tratamiento principal. Es un área que requiere más investigación específica, pero subraya la interconexión de los sistemas metabólicos.
Factores que Influyen en la HFE y Estrategias de Optimización
La actividad de la proteína HFE y, por extensión, el metabolismo del hierro, están influenciados por una variedad de factores genéticos y ambientales. Además de las mutaciones en el propio gen HFE, existen otros genes moduladores de la hepcidina que pueden influir en la expresión fenotípica de la hemocromatosis. Por ejemplo, mutaciones en genes como el receptor de transferrina 2 (TfR2), la hemojuvelina (HJV) o la propia hepcidina (HAMP) también pueden causar formas menos comunes de hemocromatosis.
Desde una perspectiva de biohacking y optimización, para individuos con predisposición genética a la sobrecarga de hierro (heterocigotos para mutaciones HFE o con riesgo elevado), ciertas estrategias pueden ser beneficiosas, siempre bajo supervisión médica. Estas incluyen:
- Monitoreo regular: Realizar análisis de sangre periódicos para medir los niveles de ferritina y saturación de transferrina.
- Dieta: Moderar el consumo de alimentos ricos en hierro hemo (carnes rojas, vísceras) y evitar suplementos de hierro o multivitamínicos que lo contengan. Limitar el alcohol, que agrava el daño hepático.
- Vitamina C: Consumir vitamina C con precaución, especialmente en grandes dosis y junto con comidas ricas en hierro, ya que aumenta la absorción.
- Donación de sangre: Para aquellos diagnosticados con hemocromatosis, la donación de sangre regular (flebotomía terapéutica) es el tratamiento de elección para reducir los depósitos de hierro.
- Fitonutrientes: Algunos compuestos vegetales, como los taninos presentes en el té o el café, pueden inhibir la absorción de hierro no hemo. Consumirlos durante las comidas puede ser una estrategia, aunque su impacto es limitado en la hemocromatosis grave.
La clave es un enfoque proactivo y personalizado, guiado por el conocimiento genético y el monitoreo clínico. La comprensión de cómo la proteína HFE regula el hierro nos permite tomar decisiones informadas para proteger nuestra salud a largo plazo.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.