Ligando PD-L1: Clave en Inmunidad y Cáncer | Glosario Ketocis
Resumen Clínico Rápido
🔬 Clasificación
Glicoproteína transmembrana (familia B7)
⚙️ Función
Inhibición de linfocitos T, tolerancia inmune
📋 Impacto
Evasión tumoral, blanco de inmunoterapia
¿Qué es el Ligando de Muerte Programada 1 (PD-L1)? Un Pilar de la Inmunidad y la Inmunooncología
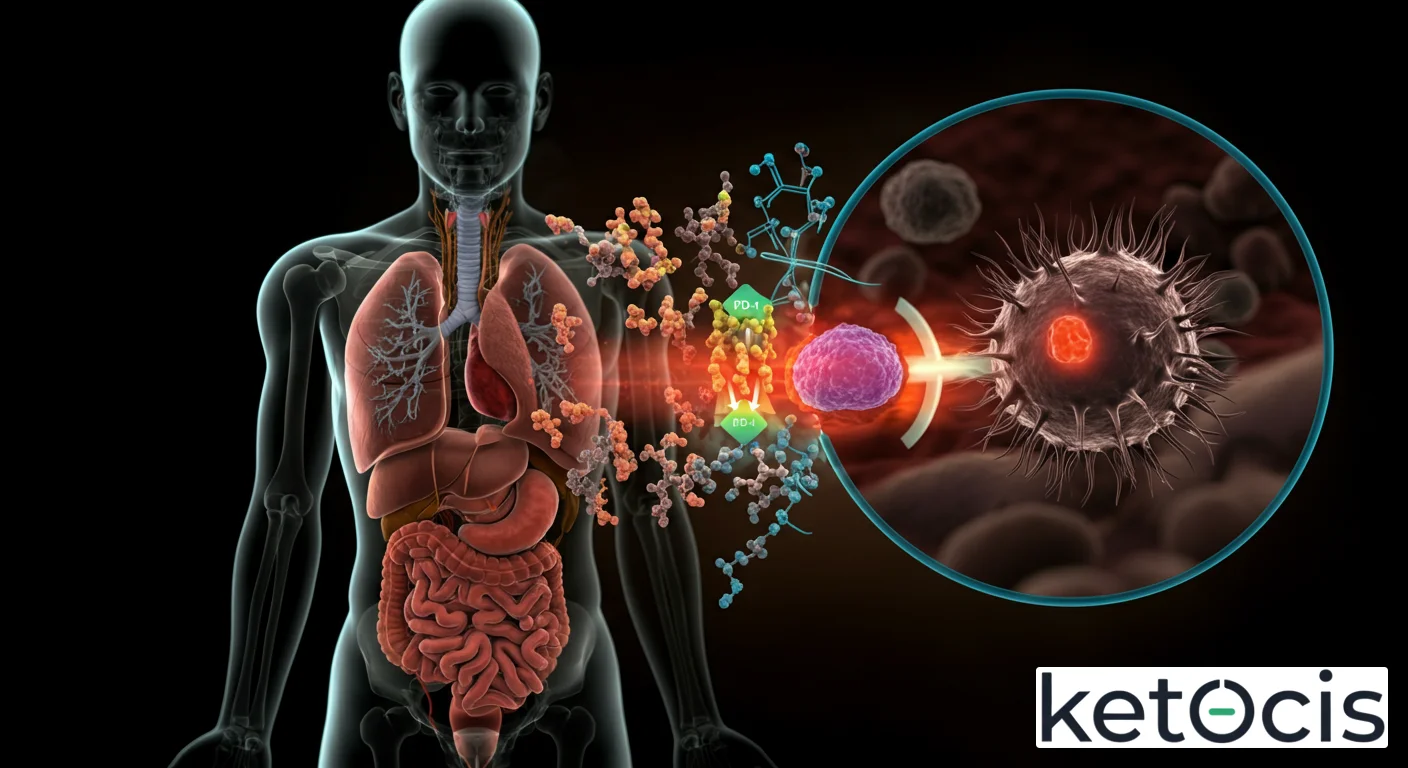
En el fascinante y complejo universo de la biología humana, existen mecanismos intrincados que rigen el equilibrio de nuestros sistemas. Uno de los más críticos, especialmente en el contexto de la defensa contra enfermedades y el mantenimiento de la salud, es la regulación de la respuesta inmunológica. Dentro de este entramado, el ligando de muerte programada 1, conocido universalmente como PD-L1 (del inglés, Programmed Death-Ligand 1), emerge como una molécula de inmensa relevancia. Se trata de una glicoproteína de transmembrana que desempeña un papel central en la modulación de la actividad de los linfocitos T, los guardianes más feroces de nuestro sistema inmune, y que ha revolucionado el tratamiento del cáncer al ser un objetivo clave para las inmunoterapias.
PD-L1 es una pieza fundamental del sistema de puntos de control inmunes, una serie de ‘frenos’ moleculares diseñados para evitar que el sistema inmune ataque erróneamente a las células sanas del propio cuerpo, un fenómeno conocido como autoinmunidad. Su interacción con su receptor cognado, el receptor de muerte programada 1 (PD-1), expresado principalmente en los linfocitos T activados, envía una señal inhibitoria que ‘apaga’ la respuesta inmune. Este mecanismo es vital para mantener la tolerancia inmunológica periférica y prevenir la inflamación excesiva tras una infección. Sin embargo, en un giro paradójico, este mismo mecanismo de protección es astutamente secuestrado por las células cancerosas para evadir la detección y destrucción por parte del sistema inmune, permitiéndoles crecer y proliferar sin control. Comprender la fisiología molecular y el papel clínico de PD-L1 es, por tanto, indispensable para cualquier investigador médico y para la vanguardia de la oncología moderna.
-
Resumen Clínico
- El Ligando de Muerte Programada 1 (PD-L1) es una glicoproteína transmembrana clave en la modulación de la respuesta inmune.
- Su interacción con el receptor PD-1 en los linfocitos T inhibe la activación y proliferación de estas células, previniendo la autoinmunidad.
- Las células tumorales a menudo sobreexpresan PD-L1 para evadir el ataque inmune, creando un microambiente inmunosupresor.
- PD-L1 es un biomarcador y un objetivo terapéutico fundamental para los inhibidores de puntos de control inmunes en el tratamiento del cáncer.
Propósito Evolutivo: El Delicado Equilibrio de la Tolerancia Inmune
La existencia de moléculas como PD-L1 no es una casualidad biológica; es el resultado de millones de años de evolución, forjando un sistema inmune capaz de discernir entre lo propio y lo ajeno, y de actuar con la fuerza necesaria sin causar daño colateral. El sistema inmune es una espada de doble filo: esencial para la supervivencia, pero potencialmente devastador si no se controla adecuadamente. Los puntos de control inmunes son los reguladores esenciales que aseguran este equilibrio.
El eje PD-1/PD-L1 es un ejemplo paradigmático de este control. Su función primaria es inducir la tolerancia inmunológica periférica. Esto significa que, una vez que los linfocitos T han cumplido su misión de eliminar una amenaza (como un virus o una bacteria), o si encuentran antígenos propios en tejidos sanos, la señalización a través de PD-1/PD-L1 frena su actividad. Esto evita la inflamación crónica, el daño a los tejidos sanos y el desarrollo de enfermedades autoinmunes. Por ejemplo, en órganos inmunoprivilegiados como el ojo o durante el embarazo (donde el feto es genéticamente ‘ajeno’), la expresión de PD-L1 es crucial para proteger estos sitios de un ataque inmune indebido. Es una medida de seguridad biológica que permite al cuerpo coexistir con sus propios componentes y con entidades no amenazantes de manera pacífica.
Un resultado negativo de PD-L1 significa que la inmunoterapia no funcionará en absoluto.
Aunque la expresión de PD-L1 es un biomarcador clave, su ausencia no descarta completamente una respuesta a la inmunoterapia. Otros factores como la carga mutacional tumoral o la presencia de células T infiltrantes pueden influir. Además, los métodos de prueba y la heterogeneidad tumoral complican la interpretación, y algunos pacientes PD-L1 negativos responden.
Fisiología Molecular: La Danza de PD-L1 y PD-1 en la Superficie Celular
Para comprender la magnitud de PD-L1, es esencial adentrarse en su estructura y función a nivel molecular. PD-L1, también conocido como B7-H1 o CD274, es una glicoproteína de tipo I que pertenece a la superfamilia B7 de moléculas coestimuladoras/coinhibitorias. Se expresa constitutivamente en una variedad de células, incluyendo células presentadoras de antígenos (APCs) como macrófagos y células dendríticas, células endoteliales, células epiteliales y, de manera crítica, en muchas células tumorales.
La expresión de PD-L1 puede ser inducida o aumentada por señales inflamatorias, particularmente por citocinas como el interferón gamma (IFN-γ), que es producido por los linfocitos T activados. Esta inducción es un mecanismo de retroalimentación negativa: cuando los linfocitos T están muy activos y producen IFN-γ para combatir una infección, este IFN-γ induce PD-L1 en las células circundantes (incluidas las propias células T, APCs y, lamentablemente, células tumorales), lo que a su vez frena la respuesta T, evitando una hiperinflamación.
Por otro lado, su compañero, el receptor PD-1 (CD279), se expresa principalmente en los linfocitos T activados (CD4+ y CD8+), linfocitos B, células NK y monocitos. Cuando PD-L1 se une a PD-1, activa una cascada de señalización intracelular que recluta fosfatasas como SHP-2 (fosfatasa que contiene dominios de homología SH2). SHP-2 desfosforila proteínas clave involucradas en la activación del receptor de células T (TCR), como ZAP70 y CD3, lo que resulta en la inhibición de la proliferación, la producción de citocinas (como IL-2 e IFN-γ) y la supervivencia de los linfocitos T. Este proceso puede llevar a la anergia T (inactivación funcional) o al agotamiento de linfocitos T, un estado de disfunción que los hace incapaces de eliminar eficazmente las células infectadas o cancerosas.
La Evasión Tumoral: Cuando el Cáncer Secuestra un Mecanismo Vital
La astucia evolutiva del cáncer se manifiesta en su capacidad para subvertir los mecanismos de defensa del huésped. En el caso de PD-L1, las células tumorales han aprendido a sobreexpresar esta molécula en su superficie. Al hacerlo, presentan una ‘señal de alto’ constante a los linfocitos T infiltrantes que intentan reconocerlas y destruirlas. Es como si el tumor se vistiera con un chaleco de invisibilidad inmunológica.
La sobreexpresión de PD-L1 en las células tumorales se produce a través de diversos mecanismos. Puede ser impulsada por señalización oncogénica intrínseca dentro de la propia célula cancerosa (por ejemplo, mutaciones en genes como EGFR o ALK), o puede ser una respuesta adaptativa al microambiente tumoral. En este último escenario, los linfocitos T infiltrantes que reconocen el tumor liberan IFN-γ, que, paradójicamente, induce la expresión de PD-L1 en las células tumorales. Esto crea un ciclo de retroalimentación negativa que protege al tumor del ataque inmune, un fenómeno conocido como resistencia inmune adaptativa.
El resultado es la creación de un microambiente tumoral inmunosupresor, donde los linfocitos T antitumorales se vuelven anérgicos o agotados, incapaces de montar una respuesta efectiva. Esta estrategia de evasión es una de las principales razones por las que el sistema inmune, a pesar de su sofisticación, a menudo falla en eliminar el cáncer de forma espontánea. La comprensión de este secuestro de PD-L1 ha sido una de las mayores revelaciones en la oncología moderna, abriendo la puerta a nuevas y revolucionarias estrategias terapéuticas.
Biohacking Inmune: El Poder de la Diversidad Microbiótica. Un intestino sano, rico en una microbiota diversa, puede modular positivamente la respuesta inmune sistémica. Ciertos perfiles microbianos se han asociado con una mejor respuesta a las inmunoterapias contra el cáncer. Considera alimentos fermentados y una dieta rica en fibra para nutrir tu ecosistema interno y fortalecer tus defensas naturales.
Inmunoterapia: Despertando al Centinela Inmune
La identificación del eje PD-1/PD-L1 como un punto de control crucial en la evasión tumoral llevó al desarrollo de una nueva clase de fármacos: los inhibidores de puntos de control inmunes (ICIs). Estos fármacos, que incluyen anticuerpos monoclonales que bloquean la interacción entre PD-1 y PD-L1, han transformado radicalmente el panorama del tratamiento del cáncer.
Existen dos tipos principales de ICIs dirigidos a este eje: los anti-PD-1 (como pembrolizumab y nivolumab) y los anti-PD-L1 (como atezolizumab, durvalumab y avelumab). Ambos actúan de manera similar: al bloquear la unión de PD-L1 a PD-1, estos fármacos liberan los ‘frenos’ de los linfocitos T, permitiéndoles reactivarse, proliferar y reconocer y destruir eficazmente las células cancerosas. Es como quitar el pie del freno y pisar el acelerador del sistema inmune.
La eficacia de estas terapias ha sido demostrada en una amplia gama de cánceres, incluyendo melanoma, cáncer de pulmón de células no pequeñas, cáncer de riñón, cáncer de vejiga, linfoma de Hodgkin, y muchos otros. Para muchos pacientes, estos tratamientos han ofrecido una esperanza sin precedentes, logrando remisiones duraderas e incluso curaciones en casos que antes eran intratables. La expresión de PD-L1 en las células tumorales o en las células inmunes infiltrantes es un biomarcador predictivo clave, utilizado para seleccionar a los pacientes que tienen más probabilidades de responder a estas terapias, aunque su interpretación no está exenta de desafíos.
Desafíos y Perspectivas: La Complejidad de PD-L1 como Biomarcador
A pesar de su éxito, la utilización de PD-L1 como biomarcador para predecir la respuesta a la inmunoterapia es compleja y presenta varios desafíos. Uno de los principales es la heterogeneidad de la expresión de PD-L1. La expresión puede variar no solo entre diferentes tipos de cáncer, sino también dentro del mismo tumor (heterogeneidad espacial) y a lo largo del tiempo (heterogeneidad temporal) debido a la dinámica del microambiente tumoral y la presión de selección inmune. Esto significa que una biopsia de una pequeña sección del tumor podría no reflejar la expresión general de PD-L1 en todo el cáncer.
Otro desafío reside en la estandarización de las pruebas. La detección de PD-L1 se realiza comúnmente mediante ensayos de inmunohistoquímica (IHC). Sin embargo, existen múltiples anticuerpos clonales (22C3, 28-8, SP142, SP263, entre otros) y plataformas de tinción, cada una con sus propios criterios de puntuación, umbrales de positividad y patrones de tinción (en células tumorales, células inmunes o ambas). Esta falta de armonización puede llevar a resultados inconsistentes y dificultar la comparación entre estudios y la toma de decisiones clínicas.
Además, no todos los pacientes con tumores PD-L1 positivos responden a la inmunoterapia, y algunos pacientes con tumores PD-L1 negativos sí lo hacen. Esto sugiere que PD-L1, aunque útil, no es el único factor determinante de la respuesta y que otros biomarcadores (como la carga mutacional tumoral, la inestabilidad microsatelital o la composición del microambiente inmune) también juegan un papel crucial. La investigación actual se enfoca en identificar combinaciones de biomarcadores y en desarrollar nuevas estrategias terapéuticas que superen la resistencia a la inmunoterapia.
Alerta Médica: No Todas las Inmunoterapias son Iguales. Aunque los inhibidores de puntos de control inmunes han revolucionado el tratamiento del cáncer, no están exentos de efectos secundarios. Estos ‘eventos adversos relacionados con el sistema inmune’ (irAEs) pueden afectar cualquier órgano y requieren un manejo especializado. Nunca te automediques ni interpretes los resultados de PD-L1 sin la guía de un oncólogo cualificado.
Conclusiones: Un Pilar Fundamental en la Inmunooncología
El ligando de muerte programada 1 (PD-L1) es mucho más que una simple molécula; es un actor central en la intrincada obra de la inmunidad y un protagonista en la batalla contra el cáncer. Su papel dual, como guardián de la tolerancia inmunológica y como facilitador de la evasión tumoral, lo convierte en un objetivo terapéutico de inmenso valor.
Desde su descubrimiento, PD-L1 ha abierto las puertas a una era de inmunooncología, donde el sistema inmune del paciente es movilizado para combatir la enfermedad. Aunque persisten desafíos en su aplicación como biomarcador, la investigación continua promete refinar nuestra comprensión y optimizar su uso, acercándonos cada vez más a la era de la medicina de precisión en el tratamiento del cáncer. Su estudio sigue siendo un campo vibrante y esencial para el avance de la medicina, ofreciendo nuevas esperanzas a millones de personas en todo el mundo.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.