Complejo de Ataque a la Membrana (MAC): Guía Definitiva
Resumen Clínico Rápido
🔬 Clasificación
Complejo Proteico Terminal
⚙️ Función
Lisis de Patógenos
📋 Impacto
Inmunidad Innata y Enfermedad
El Complejo de Ataque a la Membrana (MAC): Un Arma Molecular de Precisión en la Inmunidad Innata
En el vasto y complejo universo de la inmunología humana, existen mecanismos de defensa tan sofisticados que su diseño parece casi de ciencia ficción. Entre estos, el Complejo de Ataque a la Membrana (MAC, por sus siglas en inglés, Membrane Attack Complex) destaca como una de las armas más potentes y directas de nuestro sistema inmune innato. Formando parte integral del sistema del complemento, el MAC es una estructura proteica polimérica diseñada con un propósito singular y devastador: perforar la membrana de células patógenas, llevándolas a la lisis y, en última instancia, a su destrucción. Esta guía exhaustiva explorará en profundidad la fisiología molecular del MAC, su propósito evolutivo, su formación, regulación y su impacto crucial en la salud y la enfermedad.
Resumen Clínico: Puntos Clave del MAC
- El Complejo de Ataque a la Membrana (MAC) es un componente terminal del sistema del complemento, vital para la inmunidad innata.
- Se ensambla en la superficie de patógenos, formando un poro transmembrana que provoca la lisis osmótica y muerte celular.
- Compuesto por proteínas C5b, C6, C7, C8 y múltiples moléculas de C9, su formación está estrictamente regulada para proteger las células del huésped.
Un sistema inmune 'potenciado' siempre es mejor para la salud.
Un sistema inmune debe ser equilibrado. La sobreactivación, como la del MAC, puede causar daño autoinmune grave, como en la Hemoglobinuria Paroxística Nocturna, demostrando que la regulación es tan vital como la capacidad de respuesta.
Propósito Evolutivo: La Defensa Primaria contra Invasores
El sistema del complemento, del cual el MAC es la culminación, es una de las ramas más antiguas y conservadas de la inmunidad. Su propósito evolutivo es claro: proporcionar una línea de defensa rápida y eficaz contra una amplia gama de patógenos, especialmente bacterias gramnegativas, virus envueltos, hongos y parásitos. La capacidad de identificar y neutralizar amenazas sin necesidad de una exposición previa o de una memoria inmunológica es lo que define la inmunidad innata, y el MAC es un testimonio de la brillantez de esta estrategia.
Desde una perspectiva evolutiva, la lisis directa de patógenos mediante la formación de poros es una solución elegante y eficiente. Antes del desarrollo de sistemas inmunes adaptativos más complejos en vertebrados, organismos unicelulares y multicelulares primitivos ya poseían mecanismos similares para defenderse de agresores microbianos. El MAC representa la sofisticación de esta estrategia, permitiendo una eliminación rápida que puede ser crucial en las etapas iniciales de una infección, limitando la replicación y diseminación del patógeno antes de que el sistema inmune adaptativo pueda montar una respuesta más específica.
Fisiología Molecular: El Ensamblaje de un Arma Letal
La formación del MAC es el resultado final de la activación de una de las tres vías del sistema del complemento: la vía clásica, la vía de la lectina o la vía alternativa. Aunque los mecanismos iniciales de activación difieren, todas convergen en la formación de una C5 convertasa, una enzima clave que escinde la proteína C5 en C5a y C5b.
Los Componentes del MAC
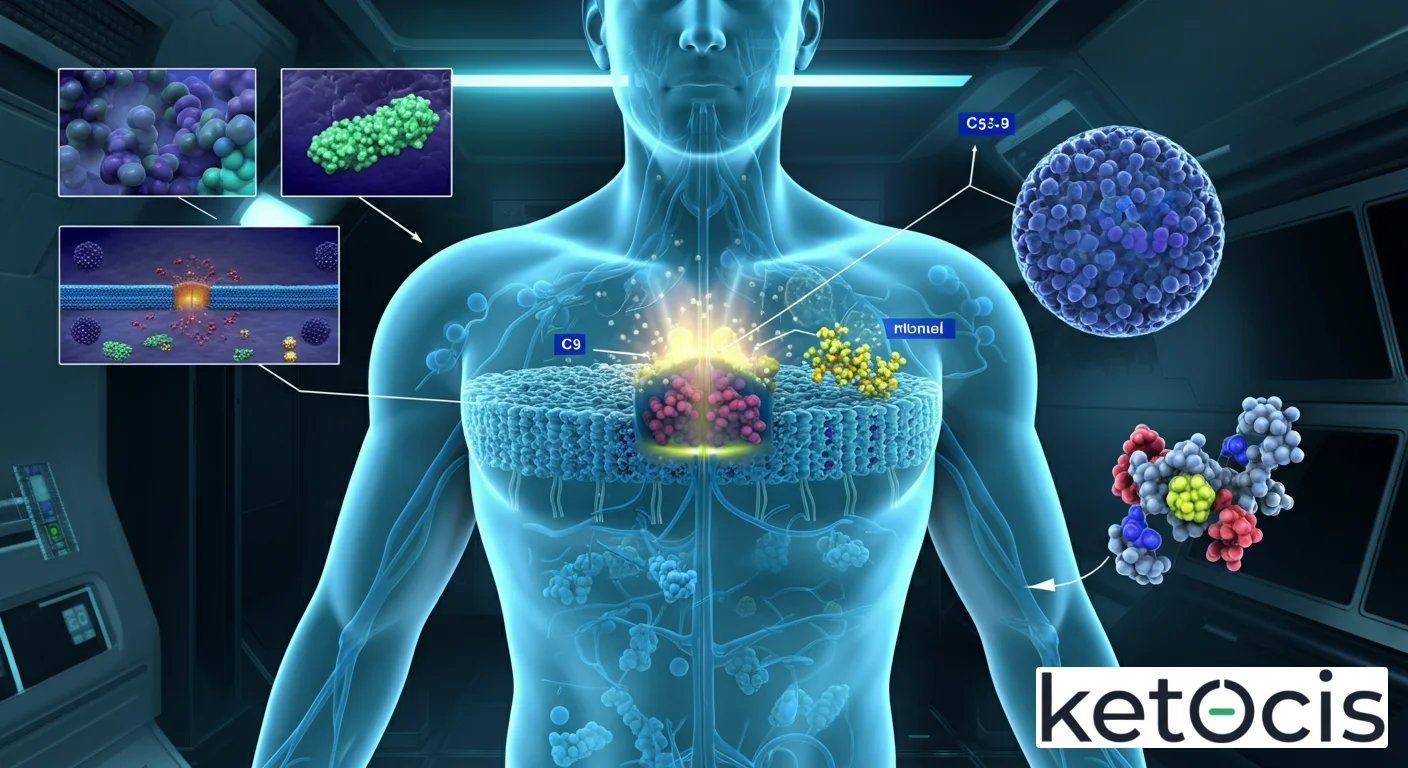
El MAC está compuesto por cinco proteínas del complemento: C5b, C6, C7, C8 y múltiples unidades de C9. Cada una juega un papel secuencial y esencial en el ensamblaje:
- C5b: El Núcleo Iniciador
Una vez generada por la C5 convertasa, la C5b es una molécula inestable que rápidamente se une a la superficie del patógeno. Esta unión es crítica, ya que sirve como plataforma para el reclutamiento de las siguientes proteínas. - C6 y C7: Anclaje a la Membrana
C6 se une a C5b, formando el complejo C5bC6. Posteriormente, C7 se une a este complejo (C5bC6C7). La adición de C7 induce un cambio conformacional que expone una región hidrofóbica en C7, permitiendo que el complejo C5bC6C7 se inserte firmemente en la bicapa lipídica de la membrana del patógeno. Este paso es el anclaje inicial del futuro poro. - C8: La Perforación Inicial
El complejo C5bC6C7 sirve entonces como sitio de unión para C8. C8 es una proteína trimérica compuesta por subunidades alfa, beta y gamma. La subunidad beta de C8 se une al complejo C5bC6C7, mientras que las subunidades alfa y gamma tienen la capacidad de insertarse en la membrana del patógeno. Esta inserción inicial de C8 ya crea un pequeño poro en la membrana, permitiendo una fuga limitada de iones y moléculas. - C9: La Polimerización y el Poro Definitivo
El complejo C5bC6C7C8 es ahora capaz de catalizar la polimerización de múltiples moléculas de C9. C9 es estructuralmente similar a la perforina, otra proteína formadora de poros del sistema inmune. Hasta 18 moléculas de C9 pueden unirse al complejo C5bC6C7C8, polimerizándose en una estructura anular que forma un gran canal transmembrana. Este canal, con un diámetro de aproximadamente 100 Å (10 nm), es lo suficientemente grande como para permitir el paso incontrolado de agua, iones y pequeñas moléculas, interrumpiendo catastróficamente la homeostasis osmótica de la célula patógena.
El resultado final es la lisis osmótica: el agua fluye hacia el interior de la célula patógena, que se hincha y estalla, llevando a su destrucción. Este proceso es increíblemente rápido y eficiente, proporcionando una defensa de primera línea contra una variedad de amenazas.
Regulación del MAC: Protegiendo al Huésped
La capacidad del MAC para destruir membranas celulares plantea una pregunta crucial: ¿cómo se asegura el cuerpo de que este potente mecanismo no dañe sus propias células? La respuesta reside en un sofisticado sistema de proteínas reguladoras que operan tanto en la fase fluida como en la superficie de las células del huésped. Esta regulación estricta es esencial para prevenir el daño autoinmune.
- Proteína S (Vitronectina): En la fase fluida, la proteína S (también conocida como vitronectina) se une a los complejos C5bC6C7 que no se han insertado en una membrana. Esta unión previene su inserción en las membranas de las células sanas del huésped, neutralizando su potencial citolítico.
- CD59 (Proteína Protectora de la Membrana): Una de las reguladoras más importantes es la CD59, una proteína anclada a la membrana de las células del huésped mediante un glicosilfosfatidilinositol (GPI). CD59 actúa uniéndose a C8 y C9 durante el ensamblaje del MAC, inhibiendo la polimerización de C9 y, por lo tanto, la formación de un poro funcional. Es un freno molecular directo que protege nuestras propias células.
- Homólogo de Proteína Restrictora (HRF) o CD59-like: Similar a CD59, el HRF también puede inhibir la polimerización de C9.
La interrupción de estos mecanismos reguladores puede tener consecuencias graves, como se observa en enfermedades donde el MAC ataca las propias células del organismo.
Biohacking Inmunológico: La Conexión Inesperada
Aunque el Complejo de Ataque a la Membrana opera a nivel molecular, su eficacia puede ser influenciada indirectamente por el estado metabólico general. Por ejemplo, se ha observado que la deficiencia de ciertos micronutrientes, como el zinc o la vitamina D, puede comprometer la función inmunitaria general. Mantener una salud metabólica óptima a través de estrategias como la dieta cetogénica o el ayuno intermitente puede potenciar la resiliencia celular y la integridad de las membranas, creando un entorno menos propicio para la proliferación patógena y, por ende, reduciendo la carga sobre el sistema del complemento. ¡Un cuerpo bien nutrido y metabólicamente flexible es un cuerpo con defensas más robustas!
Impacto en la Salud y la Enfermedad: Un Doble Filo
La actividad del MAC es una espada de doble filo. Es esencial para la defensa contra infecciones, pero su desregulación puede conducir a enfermedades autoinmunes y daño tisular.
Beneficios Clínicos: Lucha contra las Infecciones
La función principal del MAC es la eliminación directa de patógenos. Las personas con deficiencias congénitas en cualquiera de los componentes terminales del complemento (C5-C9) son particularmente susceptibles a infecciones recurrentes por bacterias encapsuladas, especialmente especies de Neisseria (como Neisseria meningitidis y Neisseria gonorrhoeae). Esto subraya la importancia crítica del MAC en la protección contra estos patógenos específicos que han desarrollado estrategias para evadir otros brazos del sistema inmune.
Además de la lisis directa, el daño a la membrana causado por el MAC puede hacer que los patógenos sean más susceptibles a la fagocitosis y a la acción de antibióticos. También puede liberar antígenos patógenos que estimulan la respuesta inmune adaptativa, sirviendo como un puente entre la inmunidad innata y adaptativa.
Patologías Asociadas a la Disfunción del MAC
La desregulación del MAC puede tener consecuencias devastadoras:
- Hemoglobinuria Paroxística Nocturna (HPN): Esta es quizás la enfermedad más conocida asociada a la disfunción del MAC. En la HPN, los glóbulos rojos carecen de proteínas ancladas a GPI, incluyendo CD59 y DAF (Factor Acelerador de la Decadencia, otro regulador del complemento). Sin estos protectores, los glóbulos rojos son vulnerables al ataque del MAC, lo que lleva a una hemólisis crónica y anemia. Los tratamientos modernos para la HPN, como el eculizumab, son anticuerpos monoclonales que bloquean C5, previniendo así la formación del MAC.
- Glomerulonefritis Membranoproliferativa (GNMP) y Enfermedad de Depósito de Componentes Densos (DDD): En estas enfermedades renales, la activación descontrolada del complemento, incluyendo la formación del MAC, contribuye al daño glomerular y a la insuficiencia renal.
- Rechazo de Trasplantes: En el rechazo hiperagudo y agudo mediado por anticuerpos, el MAC juega un papel central en la destrucción de los tejidos trasplantados.
- Esclerosis Múltiple: Se ha sugerido que el MAC contribuye al daño de la mielina en enfermedades neurodegenerativas como la esclerosis múltiple, atacando las células oligodendrocíticas y neuronas.
Alerta Médica: El Peligro de la Activación Incontrolada
La activación descontrolada o inapropiada del sistema del complemento, y por ende del Complejo de Ataque a la Membrana, es un factor crítico en la patogénesis de numerosas enfermedades autoinmunes e inflamatorias. Un ataque del MAC a las propias células del organismo puede desencadenar un daño tisular masivo e irreversible. Es crucial entender que, si bien la inflamación es una respuesta protectora, la inflamación crónica o desregulada impulsada por un complemento hiperactivo puede ser extremadamente destructiva. Nunca subestimes la importancia de un sistema inmune equilibrado; la sobreactivación es tan peligrosa como la deficiencia. Consulta siempre a un profesional de la salud ante síntomas de disfunción inmunitaria.
Mitos y Realidades del MAC
Mito Popular Falso: El sistema inmune es una entidad única que siempre funciona de manera coordinada para protegernos, y si lo ‘potenciamos’ indiscriminadamente, siempre será mejor.
Explicación Científica: Esta afirmación es una simplificación peligrosa. El sistema inmune es una red intrincada de componentes, como el MAC, que deben estar finamente regulados. Un ‘potenciamiento’ indiscriminado puede llevar a la sobreactivación de ciertas vías, como la del complemento, resultando en un ataque a las propias células del huésped. Enfermedades autoinmunes y condiciones como la HPN demuestran que un sistema inmune hiperactivo o desregulado puede ser tan dañino como uno deficiente. La clave no es ‘potenciar’, sino mantener el equilibrio y la homeostasis, asegurando que cada componente, incluido el MAC, actúe de manera apropiada y controlada.
Conclusión: El MAC como Pilar de la Inmunidad
El Complejo de Ataque a la Membrana es una maravilla de la ingeniería biológica, un arma molecular de precisión que representa la culminación de una de las vías de defensa más antiguas y potentes del cuerpo. Su capacidad para perforar y destruir patógenos de manera rápida y eficiente es fundamental para nuestra supervivencia. Sin embargo, la sofisticación de su mecanismo se equilibra con una regulación igualmente intrincada, diseñada para proteger nuestras propias células de su poder destructivo.
La comprensión del MAC no solo profundiza nuestro aprecio por la complejidad del sistema inmune, sino que también abre puertas a nuevas estrategias terapéuticas para enfermedades donde el complemento juega un papel central. Desde el desarrollo de fármacos que inhiben su formación hasta la manipulación de sus reguladores, la investigación continua sobre el MAC promete mejorar la vida de millones de personas afectadas por trastornos inmunes e infecciosos. Es un testimonio de que, en la biología, la elegancia y la letalidad pueden coexistir en una misma y fascinante estructura.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.