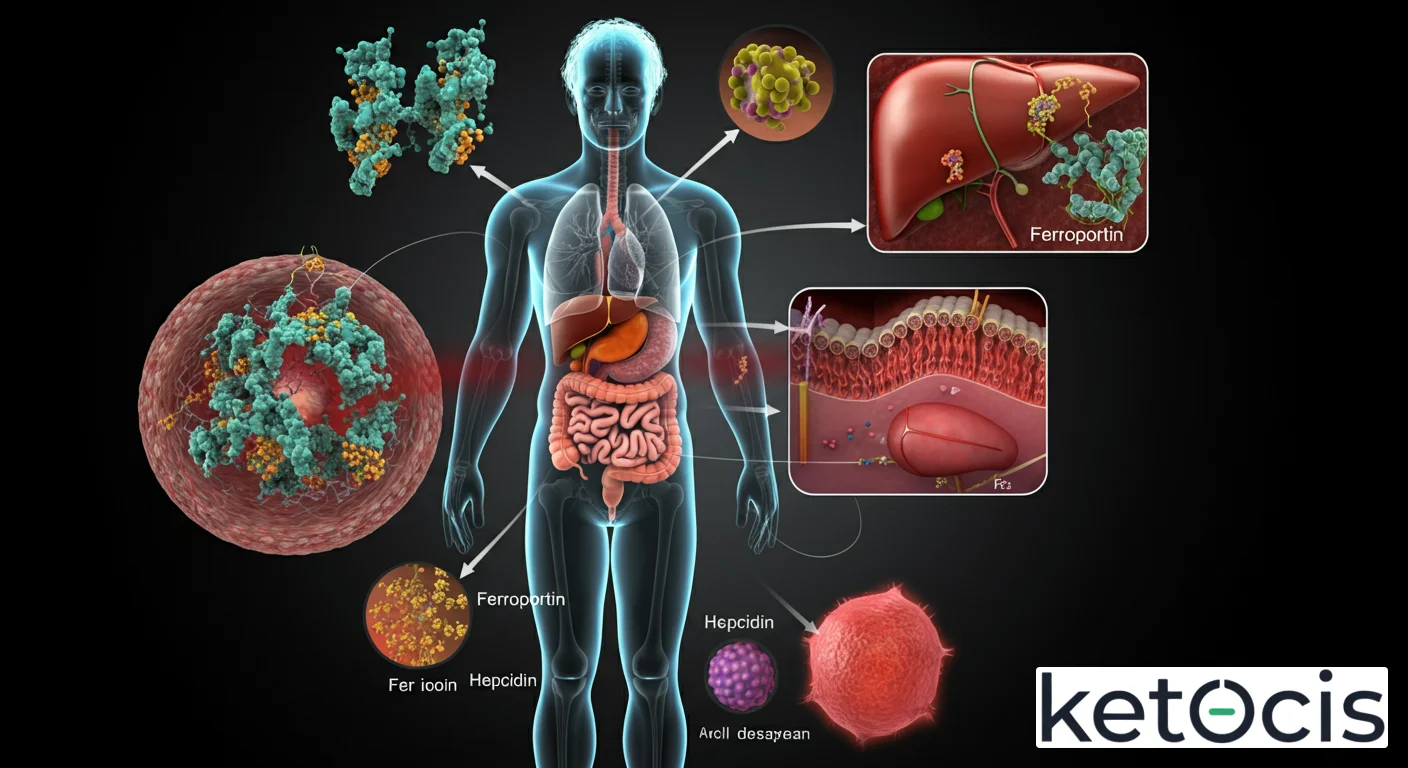
Ferroportina: El Guardián del Hierro Celular y su Rol Metabólico
Resumen Clínico Rápido
🔬 Clasificación
Proteína transmembrana, transportador de eflujo (SLC40A1)
⚙️ Función
Única exportadora celular de hierro, crucial para la homeostasis sistémica
📋 Impacto
Regulación de absorción, reciclaje y almacenamiento de hierro; implicada en anemias y hemocromatosis
Ferroportina: El Guardián Molecular del Hierro en la Homeostasis Metabólica
En el intrincado universo de la biología humana, donde cada molécula desempeña un papel vital, la ferroportina emerge como un actor central en uno de los procesos más fundamentales para la vida: la homeostasis del hierro. Este metal de transición, esencial para funciones como el transporte de oxígeno, la respiración celular y la síntesis de ADN, es también un potente pro-oxidante si se encuentra en exceso. La delicada balanza entre la suficiencia y la toxicidad del hierro es mantenida por una red de proteínas finamente reguladas, y en el epicentro de esta red se encuentra la ferroportina (FPN1 o SLC40A1), la única proteína conocida capaz de exportar hierro desde el interior de las células hacia el torrente sanguíneo. Su descubrimiento revolucionó nuestra comprensión de cómo el cuerpo gestiona este metal crucial, abriendo nuevas vías para el diagnóstico y tratamiento de trastornos relacionados con el hierro.
La ferroportina no es simplemente un canal pasivo; es un sofisticado regulador cuya actividad está meticulosamente controlada por señales sistémicas y celulares, siendo la hepcidina, una hormona peptídica, su principal antagonista. Comprender la ferroportina es adentrarse en la complejidad de la fisiología del hierro, un viaje que revela conexiones profundas con la inflamación, la eritropoyesis, el metabolismo energético y, sorprendentemente, con estados metabólicos como la cetosis y el ayuno. Esta guía exhaustiva explorará su origen, estructura, mecanismo de acción, regulación, implicaciones patológicas y el fascinante vínculo con la optimización metabólica, proporcionando una visión definitiva para el Glosario Ketocis.
Resumen Clínico
-
La ferroportina (FPN1) es la única proteína transmembrana conocida capaz de exportar hierro desde el interior de las células hacia la circulación sanguínea, siendo crucial para la homeostasis sistémica del hierro.
-
Su función es vital en enterocitos (absorción de hierro dietético), macrófagos (reciclaje de hierro de eritrocitos senescentes) y hepatocitos (liberación de hierro almacenado).
-
La actividad de la ferroportina está principalmente regulada por la hormona peptídica hepcidina, que induce su internalización y degradación, reduciendo la exportación de hierro y previniendo su sobrecarga.
Origen y Estructura Molecular de la Ferroportina
La ferroportina, también conocida como Solute Carrier Family 40 Member 1 (SLC40A1), es una proteína transmembrana altamente conservada a lo largo de la evolución, lo que subraya su importancia biológica fundamental. Se expresa en una variedad de tipos celulares clave para el metabolismo del hierro, incluyendo los enterocitos del duodeno (donde el hierro dietético es absorbido), los macrófagos del sistema reticuloendotelial (que reciclan el hierro de los eritrocitos viejos), los hepatocitos (el principal sitio de almacenamiento y regulación del hierro), y células placentarias, entre otras. Esta distribución estratégica asegura una gestión integral del hierro en todo el organismo.
Estructuralmente, la ferroportina es una proteína multipaso que atraviesa la membrana celular aproximadamente doce veces, formando un canal o poro a través del cual el hierro ferroso (Fe2+) puede ser transportado. Su dominio N-terminal y C-terminal se encuentran en el citoplasma. La exportación de Fe2+ a través de la ferroportina es facilitada por la acción de ferroxidasas extracelulares, como la hefaestina en los enterocitos y la ceruloplasmina en los macrófagos y hepatocitos. Estas enzimas oxidan el Fe2+ a hierro férrico (Fe3+) una vez que sale de la célula, permitiéndole unirse a la transferrina en el plasma para su transporte seguro y eficiente. Sin esta oxidación, el hierro férrico sería insoluble y tóxico.
El hierro es siempre bueno en grandes cantidades y suplementar es siempre beneficioso.
El exceso de hierro es tóxico, generando estrés oxidativo y daño tisular. La suplementación solo debe realizarse bajo indicación médica tras confirmar una deficiencia, ya que la ferroportina y la hepcidina regulan estrictamente su disponibilidad para evitar la sobrecarga.
Mecanismo de Acción: El Exportador Esencial de Hierro
El mecanismo de acción de la ferroportina es un ejemplo exquisito de transporte facilitado que opera en un contexto de regulación estricta. Dentro de la célula, el hierro que no es inmediatamente utilizado se almacena en la ferritina, o se dirige hacia la mitocondria para la síntesis de grupos hemo y clústeres de hierro-azufre. Sin embargo, cuando los niveles intracelulares de hierro son elevados o el organismo requiere hierro para la eritropoyesis, la ferroportina se activa para liberar este metal al torrente sanguíneo. La proteína actúa como un eflujo transportador, moviendo el hierro desde el citoplasma, donde su exceso podría generar estrés oxidativo, hacia el espacio extracelular.
La eficiencia de la ferroportina es crucial. En los enterocitos, por ejemplo, la absorción del hierro dietético se produce principalmente a través del transportador de metales divalentes 1 (DMT1) en la membrana apical. Una vez dentro, el hierro debe ser exportado por la ferroportina en la membrana basolateral para entrar en la circulación. De manera similar, los macrófagos, que fagocitan y degradan eritrocitos senescentes, liberan el hierro recuperado de la hemoglobina a través de la ferroportina para que sea reutilizado. La coordinación entre la ferroportina y las ferroxidasas es fundamental: la ferroportina exporta Fe2+, y la ferroxidasa inmediatamente lo oxida a Fe3+, creando un gradiente electroquímico que favorece la salida continua de hierro y su posterior unión a la transferrina.
Regulación de la Ferroportina: La Danza con la Hepcidina
La ferroportina no opera de forma aislada; su actividad está finamente sintonizada por una compleja red de señales reguladoras, siendo la hepcidina la más prominente y poderosa. La hepcidina es una hormona peptídica de 25 aminoácidos, sintetizada principalmente por el hígado, que actúa como el principal regulador negativo de la ferroportina. Su descubrimiento, y la dilucidación de su mecanismo de acción, transformó nuestra comprensión de la fisiología del hierro.
Cuando los niveles de hierro en el cuerpo son elevados o hay inflamación, el hígado aumenta la producción de hepcidina. Esta hormona se une a la ferroportina en la superficie celular, desencadenando su internalización y posterior degradación lisosomal. Al eliminar la ferroportina de la membrana plasmática, la hepcidina bloquea la exportación de hierro desde los enterocitos, macrófagos y hepatocitos, lo que resulta en una menor absorción de hierro dietético, una reducción en la liberación de hierro reciclado y una mayor retención de hierro intracelular. Este mecanismo previene la sobrecarga de hierro y protege al cuerpo de su toxicidad.
Por el contrario, en situaciones de deficiencia de hierro, anemia o aumento de la eritropoyesis (cuando se necesita más hierro para producir glóbulos rojos), la producción de hepcidina disminuye. Esto permite que la ferroportina permanezca en la superficie celular, facilitando la exportación de hierro y aumentando su disponibilidad sistémica. Factores como la hipoxia, las infecciones bacterianas y diversas citocinas inflamatorias (como la IL-6) también influyen en la expresión de hepcidina, lo que explica por qué la inflamación crónica a menudo conduce a la anemia de la enfermedad crónica, donde el hierro se secuestra dentro de las células.
Ferroportina en la Homeostasis Sistémica del Hierro y Patologías
La función de la ferroportina es indispensable para mantener la homeostasis del hierro a nivel sistémico. Su expresión diferencial y su regulación por la hepcidina son críticas para el equilibrio. En los enterocitos duodenales, la ferroportina media la liberación de hierro absorbido de la dieta. En los macrófagos, facilita el reciclaje del hierro de los eritrocitos viejos, un proceso que recicla aproximadamente 20-25 mg de hierro al día, la mayor parte del hierro necesario para la eritropoyesis. En los hepatocitos, la ferroportina contribuye a la liberación de hierro almacenado según las demandas del organismo.
Las disfunciones en la ferroportina o en su regulación tienen profundas implicaciones clínicas:
Hemocromatosis Tipo 4 (Enfermedad de Ferroportina)
Las mutaciones en el gen SLC40A1 que codifica la ferroportina pueden dar lugar a una forma de hemocromatosis, una enfermedad de sobrecarga de hierro. Existen dos tipos principales de mutaciones:
-
Mutaciones de ‘pérdida de función’ (Loss-of-function): Estas mutaciones impiden que la ferroportina exporte hierro de manera eficiente o que sea correctamente regulada por la hepcidina. El hierro se acumula dentro de los macrófagos y hepatocitos, pero los niveles de hierro sérico pueden ser normales o incluso bajos, lo que confunde el diagnóstico. Los síntomas son similares a otras hemocromatosis, pero el patrón de acumulación de hierro es distinto.
-
Mutaciones de ‘ganancia de función’ (Gain-of-function): Más raras, estas mutaciones hacen que la ferroportina sea resistente a la degradación por hepcidina. El resultado es una liberación excesiva de hierro de las células, llevando a una sobrecarga sistémica de hierro con niveles elevados de hierro sérico y ferritina, similar a la hemocromatosis hereditaria clásica.
Anemia de la Enfermedad Crónica (Anemia de la Inflamación)
En condiciones inflamatorias crónicas (como infecciones crónicas, enfermedades autoinmunes o cáncer), la inflamación eleva los niveles de hepcidina. La hepcidina, a su vez, degrada la ferroportina en macrófagos y enterocitos, secuestrando el hierro dentro de estas células y reduciendo su disponibilidad para la eritropoyesis. Esto conduce a una anemia funcional por deficiencia de hierro, a pesar de que el cuerpo puede tener reservas adecuadas de hierro. La ferroportina es, por lo tanto, un objetivo terapéutico clave para revertir esta forma común de anemia.
Otros Trastornos
La disfunción de la ferroportina también se ha relacionado con otras condiciones, incluyendo trastornos neurodegenerativos donde la desregulación del hierro juega un papel, y ciertos tipos de cáncer, donde las células tumorales pueden manipular el metabolismo del hierro para su proliferación.
Biohacking del Hierro: La Sincronización Circadiana
¿Sabías que la absorción y el metabolismo del hierro tienen un ritmo circadiano? La hepcidina, el regulador clave de la ferroportina, muestra fluctuaciones diarias, con niveles más bajos por la mañana y más altos por la tarde. Optimizar tu ingesta de hierro (si es necesaria) en las primeras horas del día podría alinearse mejor con este ritmo natural, potencialmente mejorando su biodisponibilidad y reduciendo la activación de la hepcidina, que es más activa por la noche, lo que podría limitar la exportación de hierro.
Ferroportina en Estados Metabólicos: Cetosis y Ayuno
La interacción entre la ferroportina y los estados metabólicos como la cetosis y el ayuno es un área de investigación emergente y fascinante. Aunque la relación directa no siempre es lineal, podemos inferir conexiones significativas a través de los mecanismos que modulan la inflamación y el estrés oxidativo, factores que influyen directamente en la expresión de hepcidina y, por ende, en la actividad de la ferroportina.
El ayuno y las dietas cetogénicas son conocidos por sus efectos antiinflamatorios. La reducción de la inflamación sistémica, mediada por la disminución de citocinas proinflamatorias como la IL-6, podría teóricamente conducir a una disminución en la producción de hepcidina. Una hepcidina más baja permitiría que la ferroportina permanezca más tiempo en la superficie celular, facilitando una mayor exportación de hierro. Esto podría ser beneficioso en contextos donde el hierro está secuestrado, como en ciertas anemias por inflamación crónica.
Además, el ayuno intermitente y la cetosis promueven la autofagia, un proceso de limpieza celular que recicla componentes dañados. La autofagia puede influir en la gestión intracelular del hierro al degradar proteínas que contienen hierro o al modular la expresión de proteínas relacionadas con el hierro. Una mejor gestión del hierro intracelular podría, a su vez, impactar las señales que regulan la ferroportina. También, el metabolismo de los cuerpos cetónicos podría influir en el estado redox celular, lo que podría tener implicaciones indirectas en la regulación del hierro.
Es importante señalar que, si bien estos mecanismos sugieren una interacción, la investigación específica sobre la ferroportina en el contexto de la cetosis y el ayuno aún está en desarrollo. Sin embargo, la mejora en la sensibilidad a la insulina y la reducción del estrés oxidativo, características de estos estados metabólicos, son condiciones que, en general, favorecen una homeostasis más equilibrada del hierro.
Optimización y Estrategias: Manteniendo el Equilibrio del Hierro
Dada la importancia de la ferroportina en la homeostasis del hierro, su optimización no se trata de manipular directamente esta proteína, sino de mantener un equilibrio sistémico que permita su función adecuada. Las estrategias se centran en un manejo consciente del hierro dietético y en el control de factores que influyen en su regulación.
-
Monitoreo de Hierro: Para la mayoría de las personas, una dieta equilibrada es suficiente. Sin embargo, en poblaciones de riesgo (mujeres en edad fértil, veganos/vegetarianos, personas con trastornos gastrointestinales), es crucial monitorear los niveles de ferritina, hierro sérico y transferrina. Esto permite identificar deficiencias o sobrecargas antes de que se vuelvan problemáticas.
-
Gestión de la Inflamación: Dado que la inflamación eleva la hepcidina y degrada la ferroportina, estrategias antiinflamatorias son clave. Esto incluye una dieta rica en antioxidantes (frutas, verduras, especias), ácidos grasos omega-3, un sueño adecuado y manejo del estrés. Las dietas cetogénicas, por su naturaleza antiinflamatoria, pueden contribuir indirectamente a un mejor manejo del hierro.
-
Evitar Excesos de Hierro: La sobrecarga de hierro es tan peligrosa como la deficiencia. Evitar la suplementación innecesaria de hierro es fundamental, especialmente si no hay un diagnóstico de deficiencia. El hierro heme (de productos animales) se absorbe más eficientemente que el hierro no-heme (de plantas), pero ambos deben consumirse con moderación.
-
Nutrientes Cofactores: La vitamina C mejora la absorción de hierro no-heme. El cobre es esencial para la función de las ferroxidasas (hefaestina, ceruloplasmina) que trabajan con la ferroportina. Asegurar una ingesta adecuada de estos nutrientes es importante para un metabolismo óptimo del hierro.
-
Ejercicio Físico: El ejercicio regular y moderado se asocia con un mejor perfil inflamatorio y una mejor salud metabólica general, lo que podría influir positivamente en la regulación de la hepcidina y la ferroportina.
Alerta Médica: El Riesgo Oculto de la Sobrecarga de Hierro
Existe un mito común de que “más hierro es siempre mejor” o que “nunca se puede tener demasiado hierro”. Esto es una creencia peligrosa. El hierro libre en exceso es altamente tóxico, actuando como un pro-oxidante que genera radicales libres, dañando lípidos, proteínas y ADN. Esta sobrecarga puede llevar a enfermedades hepáticas, cardíacas, diabetes, neurodegeneración y aumentar el riesgo de infecciones. La suplementación de hierro sin supervisión médica y sin una deficiencia confirmada es un riesgo metabólico significativo y debe evitarse rigurosamente. La ferroportina es nuestra principal defensa contra esta toxicidad, y su mal funcionamiento puede tener consecuencias devastadoras.
Conclusión: La Ferroportina, un Pilar de la Salud Metabólica
La ferroportina es mucho más que una simple proteína transportadora; es un guardián molecular cuya vigilancia constante asegura que el hierro, un elemento de doble filo, se mantenga en el delicado equilibrio que la vida requiere. Desde su función en la absorción y reciclaje hasta su papel central en la prevención de la toxicidad por sobrecarga, la ferroportina personifica la sofisticación de los sistemas reguladores del cuerpo.
Su intrincada relación con la hepcidina y su sensibilidad a factores como la inflamación y los estados metabólicos, como la cetosis y el ayuno, la posicionan como un objetivo de interés no solo para el tratamiento de trastornos del hierro, sino también para la comprensión de la salud metabólica en un sentido más amplio. Como investigadores y profesionales de la salud, nuestro conocimiento de la ferroportina continúa expandiéndose, revelando nuevas capas de su importancia y abriendo puertas a estrategias innovadoras para optimizar la salud humana, siempre respetando la complejidad y la sabiduría intrínseca de la biología.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.