¿Qué es el complejo principal de histocompatibilidad clase II (MHC-II) microglial? – Análisis Completo y Beneficios
Resumen Clínico Rápido
🔬 Clasificación
Glicoproteína de superficie celular
⚙️ Función
Presentación de antígenos a Linfocitos T CD4+
📋 Impacto
Neuroinmunidad, enfermedades neurodegenerativas, inflamación
El Complejo Principal de Histocompatibilidad Clase II (MHC-II) Microglial: Un Centinela Inmunológico en el Cerebro
En el vasto y enigmático universo del sistema nervioso central (SNC), la inmunidad ha sido, durante mucho tiempo, un terreno de debate y misterio. Lejos de ser un órgano inmunoprivilegiado pasivo, el cerebro alberga su propio ejército de células inmunes residentes, las
microglía. Estas células gliales son los macrófagos del cerebro, ejerciendo una vigilancia constante sobre el microambiente neural. Sin embargo, su papel se eleva a un nivel de complejidad superior cuando expresan el Complejo Principal de Histocompatibilidad Clase II (MHC-II), una maquinaria molecular crucial para la orquestación de la respuesta inmune adaptativa.
El MHC-II microglial no es una simple curiosidad biológica; es un actor fundamental en la intersección de la neuroinmunología, la neuroinflamación y la patogénesis de numerosas enfermedades neurológicas y psiquiátricas. Su expresión y función son finamente reguladas, reflejando la delicadeza con la que el cerebro gestiona su propia defensa. Comprender este complejo es desentrañar una de las claves maestras para entender cómo el cerebro se protege, se repara y, a veces, se daña a sí mismo.
Esta guía enciclopédica se adentrará en la esencia del MHC-II microglial, explorando su propósito evolutivo, su intrincada fisiología molecular y sus profundas implicaciones en la salud y la enfermedad. Desde su papel en la presentación de antígenos hasta su modulación por estados metabólicos como la cetosis, desvelaremos la ciencia detrás de este centinela inmunológico cerebral.
Resumen Clínico
- El MHC-II microglial es crucial para la presentación de antígenos en el SNC, uniendo la inmunidad innata y adaptativa.
- Su expresión es inducida por la activación microglial y citocinas proinflamatorias como el IFN-γ.
- Juega un doble papel: neuroprotección en la vigilancia y eliminación, y neuroinflamación en patologías crónicas.
Propósito Evolutivo: La Necesidad de una Inmunidad Adaptativa en el Cerebro
El concepto de un cerebro “inmunoprivilegiado” ha evolucionado significativamente. Si bien la barrera hematoencefálica (BHE) restringe el acceso de células inmunes periféricas y moléculas grandes, no aísla completamente el SNC del sistema inmune. La evolución ha dotado al cerebro de mecanismos intrínsecos para detectar y responder a amenazas, y el MHC-II microglial es un pilar central de esta estrategia.
La Microglía como Célula Presentadora de Antígenos (APC)
Desde una perspectiva evolutiva, la presencia de células capaces de presentar antígenos dentro del SNC es una adaptación crítica. En un entorno tan vital y delicado como el cerebro, la capacidad de identificar y responder a patógenos, tejidos dañados o autoantígenos de manera controlada es esencial para la supervivencia del organismo. Las microglía, con su plasticidad fenotípica y su capacidad de migración, se convirtieron en las candidatas ideales para esta función.
La expresión de MHC-II por la microglía permite al cerebro interactuar directamente con los linfocitos T CD4+ (células T helper), que son los directores de la respuesta inmune adaptativa. Esta interacción es vital para:
- Detección de Patógenos: Identificar y montar una respuesta específica contra virus, bacterias u otros agentes infecciosos que logran traspasar la BHE.
- Eliminación de Residuos: Presentar autoantígenos derivados de neuronas dañadas o detritos celulares, facilitando su eliminación y promoviendo la homeostasis.
- Vigilancia Inmunológica: Mantener una supervisión constante sobre el microambiente cerebral, asegurando que cualquier anomalía sea reconocida y abordada.
Este mecanismo asegura que el cerebro no solo tenga una primera línea de defensa (inmunidad innata microglial), sino también la capacidad de activar una respuesta inmune altamente específica y de memoria, crucial para una protección a largo plazo y la prevención de daños colaterales excesivos.
El cerebro es un órgano completamente inmunoprivilegiado y la microglía no participa activamente en la inmunidad adaptativa.
La microglía, al expresar MHC-II, actúa como célula presentadora de antígenos dentro del SNC, vinculando la inmunidad innata y adaptativa, crucial para la vigilancia y respuesta a amenazas, aunque de forma regulada.
Fisiología Molecular: El Intrincado Mecanismo del MHC-II Microglial
El MHC-II es un heterodímero de glicoproteínas de superficie celular compuesto por una cadena alfa (α) y una cadena beta (β), cada una con dos dominios extracelulares, un dominio transmembrana y una cola citoplasmática. La característica más importante de estas moléculas es su capacidad para unir y presentar fragmentos de péptidos antigénicos a los receptores de células T (TCR) de los linfocitos T CD4+.
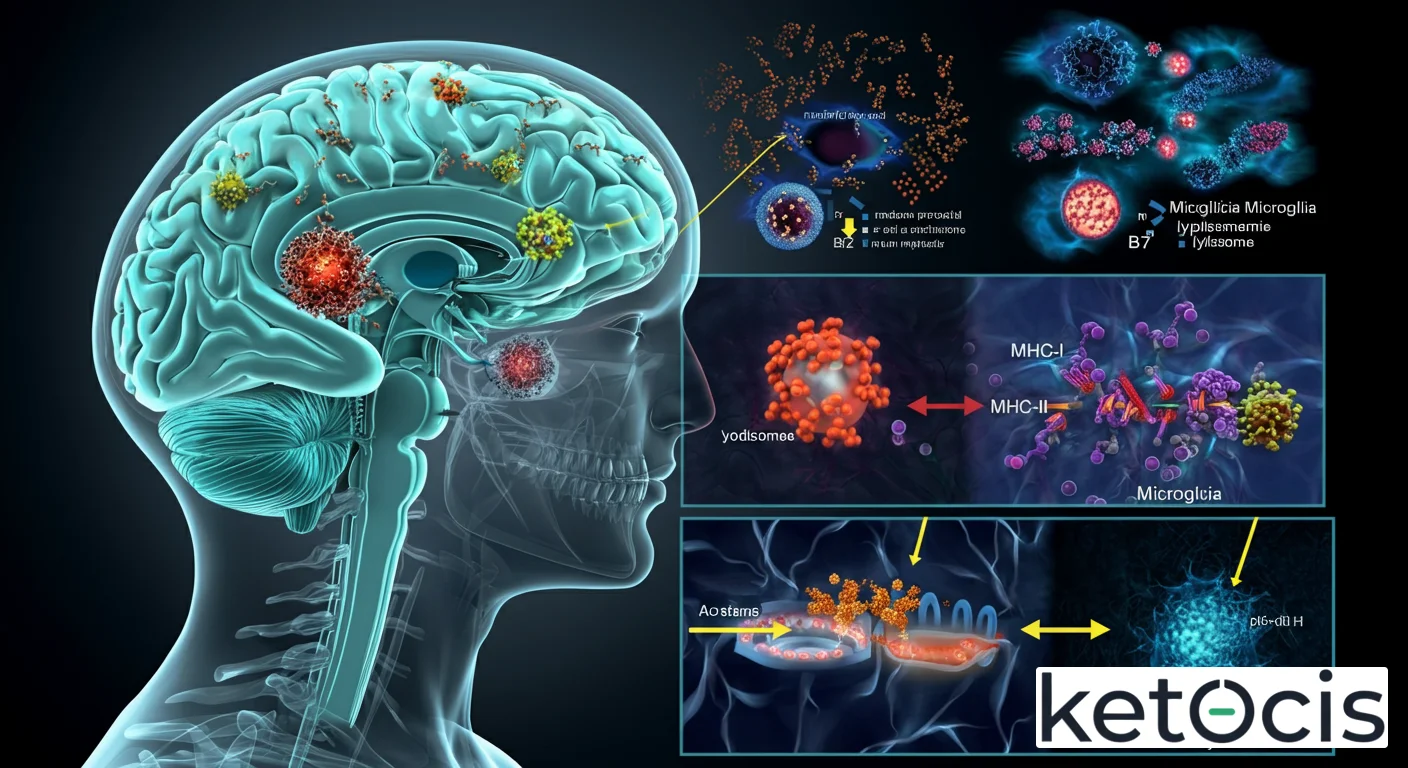
Vía de Procesamiento de Antígenos Clase II
El proceso por el cual el MHC-II microglial presenta antígenos es molecularmente complejo y finamente regulado:
- Captura de Antígenos: Las microglía, como otras APCs, internalizan proteínas extracelulares (antígenos) a través de endocitosis, fagocitosis o pinocitosis.
- Procesamiento en Endosomas/Lisosomas: Una vez dentro de la célula, los antígenos son transportados a compartimentos endosomales y lisosomales ácidos, donde son degradados en péptidos más pequeños por enzimas proteolíticas.
- Síntesis y Transporte de MHC-II: Las cadenas α y β del MHC-II se sintetizan en el retículo endoplasmático (RE). En el RE, se asocian con una proteína llamada cadena invariante (Ii). La Ii tiene dos funciones clave: previene la unión prematura de péptidos endógenos al MHC-II en el RE y dirige el complejo MHC-II-Ii hacia los compartimentos endosomales.
- Intercambio de Péptidos: Dentro de los endosomas especializados, la Ii es parcialmente degradada, dejando un pequeño fragmento llamado CLIP (peptidasa de cadena invariante asociada a clase II). La molécula HLA-DM (una molécula similar al MHC-II pero no presentadora de antígenos) facilita el intercambio de CLIP por péptidos antigénicos de alta afinidad generados a partir de las proteínas internalizadas.
- Expresión en Superficie Celular: Una vez que el péptido antigénico está unido al MHC-II, el complejo es transportado a la superficie de la microglía, donde puede interactuar con los TCR de los linfocitos T CD4+.
Regulación de la Expresión de MHC-II en Microglía
En condiciones de homeostasis, la microglía en el cerebro sano expresa niveles muy bajos o indetectables de MHC-II. Sin embargo, su expresión es drásticamente inducida en respuesta a señales proinflamatorias o de daño. Los principales inductores incluyen:
- Interferón Gamma (IFN-γ): Es el principal inductor de la expresión de MHC-II. Producido por células T activadas y células NK, el IFN-γ señaliza a través de la vía JAK-STAT para activar la transcripción de genes MHC-II.
- Factor de Necrosis Tumoral Alfa (TNF-α) e Interleucina-1 Beta (IL-1β): Estas citocinas proinflamatorias también pueden potenciar la expresión de MHC-II, a menudo en sinergia con IFN-γ.
- Ligandos de TLR (Toll-like Receptor): La activación de TLRs microgliales por patrones moleculares asociados a patógenos (PAMPs) o patrones moleculares asociados a daño (DAMPs) puede iniciar cascadas de señalización que resultan en la inducción de MHC-II.
La expresión de MHC-II por la microglía no solo depende de las señales del microambiente, sino también del estado de activación de la microglía misma. Las microglía “activadas” o “reactivas” son las que tienen mayor probabilidad de expresar altos niveles de MHC-II y, por lo tanto, de ejercer su función presentadora de antígenos.
Biohacking y Optimización
La cetosis nutricional, lograda a través de dietas cetogénicas o ayuno intermitente, ha demostrado modular la actividad microglial. El β-hidroxibutirato (BHB), el principal cuerpo cetónico, actúa como un inhibidor de la histona desacetilasa (HDAC), lo que puede influir en la expresión génica de citocinas proinflamatorias y, potencialmente, en la expresión de MHC-II microglial. Además, el BHB se une al receptor GPR109A, ejerciendo efectos antiinflamatorios directos. Optimizar la cetosis podría ser una estrategia para modular la neuroinflamación y la reactividad microglial en contextos donde la sobreexpresión de MHC-II es perjudicial, promoviendo un ambiente cerebral más resiliente y menos inflamatorio.
Beneficios e Implicaciones: El Doble Filo del MHC-II Microglial
El MHC-II microglial es una herramienta poderosa, pero su impacto en la salud cerebral es un arma de doble filo, con roles tanto neuroprotectores como neuroinflamatorios.
Neuroprotección y Homeostasis
En un contexto fisiológico, la expresión de MHC-II por la microglía es fundamental para mantener la homeostasis cerebral y proteger contra amenazas. Sus funciones neuroprotectoras incluyen:
- Eliminación de Patógenos: Al presentar antígenos de patógenos, la microglía activa linfocitos T específicos que ayudan a erradicar infecciones en el SNC, minimizando el daño neuronal.
- Resolución de Daño: Tras una lesión, la microglía fagocita detritos celulares y presenta autoantígenos. Una respuesta T CD4+ bien regulada puede facilitar la limpieza y la reparación tisular, previniendo la autoinmunidad crónica.
- Tolerancia Central: Se postula que la microglía puede presentar autoantígenos en un contexto no inflamatorio (o “tolerogénico”), lo que podría inducir tolerancia en los linfocitos T que ingresan al SNC, previniendo reacciones autoinmunes indeseadas.
- Vigilancia Inmunológica: El MHC-II microglial permite una supervisión constante, asegurando que cualquier cambio en el microambiente sea detectado y, si es necesario, se active una respuesta inmune adaptativa.
Neuroinflamación y Enfermedades Neurológicas
Sin embargo, una expresión crónica o desregulada de MHC-II microglial puede contribuir significativamente a la patogénesis de diversas enfermedades neurodegenerativas y autoinmunes del SNC. En este escenario, la microglía se convierte en un motor de neuroinflamación sostenida:
- Esclerosis Múltiple (EM): Es el paradigma de una enfermedad autoinmune del SNC donde el MHC-II microglial juega un papel central. La microglía activada presenta autoantígenos de la mielina a los linfocitos T autorreactivos, desencadenando una respuesta inmune que ataca la vaina de mielina, provocando desmielinización y daño axonal.
- Enfermedad de Alzheimer (EA): En la EA, la microglía se activa en respuesta a los depósitos de beta-amiloide y ovillos neurofibrilares de tau. La expresión de MHC-II se eleva en las microglía asociadas a placas, sugiriendo un papel en la presentación de péptidos relacionados con la patología a células T, lo que podría perpetuar la neuroinflamación.
- Enfermedad de Parkinson (EP): La neuroinflamación también es una característica distintiva de la EP. La microglía en la sustancia negra de pacientes con EP expresa MHC-II, implicando su participación en la respuesta inmune contra las neuronas dopaminérgicas degeneradas o agregados de α-sinucleína.
- Accidente Cerebrovascular (ACV) e Isquemia: Después de un ACV, la microglía se activa rápidamente. La expresión de MHC-II es transitoria y puede ser beneficiosa en la fase aguda para la limpieza de detritos, pero una activación prolongada y la presentación de autoantígenos pueden contribuir a la extensión del daño y a la disfunción neurológica a largo plazo.
La clave reside en el contexto y la duración de la activación. Una activación transitoria y controlada con expresión de MHC-II puede ser neuroprotectora, mientras que una activación crónica y desregulada puede ser detrimental.
Alerta Médica
Es un error común simplificar la microglía como «buena» o «mala». La realidad es que su fenotipo y función son extraordinariamente plásticos y dependientes del contexto. La expresión de MHC-II microglial, aunque crítica para la inmunidad cerebral, no es intrínsecamente patogénica. Una activación crónica e inapropiada, que conduce a una neuroinflamación sostenida y a la presentación de autoantígenos en un contexto proinflamatorio, es lo que constituye un riesgo significativo para el desarrollo y progresión de enfermedades neurodegenerativas y autoinmunes. La modulación, no la supresión total, es la clave terapéutica.
Mitos y Realidades sobre el MHC-II Microglial
Mito: El cerebro está completamente aislado del sistema inmune y no necesita MHC-II.
Realidad: Aunque el cerebro goza de un privilegio inmunológico parcial debido a la BHE, no está completamente aislado. Existe una comunicación constante entre el SNC y el sistema inmune periférico a través de puntos de acceso como los plexos coroideos, las meninges y el sistema linfático dural. Las microglía expresan MHC-II precisamente porque la inmunidad adaptativa es necesaria para responder eficazmente a patógenos o daños que ocurren dentro del SNC, proporcionando una vigilancia y respuesta local especializada.
Mito: Toda la microglía expresa MHC-II de forma constitutiva.
Realidad: En condiciones de homeostasis, la microglía residente en el cerebro sano expresa niveles muy bajos o indetectables de MHC-II. Su expresión es inducida y regulada al alza principalmente por citocinas proinflamatorias como el IFN-γ, y en respuesta a la activación por patógenos, daño tisular o estados de enfermedad. Es un marcador de activación microglial y de su capacidad de interactuar con linfocitos T.
Mito: El MHC-II microglial es siempre perjudicial y contribuye a la neurodegeneración.
Realidad: Este es un ejemplo clásico del «doble filo». Si bien el MHC-II microglial juega un papel crucial en la patogénesis de enfermedades como la Esclerosis Múltiple y contribuye a la neuroinflamación en la EA y EP, también es esencial para la neuroprotección y la resolución de infecciones o lesiones. Por ejemplo, en el contexto de una infección viral del SNC, la presentación de antígenos virales por la microglía es vital para eliminar el patógeno. El impacto es altamente dependiente del contexto, la duración de la activación y el tipo de antígeno presentado.
Conclusión: Un Actor Central en la Orquesta Inmune del Cerebro
El Complejo Principal de Histocompatibilidad Clase II (MHC-II) microglial representa un componente fascinante y esencial de la inmunidad cerebral. Desde su propósito evolutivo de conferir al cerebro una capacidad de respuesta inmune adaptativa, hasta su intrincada fisiología molecular que permite la presentación de antígenos a los linfocitos T, su papel es multifacético y contextual.
La microglía, equipada con el MHC-II, actúa como un centinela vigilante, capaz de orquestar respuestas inmunes específicas que son vitales para la eliminación de patógenos y la resolución de daños. Sin embargo, cuando esta maquinaria se desregula, puede convertirse en un motor de neuroinflamación crónica, contribuyendo a la progresión de devastadoras enfermedades neurológicas. La comprensión de estos mecanismos no solo profundiza nuestro conocimiento fundamental del cerebro, sino que también abre nuevas avenidas para el desarrollo de terapias dirigidas que modulen la función microglial y el MHC-II, con la promesa de restaurar la homeostasis cerebral y mejorar la calidad de vida de los pacientes. La interacción entre el metabolismo (como la cetosis) y la función microglial, incluyendo la expresión de MHC-II, es un campo emergente que promete estrategias innovadoras para la optimización de la salud cerebral.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.