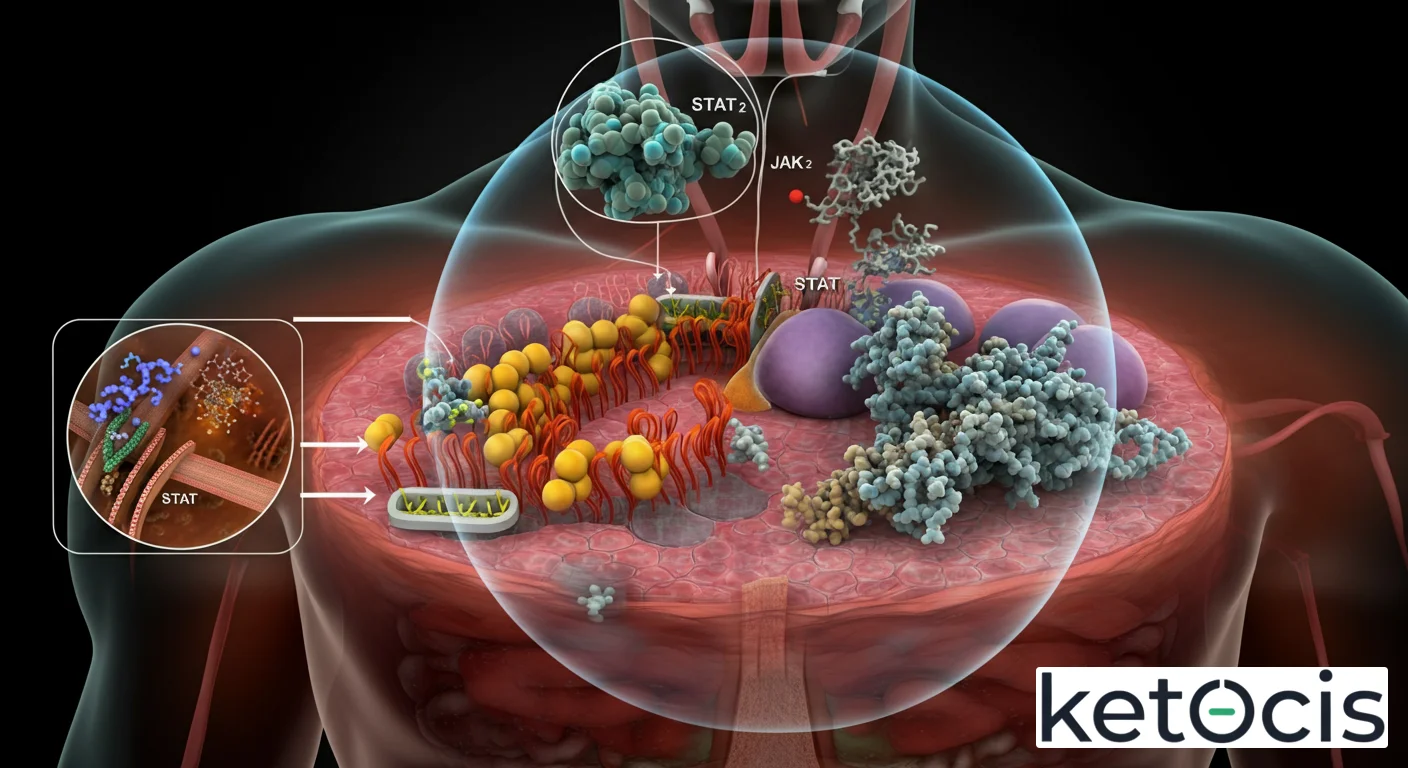
¿Qué es el transductor de señal y activador de transcripción (STAT)? – Análisis Completo y Beneficios
Resumen Clínico Rápido
🔬 Clasificación
Factores de Transcripción
⚙️ Función
Transducción de Señales y Activación Génica
📋 Impacto
Inmunidad, Desarrollo, Cáncer, Metabolismo
En el intrincado universo de la biología celular, la comunicación es la clave para la supervivencia y el funcionamiento armónico de cualquier organismo multicelular. Las células no operan de forma aislada; constantemente reciben y procesan un torrente de información del entorno, desde hormonas y factores de crecimiento hasta citoquinas y nutrientes. Esta capacidad de percibir, interpretar y responder a señales externas es fundamental para procesos tan diversos como el desarrollo embrionario, la respuesta inmune, la homeostasis tisular y la adaptación metabólica.
En el corazón de esta red de comunicación se encuentran los Transductores de Señal y Activadores de la Transcripción, conocidos universalmente por su acrónimo: STAT. Estas proteínas son un pilar central en una de las vías de señalización más directas y eficientes conocidas en la biología: la vía JAK-STAT. Actuando como mensajeros moleculares, los STATs tienen la singular capacidad de traducir señales extracelulares directamente en cambios en la expresión génica dentro del núcleo celular, orquestando así respuestas celulares rápidas y específicas. Su descubrimiento y el desentrañamiento de sus mecanismos han transformado nuestra comprensión de cómo las células coordinan sus funciones, revelando su papel indispensable en la salud y su implicación crítica en la patogénesis de numerosas enfermedades, desde el cáncer hasta los trastornos autoinmunes y metabólicos.
Esta guía enciclopédica desglosará la complejidad de los STATs, explorando su propósito evolutivo, su fisiología molecular, sus roles multifacéticos en la biología y su intrigante conexión con estados metabólicos como la cetosis y el ayuno, ofreciendo una perspectiva integral para el glosario Ketocis.
Resumen Clínico
- Punto clave 1: Los STATs son factores de transcripción que conectan directamente señales de superficie celular (como citoquinas y factores de crecimiento) con la expresión génica en el núcleo.
- Punto clave 2: Desempeñan roles críticos en la inmunidad, el desarrollo, la proliferación celular, la diferenciación y la homeostasis, siendo activados principalmente por la vía JAK-STAT.
- Punto clave 3: La desregulación de la señalización STAT está implicada en diversas patologías, incluyendo cáncer, enfermedades autoinmunes e inflamatorias, y trastornos metabólicos, lo que los convierte en importantes dianas terapéuticas.
Los STATs son siempre proteínas beneficiosas que solo protegen la célula.
Si bien los STATs son cruciales para la homeostasis y la respuesta inmune, su activación constitutiva o aberrante es un motor clave en la progresión de diversos cánceres y enfermedades autoinmunes, transformándose en promotores de patología.
Propósito Evolutivo: La Eficiencia de la Señalización Directa
La vía JAK-STAT representa una de las estrategias más antiguas y conservadas de señalización celular en eucariotas, evidenciando su profundo propósito evolutivo. La necesidad de una respuesta rápida y precisa a los cambios ambientales y a las amenazas internas impulsó el desarrollo de un sistema que pudiera traducir un estímulo externo directamente en una modificación del programa genético de la célula, sin la necesidad de cascadas intermedias largas y complejas que podrían introducir retrasos o errores.
Desde organismos unicelulares hasta mamíferos complejos, la capacidad de detectar y reaccionar ante señales como nutrientes, patógenos o factores de estrés es vital. En organismos multicelulares, esta necesidad se amplifica con la exigencia de coordinar el comportamiento de miles de millones de células para asegurar el desarrollo adecuado, la defensa contra infecciones y la reparación de tejidos. Los STATs surgieron como componentes clave de este sistema de señalización directa, permitiendo que las células respondan de manera eficiente a citoquinas y factores de crecimiento, moléculas que actúan como el lenguaje intercelular principal para coordinar funciones.
La simplicidad y linealidad de la vía JAK-STAT (señal-receptor-JAK-STAT-núcleo-gen) minimizan los pasos y, por ende, el tiempo de respuesta. Esta característica es particularmente ventajosa en contextos donde la velocidad es esencial, como en la respuesta inmune, donde la activación rápida de genes antivirales o antibacterianos puede significar la diferencia entre la erradicación del patógeno y la propagación de la infección. Además, la modularidad de la vía, con diferentes combinaciones de JAKs y STATs respondiendo a distintas citoquinas, permitió una especificidad y una diversidad de respuestas adaptadas a las crecientes complejidades de los organismos.
En esencia, el propósito evolutivo de los STATs fue proporcionar un mecanismo robusto, eficiente y altamente regulado para la transducción de señales, garantizando que las células puedan tomar decisiones rápidas y apropiadas en respuesta a su entorno, lo que es fundamental para la homeostasis, el desarrollo y la supervivencia en un mundo dinámico y desafiante.
Fisiología Molecular: La Coreografía de la Activación Génica
La familia de proteínas STAT comprende siete miembros en mamíferos: STAT1, STAT2, STAT3, STAT4, STAT5A, STAT5B y STAT6. Cada uno exhibe una estructura modular conservada que incluye un dominio N-terminal (NTD), un dominio de enrollamiento en espiral (CCD), un dominio de unión al ADN (DBD), un dominio de unión al SH2 (SH2) y un dominio de transactivación (TAD). Estas regiones son cruciales para la interacción proteína-proteína, la unión al ADN y la activación de la transcripción.
El Mecanismo JAK-STAT: Un Camino Directo al Núcleo
La vía JAK-STAT es un paradigma de señalización intracelular que evita los segundos mensajeros convencionales, permitiendo una comunicación directa entre la membrana plasmática y el genoma. El proceso se despliega en una serie de pasos elegantemente coordinados:
- Reconocimiento del Ligando y Activación del Receptor: El proceso comienza cuando una citoquina, un factor de crecimiento u otra molécula señalizadora (el ligando) se une a su receptor específico en la superficie celular. Muchos de estos receptores carecen de actividad enzimática intrínseca, pero están asociados a una familia de tirosina quinasas citoplasmáticas llamadas Janas Quinasas (JAKs). Existen cuatro miembros de la familia JAK: JAK1, JAK2, JAK3 y TYK2.
- Dimerización del Receptor y Activación de JAKs: La unión del ligando induce un cambio conformacional en el receptor, a menudo causando su dimerización o multimerización. Esta proximidad física activa las JAKs asociadas, que se autofosforilan en residuos de tirosina. Una vez activadas, las JAKs fosforilan residuos de tirosina específicos en la cola citoplasmática de los receptores.
- Reclutamiento y Fosforilación de STATs: Los residuos de tirosina fosforilados en el receptor actúan como sitios de acoplamiento para el dominio SH2 de las proteínas STAT. Una vez reclutados al receptor, los STATs son fosforilados por las JAKs activadas en un residuo de tirosina clave dentro de su dominio SH2.
- Dimerización y Translocación Nuclear: La fosforilación en tirosina de los STATs es el evento crítico que permite su activación. Esta modificación induce un cambio conformacional que expone el dominio SH2 de una molécula STAT para unirse al residuo de tirosina fosforilado de otra molécula STAT, formando un homodímero o heterodímero (por ejemplo, STAT1/STAT1, STAT1/STAT2, STAT3/STAT3). Estos dímeros de STAT activados se disocian del receptor y son transportados activamente al núcleo celular a través de los poros nucleares.
- Unión al ADN y Activación de la Transcripción: Una vez en el núcleo, los dímeros de STAT se unen a secuencias específicas de ADN en las regiones promotoras de sus genes diana, conocidas como elementos GAS (Gamma-activated sites). Esta unión al ADN, junto con las interacciones con coactivadores transcripcionales a través de su dominio TAD, inicia o modula la transcripción de genes específicos, lo que resulta en la síntesis de nuevas proteínas y, en última instancia, en la respuesta celular deseada.
Especificidad y Regulación
La especificidad de la vía JAK-STAT se logra mediante la interacción selectiva entre ligandos, receptores, JAKs y STATs. Por ejemplo, el interferón-gamma activa preferentemente JAK1/JAK2 y STAT1, mientras que la IL-6 activa JAK1/JAK2 y STAT3. Esta modularidad permite que una amplia gama de señales induzca respuestas celulares distintas y finamente sintonizadas.
La vía también está sujeta a una estricta regulación para prevenir la activación excesiva y mantener la homeostasis. Los principales mecanismos de regulación negativa incluyen:
- Proteínas SOCS (Suppressors of Cytokine Signaling): Inducidas por la propia señalización JAK-STAT, las SOCS actúan como un bucle de retroalimentación negativa, inhibiendo directamente las JAKs o compitiendo con los STATs por los sitios de unión en los receptores.
- Tirosina Fosfatasas (PTPs): Estas enzimas desfosforilan los residuos de tirosina en los receptores, JAKs y STATs, terminando la señal.
- Proteínas PIAS (Protein Inhibitors of Activated STATs): Las PIAS se unen a los STATs activados en el núcleo, inhibiendo su unión al ADN o reclutando represores transcripcionales.
Esta compleja coreografía molecular asegura que la señalización STAT sea potente, específica y controlada, permitiendo a la célula responder de manera adaptativa a su entorno.
Beneficios y Roles Fisiológicos
La ubicuidad de la vía JAK-STAT en la señalización celular subraya su importancia crítica en una multitud de procesos fisiológicos esenciales:
- Inmunidad y Defensa del Huésped: Los STATs son actores centrales en la respuesta inmune, mediando los efectos de citoquinas clave como los interferones (IFNs), interleucinas (ILs) y factores estimulantes de colonias (CSFs). Por ejemplo, STAT1 es indispensable para la respuesta antiviral e inmunidad mediada por IFN-gamma. STAT4 es crucial para el desarrollo de células T helper tipo 1 (Th1) y la inmunidad contra patógenos intracelulares. STAT6 promueve la diferenciación de células Th2, importantes en la defensa contra parásitos y en respuestas alérgicas. STAT3, por su parte, es vital para la diferenciación de células Th17 y regula la inflamación y la tolerancia inmune.
- Desarrollo y Diferenciación Celular: Durante el desarrollo embrionario, los STATs guían la formación de diversos tejidos y órganos. Por ejemplo, STAT3 es fundamental en la señalización de LIF (Factor Inhibidor de la Leucemia), manteniendo la pluripotencia de las células madre embrionarias. STAT5 es crucial en la hematopoyesis (formación de células sanguíneas) y en el desarrollo de las glándulas mamarias y la producción de leche.
- Proliferación, Supervivencia y Apoptosis Celular: La activación de STATs, particularmente STAT3 y STAT5, a menudo promueve la proliferación y supervivencia celular al inducir la expresión de genes anti-apoptóticos y pro-mitogénicos. Este rol es vital para la reparación de tejidos y el mantenimiento de la homeostasis, pero también es explotado por las células cancerosas.
- Metabolismo y Homeostasis Energética: Los STATs también juegan un papel en la regulación metabólica. Por ejemplo, STAT3 es un transductor clave de la señal de la leptina, una hormona que regula el apetito y el gasto energético. La activación de STAT3 en el hipotálamo media la supresión del apetito y el aumento del gasto energético. De manera similar, la señalización STAT puede influir en la adipogénesis y la sensibilidad a la insulina.
Estos ejemplos ilustran la versatilidad y la importancia multifacética de los STATs como reguladores maestros de la función celular, asegurando que las células puedan coordinar sus respuestas a una amplia gama de estímulos para mantener la salud y la integridad del organismo.
Biohacking: La Modulación Dietética y los STATs
Investigaciones emergentes sugieren que ciertos compuestos bioactivos presentes en la dieta pueden modular la actividad de los STATs. Por ejemplo, la curcumina (del cúrcuma) y el resveratrol (del vino tinto/uvas) han demostrado inhibir la activación constitutiva de STAT3 en modelos de cáncer y reducir la inflamación al suprimir vías pro-inflamatorias mediadas por STATs. Integrar alimentos ricos en estos fitoquímicos podría ser una estrategia de biohacking nutricional para apoyar la regulación de la señalización STAT y sus efectos antiinflamatorios y anticancerígenos, aunque se requiere más investigación en humanos.
Mitos y Riesgos: La Dualidad de la Potencia
Como con cualquier sistema biológico potente, la desregulación de la vía JAK-STAT puede tener consecuencias patológicas significativas, transformando lo que es un mecanismo vital en un motor de enfermedad.
Mito: Los STATs son siempre proteínas beneficiosas que solo protegen la célula.
Explicación Científica: Si bien los STATs son cruciales para la homeostasis y la respuesta inmune, su activación constitutiva o aberrante es un motor clave en la progresión de diversos cánceres y enfermedades autoinmunes, transformándose en promotores de patología.
Riesgos y Patologías Asociadas a la Desregulación de STATs
- Cáncer: La activación constitutiva (persistente e incontrolada) de STAT3 y STAT5 es una característica distintiva de muchos tipos de cáncer, incluyendo leucemias, linfomas y carcinomas de mama, próstata, pulmón y colon. La activación aberrante de estos STATs promueve la proliferación incontrolada, la supervivencia celular al inhibir la apoptosis, la angiogénesis (formación de nuevos vasos sanguíneos que alimentan el tumor) y la metástasis. Además, STAT3 puede inducir la expresión de genes que suprimen la respuesta inmune antitumoral, permitiendo que las células cancerosas evadan la vigilancia inmunológica. Por estas razones, los inhibidores de STAT3 y STAT5 son una prometedora clase de agentes terapéuticos en investigación oncológica.
- Enfermedades Autoinmunes e Inflamatorias: La hiperactividad de ciertos STATs puede contribuir a la patogénesis de enfermedades autoinmunes y trastornos inflamatorios crónicos. Por ejemplo, una señalización excesiva de STAT1 puede exacerbar la inflamación y el daño tisular en enfermedades como el lupus eritematoso sistémico. La activación descontrolada de STAT3 y STAT4 se asocia con enfermedades inflamatorias intestinales, artritis reumatoide y esclerosis múltiple, al promover la diferenciación de células T pro-inflamatorias (Th1 y Th17).
- Trastornos Metabólicos: La señalización STAT también está implicada en la fisiopatología de trastornos metabólicos. La resistencia a la leptina, un sello distintivo de la obesidad, a menudo se asocia con una señalización defectuosa de STAT3 en el hipotálamo, lo que lleva a una incapacidad para suprimir el apetito. Además, la desregulación de STATs puede influir en la adipogénesis (formación de tejido graso) y la sensibilidad a la insulina, contribuyendo al desarrollo de la diabetes tipo 2.
Alerta Médica: Inhibidores de JAK/STAT y Riesgos Inmunosupresores
Los fármacos que inhiben la vía JAK-STAT, como los inhibidores de JAK (ej., tofacitinib, baricitinib), son altamente efectivos en el tratamiento de enfermedades autoinmunes e inflamatorias crónicas. Sin embargo, al suprimir una vía crucial para la inmunidad, pueden aumentar el riesgo de infecciones oportunistas graves, reactivación de infecciones latentes (como el herpes zóster) y, en algunos casos, ciertos tipos de cáncer. Es fundamental que su uso sea supervisado por un especialista, balanceando los beneficios terapéuticos con los riesgos inmunosupresores.
Los STATs en el Contexto de Ketocis y Ayuno
El estudio de la interacción entre la señalización STAT y los estados metabólicos como la cetosis y el ayuno es un campo de investigación en evolución, pero ya se vislumbran conexiones fascinantes.
La cetosis nutricional y el ayuno intermitente son conocidos por sus efectos antiinflamatorios y su capacidad para modular el sistema inmune. Dado que los STATs son centrales en la señalización de citoquinas pro-inflamatorias (como IL-6, que activa STAT3) e inmunomoduladoras (como interferones, que activan STAT1/2), es plausible que estos estados metabólicos influyan en la actividad de los STATs.
- Reducción de la Inflamación: La cetosis se asocia con una disminución de marcadores inflamatorios sistémicos. Es posible que esto se deba, en parte, a una modulación de la activación de STAT3, que es un promotor clave de la inflamación. El beta-hidroxibutirato (BHB), el principal cuerpo cetónico, ha demostrado tener propiedades antiinflamatorias directas, incluyendo la inhibición del inflamasoma NLRP3, lo que podría indirectamente afectar la producción de citoquinas y, por ende, la activación de STATs.
- Inmunomodulación: El ayuno y la cetosis pueden alterar la función de las células inmunes, induciendo autofagia y promoviendo un fenotipo más tolerogénico o reparador. Estas adaptaciones celulares involucran vías de señalización complejas donde los STATs probablemente juegan un papel. Por ejemplo, la autofagia puede influir en la degradación de componentes de la vía JAK-STAT, afectando su activación.
- Metabolismo de Lípidos y Glucosa: Dado el papel de STAT3 en la señalización de la leptina y su influencia en la adipogénesis, los cambios metabólicos inducidos por la cetosis y el ayuno (como la mejora de la sensibilidad a la insulina y la oxidación de grasas) podrían implicar una reprogramación de la señalización STAT en tejidos metabólicamente activos como el hígado y el tejido adiposo.
Aunque la investigación directa sobre el impacto específico de la cetosis y el ayuno en la actividad de cada miembro de la familia STAT aún está en sus primeras etapas, la comprensión de estas interacciones podría abrir nuevas vías para el biohacking metabólico y el desarrollo de estrategias terapéuticas para enfermedades inflamatorias y metabólicas.
Conclusión
Los Transductores de Señal y Activadores de la Transcripción (STAT) son mucho más que meros intermediarios; son decisores moleculares que orquestan respuestas celulares vitales. Su capacidad para traducir rápidamente señales externas en cambios genéticos los convierte en pilares de la inmunidad, el desarrollo y la homeostasis. Sin embargo, esta misma potencia los hace vulnerables a la desregulación, convirtiéndolos en actores clave en la patogénesis del cáncer, las enfermedades autoinmunes y los trastornos metabólicos. La investigación continua sobre los STATs no solo profundiza nuestra comprensión de la biología fundamental, sino que también abre avenidas prometedoras para el desarrollo de terapias dirigidas, y nos invita a explorar cómo las intervenciones de estilo de vida, como la dieta cetogénica y el ayuno, podrían modular estos intrincados sistemas para optimizar la salud humana.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.