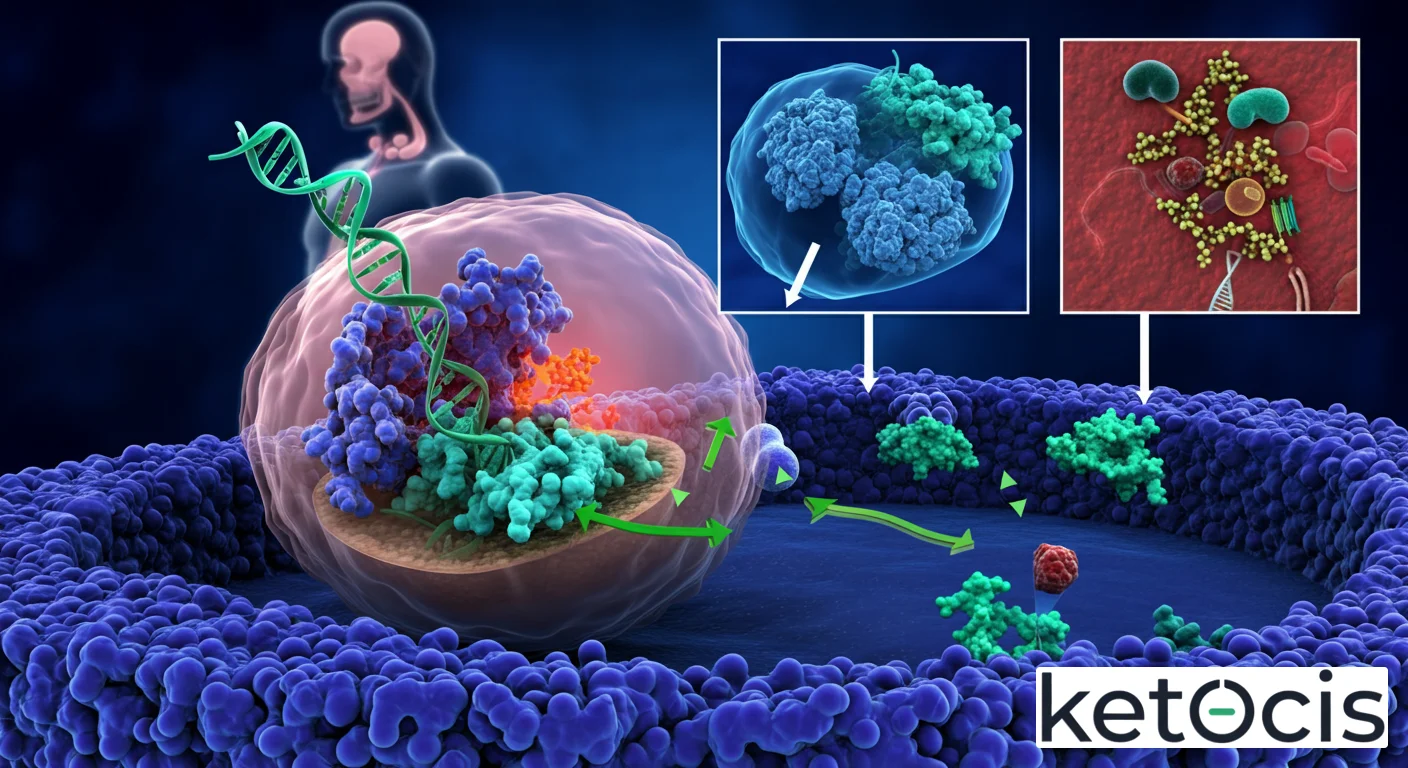
TLR9: Receptor Toll-like 9, Inmunidad y Metabolismo
Resumen Clínico Rápido
🔬 Clasificación
Receptor de Reconocimiento de Patrones (PRR), familia TLR
⚙️ Función
Detecta ADN no metilado (bacteriano/viral)
📋 Impacto
Inmunidad antiviral/bacteriana, autoinmunidad, cáncer
En el vasto y complejo universo de la inmunología, existen centinelas moleculares cuya función es discernir lo propio de lo ajeno, lo benigno de lo patógeno. Entre estos guardianes, el receptor de tipo Toll 9, o TLR9 por sus siglas en inglés (Toll-like Receptor 9), emerge como una pieza fundamental en la orquesta de la inmunidad innata. Este receptor intracelular, estratégicamente ubicado en compartimentos endosomales de células inmunes clave, posee la extraordinaria capacidad de reconocer patrones moleculares asociados a patógenos (PAMPs), específicamente secuencias de ADN no metilado que son características de bacterias y virus. Su activación desencadena una cascada de señalización que culmina en una potente respuesta inflamatoria e antiviral, sentando las bases para una defensa eficaz contra invasores microbianos.
La relevancia de TLR9 no se limita a su papel como detector de amenazas externas. Su disfunción o activación inapropiada está intrínsecamente ligada a diversas patologías, incluyendo enfermedades autoinmunes como el lupus eritematoso sistémico, ciertos tipos de cáncer y condiciones inflamatorias crónicas. Comprender la fisiología molecular de TLR9 y sus intrincadas interacciones con el entorno celular y metabólico no es solo un ejercicio académico, sino una puerta hacia nuevas estrategias terapéuticas y de optimización de la salud. En esta guía definitiva, exploraremos la naturaleza de TLR9, su mecanismo de acción, su papel en la salud y la enfermedad, y cómo podría ser modulado, incluso en el contexto de estados metabólicos como la cetosis y el ayuno.
Resumen Clínico: Puntos Clave sobre TLR9
- Reconocimiento de ADN Patógeno: TLR9 es un receptor crucial que detecta secuencias de ADN no metilado, típicamente de origen bacteriano o viral, activando la inmunidad innata.
- Ubicación Estratégica: Reside en los endosomas de células inmunes como células dendríticas plasmocitoides, macrófagos y linfocitos B, esencial para el procesamiento de patógenos.
- Rol Bifacético: Es indispensable para la defensa antiviral y antibacteriana, pero su activación aberrante puede contribuir a enfermedades autoinmunes y ciertos cánceres.
Origen y Estructura Molecular del Receptor de Tipo Toll 9
Los receptores de tipo Toll (TLRs) son una familia conservada evolutivamente de receptores de reconocimiento de patrones (PRRs) que actúan como la primera línea de defensa inmunológica innata. Descubiertos inicialmente en Drosophila melanogaster por su papel en el desarrollo embrionario y la inmunidad antifúngica, los homólogos mamíferos han revelado una complejidad y especificidad sorprendentes. El TLR9 es uno de los diez TLRs funcionales identificados en humanos, y se distingue por su capacidad para reconocer específicamente el ADN. A diferencia de otros TLRs que se encuentran en la superficie celular y detectan componentes de la membrana bacteriana (como TLR4 para el lipopolisacárido), TLR9 se localiza intracelularmente, predominantemente en los endosomas y lisosomas de células inmunes.
Estructuralmente, TLR9 es una proteína transmembrana tipo I compuesta por un dominio extracelular rico en repeticiones de leucina (LRRs) que es responsable del reconocimiento del ligando, un dominio transmembrana y un dominio citoplasmático conocido como dominio de homología Toll/IL-1 receptor (TIR). El dominio TIR es esencial para la señalización intracelular, sirviendo como plataforma de acoplamiento para proteínas adaptadoras. La secuencia de ADN que TLR9 reconoce son los motivos CpG no metilados, que son abundantes en el genoma bacteriano y viral, pero escasos y altamente metilados en el ADN de mamíferos. Esta diferencia en la metilación permite a TLR9 discriminar entre el ADN patógeno y el propio, un mecanismo crucial para evitar la autoinmunidad.
Un mito común es que todos los receptores de tipo Toll se encuentran en la superficie celular y detectan solo componentes externos de patógenos.
La realidad es que la familia TLR es diversa; mientras algunos, como TLR4, están en la superficie, otros como TLR9 y TLR3 están en compartimentos intracelulares (endosomas), detectando ácidos nucleicos de patógenos que ya han sido internalizados por la célula.
Mecanismo de Acción y Vías de Señalización
La activación de TLR9 es un proceso finamente regulado que comienza con la endocitosis de patógenos o complejos inmunes que contienen ADN. Una vez dentro de los endosomas, el ADN patógeno es liberado y procesado, exponiendo los motivos CpG no metilados. TLR9, al encontrarse en la membrana endosomal, se une a estas secuencias de ADN, lo que induce un cambio conformacional y la dimerización del receptor. Esta dimerización es el evento inicial que recluta proteínas adaptadoras citoplasmáticas al dominio TIR.
La principal proteína adaptadora para TLR9 es la proteína de diferenciación mieloide 88 (MyD88). Una vez reclutada, MyD88 inicia una compleja cascada de señalización que involucra la activación de varias quinasas, como las quinasas asociadas a receptores de IL-1 (IRAKs) y el factor 6 asociado al receptor de TNF (TRAF6). Esta vía conduce finalmente a la activación de factores de transcripción clave, en particular el factor nuclear kappa-B (NF-κB) y los factores reguladores del interferón (IRFs), especialmente IRF7.
La activación de NF-κB resulta en la transcripción de genes pro-inflamatorios, incluyendo citocinas como el factor de necrosis tumoral alfa (TNF-α), la interleucina 6 (IL-6) y la interleucina 1 beta (IL-1β), quimiocinas y moléculas de adhesión. Por otro lado, la activación de IRF7 es crucial para la producción de interferones de tipo I (IFN-α/β), que son citocinas antivirales potentes. Esta doble vía de señalización permite a la célula montar una respuesta inmunológica integral y adaptada al tipo de amenaza detectada. La modulación de la acidez endosomal, por ejemplo, mediante fármacos como la cloroquina, puede inhibir la activación de TLR9 al impedir la disociación del ADN de sus proteínas protectoras y el acceso al receptor.
Rol en la Inmunidad Innata y la Defensa Antiviral/Antibacteriana
El papel principal de TLR9 es actuar como un sensor crítico de infecciones virales y bacterianas. En el contexto de las infecciones virales, TLR9 detecta el ADN viral que se libera durante la replicación del virus o de las partículas virales internalizadas. Esta detección es especialmente importante para virus con genomas de ADN, como los herpesvirus o adenovirus, o virus de ARN que tienen una fase de ADN en su ciclo de vida (retrovirus). La activación de TLR9 en células como las células dendríticas plasmocitoides (pDCs), que son las principales productoras de interferón de tipo I, es vital para una rápida y potente respuesta antiviral.
En las infecciones bacterianas, TLR9 reconoce el ADN genómico bacteriano que es liberado por las bacterias patógenas. Esta detección es crucial para iniciar respuestas inflamatorias que ayudan a eliminar las bacterias. Por ejemplo, en infecciones por Escherichia coli o Mycobacterium tuberculosis, la activación de TLR9 contribuye a la producción de citocinas y quimiocinas que reclutan otras células inmunes al sitio de la infección y coordinan la eliminación del patógeno. La capacidad de TLR9 para diferenciar el ADN microbiano del ADN del huésped es un pilar de la inmunidad innata, protegiéndonos de las amenazas externas sin dañar nuestros propios tejidos.
TLR9 y la Autoinmunidad: Cuando el Sistema se Equivoca
A pesar de su papel protector, una activación inapropiada o desregulada de TLR9 puede tener consecuencias devastadoras, siendo un factor clave en el desarrollo de enfermedades autoinmunes. La autoinmunidad ocurre cuando el sistema inmune, por error, ataca los propios tejidos del cuerpo. En el caso de TLR9, el problema surge cuando el receptor reconoce el ADN del huésped como si fuera un patógeno. Esto puede ocurrir si el ADN propio se presenta de una manera atípica, por ejemplo, en complejos inmunes con anticuerpos anti-ADN o cuando hay una liberación excesiva de ADN nuclear o mitocondrial de células dañadas o apoptóticas.
La enfermedad prototípica asociada a la disfunción de TLR9 es el lupus eritematoso sistémico (LES). En pacientes con LES, se ha observado que los complejos inmunes que contienen ADN propio y anticuerpos anti-ADN pueden ser internalizados por células inmunes, especialmente los linfocitos B y las pDCs. Una vez dentro del endosoma, el ADN propio, que normalmente estaría metilado y sería inaccesible, puede activar TLR9. Esta activación conduce a una producción crónica de interferones de tipo I y otras citocinas pro-inflamatorias, que son características patogénicas del LES. La modulación de TLR9, por lo tanto, representa una estrategia terapéutica prometedora para el tratamiento de estas enfermedades.
TLR9 en la Oncología: Un Arma de Doble Filo
El papel de TLR9 en el cáncer es complejo y a menudo contradictorio, actuando como un arma de doble filo que puede promover o suprimir el crecimiento tumoral dependiendo del contexto. Por un lado, la activación de TLR9 puede ser beneficiosa en la inmunoterapia contra el cáncer. Los agonistas de TLR9 (oligonucleótidos CpG sintéticos) se han investigado como adyuvantes en vacunas contra el cáncer y como agentes inmunoterapéuticos directos. Al activar TLR9 en células inmunes, estos agonistas pueden potenciar la respuesta antitumoral mediante la inducción de citocinas pro-inflamatorias, la maduración de células dendríticas y la activación de células T citotóxicas, lo que lleva a la eliminación de células cancerosas.
Sin embargo, en otros contextos, TLR9 puede promover la progresión del cáncer. Algunos tumores pueden liberar ADN tumoral que activa TLR9 en las células inmunes del microambiente tumoral, lo que puede inducir una respuesta inflamatoria crónica que favorece el crecimiento del tumor, la angiogénesis y la metástasis. Además, en ciertos tipos de cáncer, las propias células tumorales pueden expresar TLR9 y su activación podría promover su proliferación o supervivencia. Esta dualidad subraya la necesidad de una comprensión profunda de los mecanismos específicos de TLR9 en diferentes tipos de cáncer para desarrollar terapias dirigidas y efectivas.
Interacción con Estados Metabólicos: Cetosis y Ayuno
El interés en la interconexión entre el metabolismo y la inmunidad ha crecido exponencialmente. Estados metabólicos como la cetosis nutricional y el ayuno intermitente o prolongado, conocidos por sus efectos antiinflamatorios y moduladores del sistema inmune, podrían influir en la actividad de TLR9. Aunque la investigación directa sobre la modulación de TLR9 por cuerpos cetónicos o el ayuno es aún incipiente, existen mecanismos plausibles.
Los cuerpos cetónicos, en particular el beta-hidroxibutirato (BHB), han demostrado tener efectos antiinflamatorios al inhibir el inflamasoma NLRP3, un complejo proteico que promueve la inflamación. Si bien NLRP3 y TLR9 son vías de señalización distintas, existe una compleja interregulación. La supresión de la inflamación generalizada por BHB podría indirectamente amortiguar la señalización de TLR9 o sus efectos río abajo. Además, el ayuno induce la autofagia, un proceso de reciclaje celular que elimina componentes celulares dañados y patógenos. Una mayor autofagia podría, en teoría, reducir la acumulación de ADN propio o patógeno en los endosomas, disminuyendo así la activación de TLR9 en situaciones de estrés celular o infección.
Otro punto de conexión es el microbioma intestinal. Tanto la cetosis como el ayuno pueden alterar la composición de la microbiota. Un microbioma saludable y equilibrado es fundamental para la homeostasis inmunológica. Las alteraciones en la composición bacteriana podrían modificar la cantidad y el tipo de ADN bacteriano al que están expuestas las células inmunes, influenciando indirectamente la activación de TLR9. La investigación futura deberá desentrañar estas complejas interacciones, pero la hipótesis de que las intervenciones metabólicas pueden afinar la respuesta de TLR9 es intrigante y con un gran potencial terapéutico.
Dato de Biohacking: Modulación de TLR9 y Microbiota
¿Sabías que la diversidad de tu microbioma intestinal podría influir en la actividad de TLR9? Ciertas bacterias comensales producen metabolitos como los ácidos grasos de cadena corta (AGCC) que pueden tener efectos inmunomoduladores. Mantener una microbiota diversa y rica, por ejemplo, a través de una dieta variada y rica en fibra (incluso en cetosis, mediante vegetales bajos en carbohidratos fermentables), o el uso de probióticos específicos, podría optimizar la respuesta de TLR9, favoreciendo su activación protectora frente a patógenos y minimizando su activación autoinmune.
Modulación Farmacológica y Estrategias Terapéuticas
Dada la importancia de TLR9 en la inmunidad y la patología, su modulación se ha convertido en un objetivo atractivo para el desarrollo de fármacos. Los agonistas de TLR9, como los oligonucleótidos CpG sintéticos, han sido explorados en ensayos clínicos como adyuvantes de vacunas para potenciar la inmunogenicidad y como agentes inmunoterapéuticos contra el cáncer y las infecciones crónicas. Su capacidad para activar potentemente las células inmunes, especialmente las pDCs, los convierte en herramientas prometedoras para inducir respuestas inmunes robustas.
Por otro lado, los antagonistas de TLR9 son de gran interés para el tratamiento de enfermedades autoinmunes como el LES, donde la hiperactividad de TLR9 contribuye a la patogénesis. Fármacos como la hidroxicloroquina, comúnmente utilizada en el LES, actúan aumentando el pH endosomal, lo que interfiere con el procesamiento del ADN y la unión a TLR9. Se están desarrollando antagonistas específicos de TLR9, como los oligonucleótidos inhibitorios (iODNs), que pueden bloquear selectivamente la unión del ligando o la dimerización del receptor, ofreciendo una mayor especificidad y menos efectos secundarios que los inmunosupresores generales. La combinación de estos enfoques con estrategias metabólicas podría abrir nuevas vías para el manejo de enfermedades.
Alerta Médica: Riesgos de la Activación Crónica de TLR9
Aunque TLR9 es crucial para la defensa inmunológica, su activación crónica o inapropiada puede ser perjudicial. Una estimulación persistente puede llevar a un estado de inflamación sistémica, contribuyendo a la patogénesis de enfermedades autoinmunes como el lupus eritematoso sistémico. La exposición constante a ADN propio o patógeno, sin una resolución adecuada de la respuesta inmune, puede agotar las células inmunes o inducir daño tisular. Es vital que la respuesta de TLR9 sea transitoria y finamente regulada para mantener la homeostasis inmunológica y evitar efectos adversos a largo plazo.
Conclusión: TLR9, un Pilar de la Inmunidad con Implicaciones Metabólicas
El receptor de tipo Toll 9 (TLR9) es indudablemente un pilar fundamental de la inmunidad innata, dotado de una capacidad única para discernir la presencia de ADN patógeno y orquestar una respuesta defensiva robusta. Su ubicación endosomal y su especificidad por los motivos CpG no metilados lo posicionan como un sensor clave en la lucha contra virus y bacterias, activando vías de señalización que culminan en la producción de citocinas pro-inflamatorias e interferones de tipo I.
Sin embargo, la sofisticación de TLR9 conlleva también una vulnerabilidad. Cuando su intrínseco mecanismo de discriminación falla, o cuando se enfrenta a una carga excesiva de ADN propio, puede volverse un promotor de la autoinmunidad y contribuir a la complejidad de enfermedades como el lupus. Su dualidad en el cáncer, tanto como objetivo terapéutico como posible facilitador tumoral, resalta la necesidad de una investigación continua y matizada. La creciente comprensión de cómo estados metabólicos como la cetosis y el ayuno pueden modular las respuestas inmunes, incluyendo potencialmente la actividad de TLR9, abre un fascinante campo para el biohacking y la medicina personalizada. A medida que desentrañamos más capas de esta compleja molécula, nos acercamos a estrategias más precisas para optimizar la salud y combatir la enfermedad, manteniendo el delicado equilibrio entre la defensa y la tolerancia.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.