Ubiquitinación: Guía Definitiva de Regulación Proteica Celular
Resumen Clínico Rápido
🔬 Clasificación
Proceso Post-Traduccional
⚙️ Función
Regulación Proteica Multifacética
📋 Impacto
Salud, Enfermedad y Longevidad
¿Qué es la Ubiquitinación? La Guía Definitiva del Glosario Ketocis
En el fascinante universo de la biología celular, donde cada molécula y cada proceso orquestan la sinfonía de la vida, la ubiquitinación emerge como un director de orquesta maestro. Lejos de ser un mero mecanismo de «eliminación de basura», este sofisticado proceso post-traduccional es fundamental para la regulación de casi todas las funciones celulares, desde la proliferación y la respuesta inmune hasta la reparación del ADN y la supervivencia neuronal. Para el Glosario Ketocis, comprender la ubiquitinación no es solo adentrarse en la bioquímica, sino entender un pilar de la salud metabólica y la longevidad.
La ubiquitinación es la modificación covalente de una proteína sustrato mediante la adición de una o más moléculas de ubiquitina, una pequeña y altamente conservada proteína reguladora de 76 aminoácidos. Este «marcador» proteico actúa como una etiqueta molecular que puede dirigir a la proteína modificada hacia una multitud de destinos celulares, siendo la degradación por el proteasoma 26S el más conocido, pero no el único ni siempre el principal. Su complejidad y omnipresencia la convierten en un campo de estudio vital para la medicina y el biohacking.
Resumen Clínico
- La ubiquitinación es un proceso esencial de modificación proteica que regula casi todas las funciones celulares.
- Involucra la conjugación de ubiquitina a proteínas sustrato a través de un sistema enzimático de E1, E2 y E3.
- Más allá de la degradación proteica, la ubiquitinación modula la actividad, localización e interacciones de las proteínas.
- Es crucial para la salud metabólica, la respuesta al estrés, la inmunidad y la prevención de enfermedades neurodegenerativas y cáncer.
- Procesos como el ayuno y la cetosis pueden influir positivamente en la eficiencia del sistema de ubiquitinación-proteasoma (UPS).
La ubiquitinación solo degrada proteínas viejas o dañadas.
Si bien es una función crucial, la ubiquitinación es un sistema sofisticado que también regula la actividad, localización e interacción de proteínas sanas, siendo vital para casi todos los procesos celulares no degradativos.
Propósito Evolutivo y Biológico: La Universalidad de un Proceso Vital
La ubiquitinación no es un capricho evolutivo reciente; su maquinaria molecular se ha mantenido notablemente conservada a lo largo de eones, desde la levadura hasta los humanos. Esta conservación subraya su papel indispensable en la supervivencia y adaptación de los organismos eucariotas. Su propósito evolutivo radica en proporcionar a la célula un mecanismo de control de calidad y regulación dinámico y extremadamente preciso para su proteoma.
Las proteínas, las «máquinas moleculares» de la célula, deben ser sintetizadas, plegadas correctamente, activadas, desactivadas y, finalmente, eliminadas de manera eficiente. Sin un sistema como la ubiquitinación, las proteínas mal plegadas o dañadas se acumularían, las señales celulares se descontrolarían y los procesos vitales se detendrían, llevando a la disfunción celular y, en última instancia, a la muerte. Es el guardián de la homeostasis proteica, asegurando que el equilibrio entre la síntesis y la degradación, así como la función, se mantenga en todo momento.
Fisiología Molecular: El Mecanismo Detrás del Proceso
El sistema de ubiquitinación es una cascada enzimática altamente organizada que opera con especificidad y eficiencia. Este proceso, conocido como el Sistema Ubiquitina-Proteasoma (UPS), se basa en la acción coordinada de tres tipos de enzimas y la propia ubiquitina.
La Ubiquitina: La «Marca» Molecular
La ubiquitina es una pequeña proteína compuesta por 76 aminoácidos, caracterizada por su extrema conservación evolutiva. Su nombre proviene de su presencia «ubicua» en todas las células eucariotas. Lo notable de la ubiquitina es que puede unirse a proteínas sustrato de múltiples maneras, formando cadenas con diferentes tipos de enlaces de lisina (K48, K63, etc.), y cada tipo de enlace puede dictar un destino celular distinto para la proteína marcada.
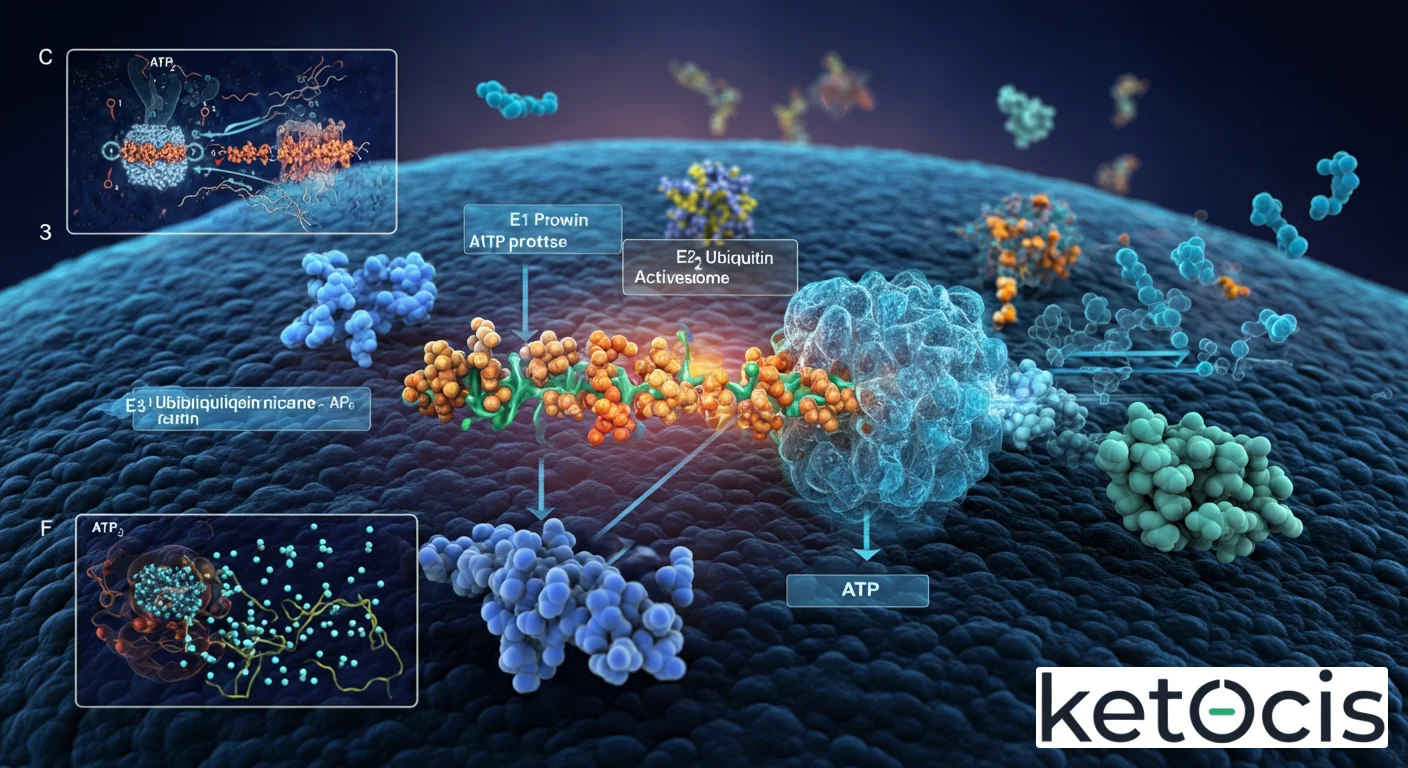
Las Enzimas E1, E2, E3: La «Maquinaria» de Ubiquitinación
La conjugación de ubiquitina a una proteína sustrato es un proceso de tres pasos catalizado por un trío de enzimas:
- E1 (Enzima Activadora de Ubiquitina): Es el primer paso. La E1 activa la ubiquitina en una reacción dependiente de ATP, formando un enlace tioéster de alta energía entre la ubiquitina y la E1. Solo hay un puñado de E1 en mamíferos.
- E2 (Enzima Conjugadora de Ubiquitina): La E1 transfiere la ubiquitina activada a una E2. Hay decenas de E2 diferentes, lo que añade una capa de especificidad al sistema.
- E3 (Ubiquitina Ligasa): Esta es la enzima clave para la especificidad del sustrato. Las E3 reconocen la proteína a ser ubiquitinada y catalizan la transferencia final de la ubiquitina de la E2 al sustrato. Existen cientos de E3 diferentes en el genoma humano, lo que permite la ubiquitinación de miles de proteínas específicas. Las E3 se clasifican principalmente en dos familias: RING (Really Interesting New Gene) y HECT (Homologous to E6-AP C-Terminus), y más recientemente RBR (RING-between-RING).
La especificidad de las E3 es lo que permite que la ubiquitinación sea un proceso tan preciso y versátil, orquestando respuestas celulares específicas a diversos estímulos.
La Cadena de Ubiquitina: El «Código» del Destino
Una vez que una ubiquitina se une a una proteína sustrato (monoubiquitinación), pueden añadirse más moléculas de ubiquitina, formando una cadena. La forma en que se unen estas moléculas (a través de qué residuos de lisina de la ubiquitina, como K48, K63, K11, etc.) determina el «código» que dirige el destino de la proteína. Por ejemplo, las cadenas de poliubiquitina unidas por K48 suelen señalar a la proteína para su degradación por el proteasoma, mientras que las cadenas unidas por K63 a menudo están implicadas en la señalización celular, la reparación del ADN o la endocitosis, sin llevar a la degradación.
El Proteasoma 26S: El «Reciclador» Celular
Para las proteínas marcadas para la degradación, el destino final es el proteasoma 26S. Este es un complejo multiproteico grande y cilíndrico, que actúa como una «máquina trituradora» molecular. Consiste en un núcleo catalítico 20S (donde ocurre la proteólisis) flanqueado por dos complejos reguladores 19S. Los complejos 19S reconocen y se unen a las proteínas poliubiquitinadas, las despliegan (un proceso ATP-dependiente) y las translocan al interior del barril 20S para su degradación en pequeños péptidos. La ubiquitina, por su parte, es reciclada y reutilizada.
Las DUBs: Las «Deshacedoras» de Ubiquitina
Para añadir otra capa de regulación y reversibilidad, existen las enzimas deubiquitinantes (DUBs). Estas enzimas hidrolizan los enlaces de ubiquitina, eliminándola de las proteínas sustrato o desensamblando las cadenas de poliubiquitina. Las DUBs son cruciales para el reciclaje de ubiquitina libre, la edición de cadenas de ubiquitina y la estabilización de proteínas, actuando como contrapeso a las ligasas E3 y añadiendo una enorme complejidad y control al sistema.
Funciones Más Allá de la Degradación: La Versatilidad de la Ubiquitinación
Aunque la degradación de proteínas es una función vital y bien estudiada, la investigación moderna ha revelado que la ubiquitinación es mucho más que una «etiqueta de muerte». Sus roles no degradativos son igualmente cruciales y explican su implicación en una gama tan amplia de procesos celulares:
- Regulación de la Actividad Proteica: La ubiquitinación puede activar o inactivar enzimas, factores de transcripción y otras proteínas, sin degradarlas. Esto puede ocurrir mediante cambios conformacionales o alterando sus sitios de unión.
- Localización Subcelular: La adición de ubiquitina puede dirigir una proteína a un compartimento celular específico, como la membrana plasmática, el núcleo o los endosomas, regulando así su acceso a diferentes vías de señalización.
- Modulación de Interacciones Proteicas: Las cadenas de ubiquitina pueden servir como plataformas de señalización, reclutando otras proteínas que contienen dominios de unión a ubiquitina, facilitando la formación de complejos proteicos o inhibiendo interacciones no deseadas.
- Roles en la Señalización Celular: Es un componente clave en vías de señalización críticas, incluyendo la respuesta inmune (activación de NF-κB), la respuesta al estrés, la apoptosis (muerte celular programada) y la autofagia. Por ejemplo, las cadenas K63-ligadas son fundamentales en la activación de kinasas y la transducción de señales.
- Reparación del ADN: La ubiquitinación de proteínas implicadas en la reparación del ADN es esencial para coordinar la respuesta celular al daño genómico, asegurando la integridad del material genético.
Ubiquitinación y Metabolismo Energético: Un Vínculo Crucial para Ketocis
Para aquellos inmersos en el mundo del Glosario Ketocis, la comprensión de la ubiquitinación es fundamental, ya que este proceso está íntimamente ligado a la salud metabólica, la respuesta al estrés y la eficiencia energética de la célula, especialmente en estados como el ayuno y la cetosis.
Ayuno y Autofagia: Sinergia con el UPS
El ayuno intermitente y prolongado son estrategias conocidas por inducir la autofagia, un proceso de «autoconsumo» celular que recicla componentes celulares dañados u obsoletos. Si bien la autofagia se encarga de estructuras más grandes como orgánulos enteros o agregados proteicos, el Sistema Ubiquitina-Proteasoma (UPS) es el principal responsable de la degradación de proteínas individuales de vida corta, mal plegadas o reguladoras. Sin embargo, ambos sistemas no son mutuamente excluyentes; de hecho, la ubiquitinación es crucial para la autofagia selectiva, donde proteínas o estructuras específicas son marcadas con ubiquitina para ser reconocidas y engullidas por los autofagosomas. En estados de ayuno, la eficiencia de ambos sistemas se optimiza para maximizar el reciclaje de nutrientes y mantener la homeostasis.
Cetosis y Regulación Proteica
La cetosis, un estado metabólico en el que el cuerpo utiliza cuerpos cetónicos como principal fuente de energía, impone un entorno metabólico único en las células. En este contexto, la regulación precisa del proteoma es aún más crítica. La ubiquitinación ayuda a las células a adaptarse a los cambios en la disponibilidad de nutrientes, regulando enzimas metabólicas clave, factores de transcripción y proteínas involucradas en la biogénesis mitocondrial. Un UPS eficiente asegura que las proteínas necesarias para la producción de cuerpos cetónicos o su utilización sean reguladas adecuadamente, mientras que las proteínas innecesarias o dañadas se eliminen, optimizando la función mitocondrial y la eficiencia energética.
Mantenimiento de la Homeostasis Celular
En última instancia, la ubiquitinación es un pilar en el mantenimiento de la homeostasis celular, especialmente bajo estrés metabólico. Permite a las células eliminar rápidamente proteínas que podrían ser tóxicas, como las que se acumulan en el daño oxidativo, o ajustar la expresión y actividad de proteínas en respuesta a cambios en el suministro de nutrientes. Una disfunción en el UPS puede llevar a la acumulación de proteínas aberrantes, estrés del retículo endoplasmático y daño celular, lo que subraya la importancia de mantener este sistema robusto para la salud a largo plazo.
Biohacking Metabólico
Para potenciar la eficiencia del sistema de ubiquitinación-proteasoma (UPS) y la autofagia, considera integrar el ayuno intermitente y el ejercicio de resistencia en tu rutina. Ambas prácticas han demostrado mejorar la capacidad de la célula para reciclar proteínas dañadas y mantener la proteostasis, lo que se traduce en mayor resiliencia celular y un envejecimiento más saludable. Suplementos como la quercetina y el resveratrol también se estudian por su potencial para modular estas vías.
Beneficios y Relevancia Clínica: Impacto en la Salud y la Enfermedad
La ubicuidad y versatilidad de la ubiquitinación significan que su correcto funcionamiento es indispensable para la prevención y tratamiento de numerosas enfermedades. Su disfunción está implicada en una amplia gama de patologías.
Neuroprotección y Enfermedades Neurodegenerativas
Enfermedades como el Alzheimer, el Parkinson y la enfermedad de Huntington se caracterizan por la acumulación de proteínas mal plegadas y agregadas en el cerebro. El UPS es la primera línea de defensa contra estas acumulaciones tóxicas. Una disminución en la eficiencia de la ubiquitinación o el proteasoma contribuye directamente a la patogénesis de estas enfermedades, ya que las neuronas pierden su capacidad para eliminar las proteínas aberrantes. Fortalecer el UPS es, por tanto, una estrategia terapéutica prometedora.
Inmunidad y Respuesta Inflamatoria
La ubiquitinación juega un papel crítico en la regulación de la respuesta inmune. Por ejemplo, es esencial para la activación de la vía NF-κB, un regulador maestro de la inflamación y la inmunidad. También modula la activación de linfocitos T y la presentación de antígenos. Una ubiquitinación desregulada puede llevar a enfermedades autoinmunes o a una respuesta inmune ineficaz contra patógenos.
Control del Ciclo Celular y Cáncer
El ciclo celular, el proceso que controla la división y proliferación de las células, está finamente regulado por la ubiquitinación. Proteínas clave del ciclo celular, como las ciclinas y los inhibidores de ciclinas, son marcadas para la degradación por el UPS en momentos específicos para asegurar una progresión ordenada. La ubiquitinación también regula importantes supresores tumorales como p53 y oncogenes. Disfunciones en este sistema, ya sea por ligasas E3 defectuosas o por la sobreexpresión de DUBs, pueden llevar a una proliferación celular descontrolada y al desarrollo del cáncer.
Envejecimiento y Longevidad
Con la edad, la eficiencia del sistema de ubiquitinación-proteasoma tiende a disminuir. Esta reducción en la capacidad de las células para eliminar proteínas dañadas contribuye a la acumulación de agregados proteicos y al declive funcional asociado al envejecimiento. Mantener un UPS robusto es un sello distintivo de la longevidad y la salud en la vejez, y muchas intervenciones antienvejecimiento, como la restricción calórica y el ejercicio, actúan en parte optimizando este sistema.
Alerta Metabólica: Mitos y Riesgos
Existe el mito de que «demasiada» degradación proteica es siempre perjudicial. Si bien la degradación excesiva puede ser un problema en ciertas condiciones patológicas (ej., atrofia muscular por caquexia), la ubiquitinación controlada es fundamental para la salud. Intentar inhibir indiscriminadamente la ubiquitinación o el proteasoma con «biohacks» no validados puede ser extremadamente peligroso, ya que interrumpe procesos celulares esenciales y puede llevar a la acumulación tóxica de proteínas, disfunción orgánica y enfermedades graves.
Conclusión: La Ubiquitinación como Pilar de la Salud Celular
La ubiquitinación es, sin lugar a dudas, uno de los mecanismos reguladores más fundamentales y complejos de la biología celular. Es un sistema de control de calidad y señalización omnipresente que va mucho más allá de la simple eliminación de proteínas, dirigiendo con precisión la vida y el destino de miles de proteínas en la célula. Desde el mantenimiento de la homeostasis y la respuesta al estrés, hasta la modulación de la inmunidad y la prevención de enfermedades degenerativas, su influencia es profunda y de gran alcance.
Para el Glosario Ketocis, la comprensión de la ubiquitinación nos ofrece una ventana a cómo la célula mantiene su vitalidad y resiliencia. Estrategias como el ayuno y la cetosis, al influir en la eficiencia de este sistema, demuestran el poder de la intervención metabólica para optimizar la salud celular y potencialmente extender la longevidad. La investigación continua en este campo no solo desentraña los misterios de la vida, sino que también abre nuevas avenidas terapéuticas para combatir algunas de las enfermedades más desafiantes de nuestro tiempo, consolidando a la ubiquitinación como un objetivo primordial en la medicina del futuro.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.