Receptores Tirosina Quinasa (RTK): Guía Completa de Señalización
Resumen Clínico Rápido
🔬 Clasificación
Proteínas Transmembrana
⚙️ Función
Transducción de Señales Extracelulares
📋 Impacto
Crecimiento, Diferenciación, Metabolismo, Cáncer
En el vasto y complejo universo de la biología celular, la comunicación es la clave. Cada célula, un microcosmos de actividad, debe interpretar las señales de su entorno para crecer, dividirse, diferenciarse o morir en el momento preciso. Esta intrincada red de comunicación se orquesta, en gran medida, a través de proteínas especializadas en la membrana celular, entre las que destacan los receptores tirosina quinasa (RTK). Son los centinelas moleculares que traducen mensajes extracelulares en respuestas intracelulares, dictando el destino y la función de la célula.
Como Investigador Médico PhD y Copywriter Clínico, mi propósito es desentrañar la fascinante ciencia detrás de los RTK, explorando su estructura, mecanismo de acción, papel crucial en el metabolismo y su implicación en enfermedades. Comprender los RTK no es solo adentrarse en la biología fundamental, sino también abrir una ventana a estrategias de biohacking metabólico y nuevas fronteras terapéuticas que prometen transformar la medicina.
Esta guía enciclopédica definitiva para el Glosario Ketocis te sumergirá en la esencia de estos receptores, revelando su insospechada influencia en nuestra salud y bienestar, desde la regulación de la glucosa hasta el desarrollo del cáncer.
Resumen Clínico
- Punto clave 1: Los Receptores Tirosina Quinasa (RTK) son proteínas transmembrana esenciales para la comunicación intercelular, activándose por la unión de ligandos externos.
- Punto clave 2: Su función principal es la transducción de señales que regulan procesos vitales como el crecimiento, la proliferación, la diferenciación celular, la supervivencia y el metabolismo.
- Punto clave 3: La disregulación de la actividad de los RTK está fuertemente asociada con diversas patologías, incluyendo el cáncer, la diabetes y enfermedades neurodegenerativas, convirtiéndolos en importantes dianas terapéuticas.
Anatomía Molecular de un RTK: Estructura y Componentes
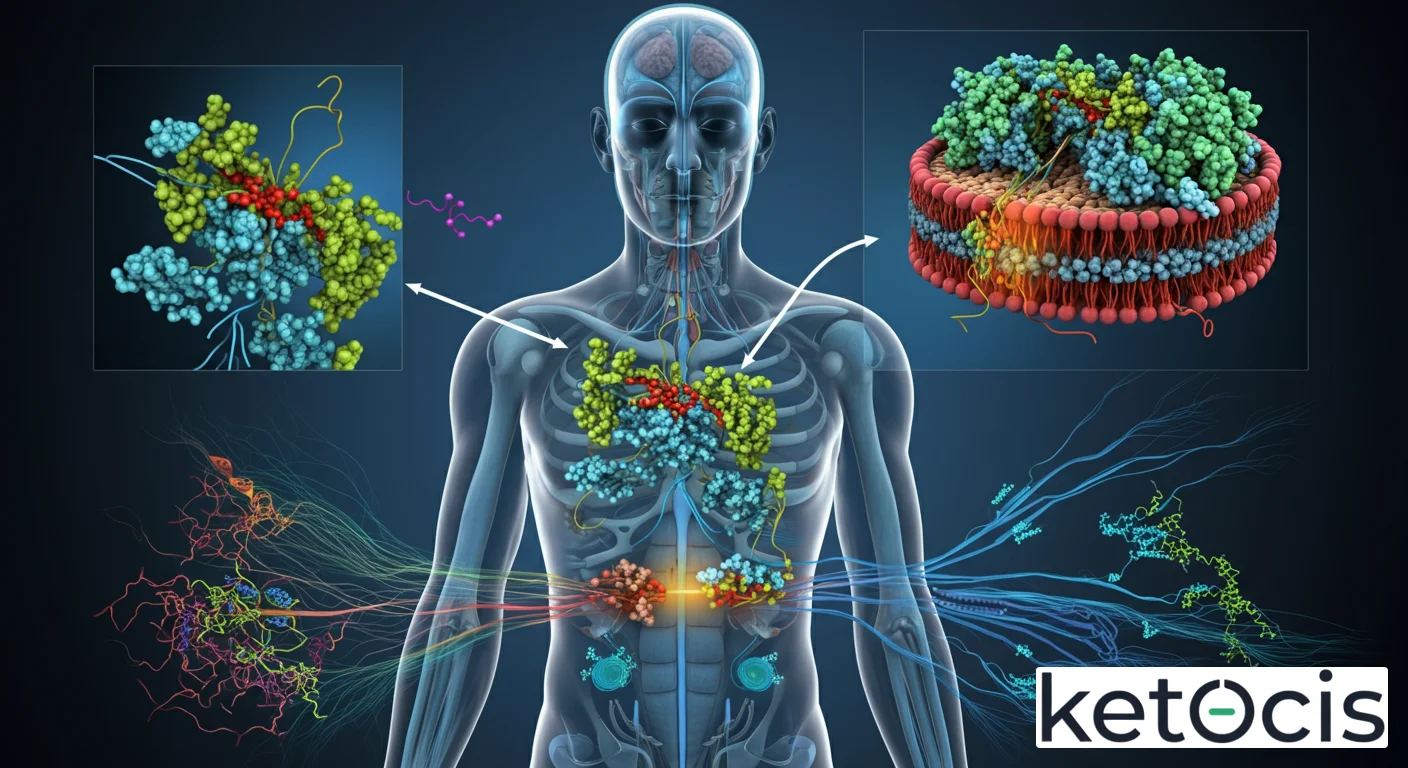
Para comprender cómo funcionan los RTK, primero debemos explorar su arquitectura molecular. Un receptor tirosina quinasa típico es una proteína transmembrana que atraviesa la bicapa lipídica de la célula, dividiéndose en tres dominios principales, cada uno con una función específica y crucial para su actividad.
El primer dominio es el dominio extracelular, la porción del receptor que se extiende fuera de la célula. Este dominio es altamente variable entre los diferentes tipos de RTK y es el encargado de reconocer y unirse específicamente a sus ligandos, que suelen ser factores de crecimiento polipeptídicos, hormonas o citoquinas. La especificidad de esta unión es fundamental para asegurar que la célula responda solo a las señales correctas en el momento adecuado.
El segundo es el dominio transmembrana, una secuencia de aminoácidos hidrofóbicos que ancla el receptor a la membrana plasmática. Este segmento, aunque aparentemente pasivo, es vital para mantener la integridad estructural del receptor y para facilitar los cambios conformacionales que ocurren tras la unión del ligando.
Finalmente, el tercer y más importante dominio funcional es el dominio intracelular. Esta porción del RTK reside en el citoplasma de la célula y contiene la actividad enzimática de la tirosina quinasa. Al activarse, este dominio cataliza la adición de grupos fosfato (fosforilación) a residuos de tirosina específicos, tanto en el propio receptor (autofosforilación) como en otras proteínas diana. Es este evento de fosforilación el que inicia la cascada de señalización intracelular.
Los RTK solo están involucrados en el cáncer.
Si bien la disregulación de los RTK es central en la oncogénesis, estos receptores son fundamentales para procesos fisiológicos normales como el desarrollo embrionario, la inmunidad, la reparación tisular y, crucialmente, la regulación metabólica de la glucosa y los lípidos. Su función es vital para la vida.
Mecanismo de Acción: La Danza de la Señalización Celular
La activación de un RTK es un proceso dinámico y finamente regulado, que comienza con la unión de su ligando específico. Esta unión provoca un cambio conformacional en el receptor que, en la mayoría de los casos, induce la dimerización o multimerización de dos o más moléculas de RTK en la membrana celular. Esta proximidad es esencial para el siguiente paso.
Una vez dimerizados, los dominios intracelulares de las quinasas se activan mutuamente en un proceso conocido como autofosforilación trans. Esto significa que cada monómero fosforila residuos de tirosina en el dominio intracelular de su compañero. Estas tirosinas fosforiladas actúan como “sitios de acoplamiento” o “plataformas de reclutamiento” para una serie de proteínas adaptadoras y enzimas intracelulares.
Estas proteínas de señalización, que contienen dominios de unión a fosfotirosina (principalmente dominios SH2 y PTB), se unen a los RTK activados. Una vez reclutadas, estas proteínas pueden activarse directamente, o servir como enlaces para reclutar aún más componentes, amplificando y diversificando la señal. Este proceso desencadena una compleja cascada de eventos de señalización que se propaga desde la membrana celular hasta el núcleo, modulando la expresión génica y alterando el comportamiento celular.
La Intrincada Red de las Vías de Señalización RTK
La activación de los RTK no es un evento aislado, sino la puerta de entrada a múltiples vías de señalización intracelulares que regulan casi todos los aspectos de la fisiología celular. Las tres vías principales, interconectadas y reguladas, son la vía MAPK/ERK, la vía PI3K/Akt/mTOR y la vía JAK/STAT.
Vía MAPK/ERK: Proliferación y Diferenciación
La vía de la proteína quinasa activada por mitógenos (MAPK) o vía ERK (quinasa regulada por señal extracelular) es una de las cascadas de señalización más estudiadas y conservadas evolutivamente. Se activa por una amplia gama de RTK, como el Receptor del Factor de Crecimiento Epidérmico (EGFR) y el Receptor del Factor de Crecimiento Derivado de Plaquetas (PDGFR). Tras la activación del RTK, se reclutan proteínas adaptadoras como Grb2 y Sos, que a su vez activan la pequeña GTPasa Ras.
Ras activado inicia una cascada de fosforilaciones secuenciales: Raf fosforila MEK, y MEK fosforila ERK. ERK activado transloca al núcleo, donde fosforila factores de transcripción, promoviendo la expresión de genes implicados en la proliferación celular, la diferenciación, la supervivencia y el ciclo celular. Un desequilibrio en esta vía es un sello distintivo de muchos tipos de cáncer.
Vía PI3K/Akt/mTOR: Crecimiento, Supervivencia y Metabolismo
La vía fosfoinositida 3-quinasa (PI3K)/Akt/mTOR es otra cascada crucial, especialmente relevante para el contexto metabólico y de longevidad. Los RTK activados reclutan y activan la PI3K, que fosforila lípidos de membrana para producir PIP3. PIP3, a su vez, recluta y activa la serina/treonina quinasa Akt (también conocida como PKB).
Akt es un nodo central que fosforila una multitud de proteínas diana, promoviendo la supervivencia celular, inhibiendo la apoptosis, regulando el metabolismo de la glucosa (ej. translocación de GLUT4), y estimulando la síntesis de proteínas. Un objetivo clave de Akt es el complejo mTOR (diana de rapamicina en mamíferos), un regulador maestro del crecimiento celular, la proliferación, la síntesis de proteínas y lípidos, y la autofagia. La hiperactividad de esta vía está implicada en el cáncer, la resistencia a la insulina y el envejecimiento.
Vía JAK/STAT: Inmunidad y Hematopoyesis
Aunque no todos los receptores de citoquinas son RTK clásicos, muchos utilizan la vía Janus Quinasa (JAK)/Transductor de Señal y Activador de la Transcripción (STAT), que comparte similitudes mecanísticas. En este caso, las quinasas JAK se asocian a receptores de citoquinas (como los de interferones o interleucinas). La unión del ligando provoca la dimerización del receptor y la activación de las JAK asociadas, que fosforilan residuos de tirosina en el receptor.
Estas tirosinas fosforiladas sirven como sitios de acoplamiento para las proteínas STAT. Una vez unidas, las STAT son fosforiladas por las JAK, se dimerizan y translocan al núcleo, donde actúan como factores de transcripción. Esta vía es fundamental para la respuesta inmune, la hematopoyesis y el desarrollo.
RTK y el Metabolismo: Un Vínculo Esencial
La influencia de los RTK se extiende profundamente en la regulación del metabolismo, siendo actores clave en la homeostasis de la glucosa, los lípidos y el balance energético. Su comprensión es vital para abordar enfermedades metabólicas prevalentes.
Receptor de Insulina (IR): El Maestro Metabólico
El Receptor de Insulina (IR) es quizás el RTK más prominente en el metabolismo. Es un receptor heterodimérico único que se activa por la unión de la insulina, una hormona peptídica central en la regulación de la glucosa. Tras la unión de la insulina, el IR se autofosforila y recluta proteínas sustrato del receptor de insulina (IRS), que a su vez activan la vía PI3K/Akt.
Esta activación conduce a la translocación de transportadores de glucosa (GLUT4) a la membrana celular en tejidos como el músculo y el tejido adiposo, permitiendo la captación de glucosa. También promueve la síntesis de glucógeno y lípidos, y la síntesis proteica. La resistencia a la insulina, una característica de la diabetes tipo 2 y el síndrome metabólico, implica una señalización IR defectuosa, a menudo debido a la fosforilación de residuos de serina/treonina en IRS en lugar de tirosina, interrumpiendo la cascada de señalización.
Receptores de Factores de Crecimiento Similares a la Insulina (IGF-1R)
Los Receptores de Factores de Crecimiento Similares a la Insulina 1 y 2 (IGF-1R e IGF-2R) son RTK estrechamente relacionados con el IR. IGF-1R se activa por el factor de crecimiento similar a la insulina 1 (IGF-1), una hormona con potentes efectos anabólicos, promoviendo el crecimiento celular, la supervivencia y la proliferación. La señalización de IGF-1R converge en gran medida con la vía PI3K/Akt/mTOR, compartiendo muchos sustratos y efectos biológicos con el IR.
La modulación de la señalización de IGF-1/IGF-1R es un área clave en la investigación de la longevidad, ya que niveles elevados se asocian con un mayor riesgo de cáncer y envejecimiento acelerado, mientras que una reducción (observada en el ayuno o dietas restrictivas) puede promover la salud y extender la vida útil.
Receptores de Factores de Crecimiento de Fibroblastos (FGFRs)
Los Receptores de Factores de Crecimiento de Fibroblastos (FGFRs) son una familia de cuatro RTK (FGFR1-4) que responden a los factores de crecimiento de fibroblastos (FGFs). Aunque inicialmente conocidos por su papel en el desarrollo y la reparación tisular, los FGFRs también son reguladores importantes del metabolismo, especialmente del metabolismo de los fosfatos, la glucosa y los lípidos. Por ejemplo, FGF21, a través de FGFR1, actúa como una hormona clave en la respuesta al ayuno, mejorando la sensibilidad a la insulina y promoviendo la oxidación de ácidos grasos.
La disregulación de FGFRs está implicada en diversas patologías, desde trastornos esqueléticos hasta síndromes metabólicos y cáncer, lo que los convierte en atractivas dianas terapéuticas.
Disregulación de RTK: Consecuencias Patológicas
Dada la centralidad de los RTK en la regulación celular, no es sorprendente que su función aberrante esté implicada en una miríada de enfermedades. La disregulación puede surgir de mutaciones genéticas, amplificación génica, sobreexpresión proteica o activación constitutiva.
RTK y Cáncer: Motores Oncogénicos
El vínculo más conocido y estudiado de los RTK es con el cáncer. Muchos RTK, cuando están mutados o sobreexpresados, actúan como oncogenes, promoviendo la proliferación celular incontrolada, la supervivencia, la angiogénesis y la metástasis. Ejemplos prominentes incluyen:
- EGFR (HER1): Mutaciones o amplificación en cáncer de pulmón, cabeza y cuello, colon.
- HER2 (EGFR2): Amplificación en cáncer de mama y gástrico.
- VEGFR (Receptor del Factor de Crecimiento Endotelial Vascular): Promueve la formación de nuevos vasos sanguíneos (angiogénesis), crucial para el crecimiento tumoral.
- PDGFR: Implicado en sarcomas y tumores cerebrales.
La identificación de RTK como motores oncogénicos ha revolucionado el tratamiento del cáncer con el desarrollo de inhibidores de tirosina quinasa (TKIs), fármacos que bloquean selectivamente la actividad de estos receptores, ofreciendo terapias dirigidas que han mejorado drásticamente los resultados en muchos pacientes.
RTK y Enfermedades Metabólicas
Más allá del IR, la disregulación de otros RTK también contribuye a trastornos metabólicos. Por ejemplo, la señalización aberrante de FGFRs puede llevar a problemas de homeostasis de fosfato (ej. raquitismo hipofosfatémico ligado al X) o a resistencia a la insulina. La sobreactivación de vías como PI3K/Akt/mTOR, a menudo downstream de RTK, está ligada a la resistencia a la insulina y la obesidad.
RTK en Enfermedades Neurodegenerativas
Los RTK también juegan un papel crucial en el sistema nervioso central, donde los receptores de neurotrofinas (Trk) son esenciales para la supervivencia, diferenciación y plasticidad neuronal. La disfunción de estos RTK se ha implicado en enfermedades neurodegenerativas como el Alzheimer y el Parkinson, abriendo nuevas vías de investigación terapéutica.
Biohacking y RTK: Optimización Metabólica
¿Sabías que puedes modular la señalización de tus RTK a través de tu estilo de vida? El ayuno intermitente y las dietas cetogénicas son poderosas herramientas de biohacking que reducen los niveles de insulina e IGF-1, atenuando la activación de sus respectivos RTK. Esto promueve vías de longevidad como la autofagia, mejora la sensibilidad a la insulina y puede reducir el riesgo de enfermedades crónicas. ¡Comprender cómo tus elecciones dietéticas impactan a nivel molecular te empodera para optimizar tu salud!
Modulación y Biohacking de los RTK para la Salud Metabólica
La comprensión de los RTK no solo nos permite desarrollar fármacos dirigidos, sino también explorar estrategias de biohacking para optimizar su función y promover la salud metabólica. Aquí, algunas aproximaciones.
Ayuno Intermitente y Dietas Cetogénicas
Estas intervenciones dietéticas han ganado popularidad por su impacto en la salud metabólica y la longevidad. Al reducir drásticamente la ingesta de carbohidratos y/o calorías durante períodos, se observa una disminución significativa en los niveles circulantes de insulina e IGF-1. Esta reducción lleva a una menor activación de los receptores IR e IGF-1R, atenuando la vía PI3K/Akt/mTOR.
La supresión de esta vía, que normalmente promueve el crecimiento y la anabolismo, desvía la célula hacia un estado de reparación y reciclaje (autofagia), mejora la sensibilidad a la insulina y puede prolongar la vida útil en modelos animales. Para los entusiastas del biohacking, esto representa una estrategia molecularmente fundamentada para optimizar la función celular y la resiliencia.
Ejercicio Físico Regular
El ejercicio es una polipíldora que afecta positivamente múltiples vías de señalización de RTK. Mejora la sensibilidad a la insulina en los tejidos periféricos, lo que significa que el IR puede responder de manera más eficiente a la insulina, incluso a niveles más bajos. También modula la expresión de factores de crecimiento y sus receptores, contribuyendo a la salud cardiovascular, muscular y metabólica general.
Nutracéuticos y Compuestos Bioactivos
Algunos compuestos derivados de plantas han demostrado la capacidad de modular las vías de señalización de RTK. Por ejemplo:
- Resveratrol: Polifenol encontrado en uvas, puede modular la vía IGF-1R/Akt/mTOR y activar SIRT1, promoviendo la longevidad.
- Curcumina: Componente activo de la cúrcuma, ha mostrado inhibir la actividad de varios RTK y sus vías descendentes, con potencial antiinflamatorio y anticancerígeno.
- Epigalocatequina galato (EGCG): Polifenol del té verde, puede inhibir la activación de EGFR y VEGFR, entre otros.
Aunque prometedores, estos compuestos requieren más investigación en humanos para confirmar dosis y eficacia, y nunca deben reemplazar tratamientos médicos.
Estrategias Farmacológicas Emergentes
Además de los TKIs en cáncer, la investigación explora cómo modular los RTK para otras enfermedades. Por ejemplo, nuevos sensibilizadores de insulina que actúan más directamente sobre la señalización del IR podrían ofrecer mejores resultados para la diabetes. La comprensión de los RTK es un terreno fértil para la farmacología innovadora.
Alerta Médica: Cuidado con la Automedicación
La complejidad de los Receptores Tirosina Quinasa (RTK) y sus intrincadas vías de señalización significa que cualquier intento de modularlos sin supervisión médica puede tener consecuencias graves e imprevistas. Los inhibidores de tirosina quinasa, por ejemplo, son fármacos potentes con efectos secundarios significativos que deben ser prescritos y monitoreados por especialistas. La automedicación con suplementos que prometen ‘biohackear’ los RTK sin evidencia científica sólida y sin el consejo de un profesional de la salud puede ser peligrosa, alterando equilibrios celulares vitales y exacerbando condiciones preexistentes. Siempre consulta a tu médico antes de iniciar cualquier nueva intervención de salud.
Perspectivas Futuras: RTK como Blanco Terapéutico
La investigación en RTK continúa siendo una de las áreas más dinámicas y prometedoras de la biomedicina. La medicina de precisión, que adapta el tratamiento a las características genéticas y moleculares individuales del paciente, se basa en gran medida en la identificación de RTK mutados o sobreexpresados como dianas.
Se están desarrollando nuevas generaciones de TKIs con mayor especificidad y menor toxicidad, así como terapias combinadas que atacan múltiples vías de señalización simultáneamente para superar la resistencia a los fármacos. Además, la comprensión del papel de los RTK en enfermedades autoinmunes, inflamatorias y neurodegenerativas está abriendo nuevas avenidas para el desarrollo de tratamientos innovadores. La manipulación precisa de la señalización de RTK es una promesa para el futuro de la salud y la enfermedad.
Conclusión
Los receptores tirosina quinasa son mucho más que simples proteínas de membrana; son los arquitectos de la comunicación celular, orquestando una sinfonía de señales que dictan la vida y la muerte de cada célula. Su papel es indispensable en el desarrollo, la fisiología y el mantenimiento de la homeostasis metabólica. Sin embargo, cuando esta orquesta se desafina, los RTK pueden convertirse en impulsores de enfermedades devastadoras como el cáncer y la diabetes.
La ciencia de los RTK no solo ha transformado nuestra comprensión de la biología celular, sino que también ha inaugurado una era de terapias dirigidas y estrategias de biohacking que nos permiten influir en nuestra salud a un nivel molecular. Desde el ayuno intermitente hasta los fármacos más avanzados, la modulación de los RTK representa una de las fronteras más emocionantes en la búsqueda de una vida más larga y saludable. Comprender su funcionamiento es empoderarse con el conocimiento para navegar el complejo paisaje de la salud humana.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.