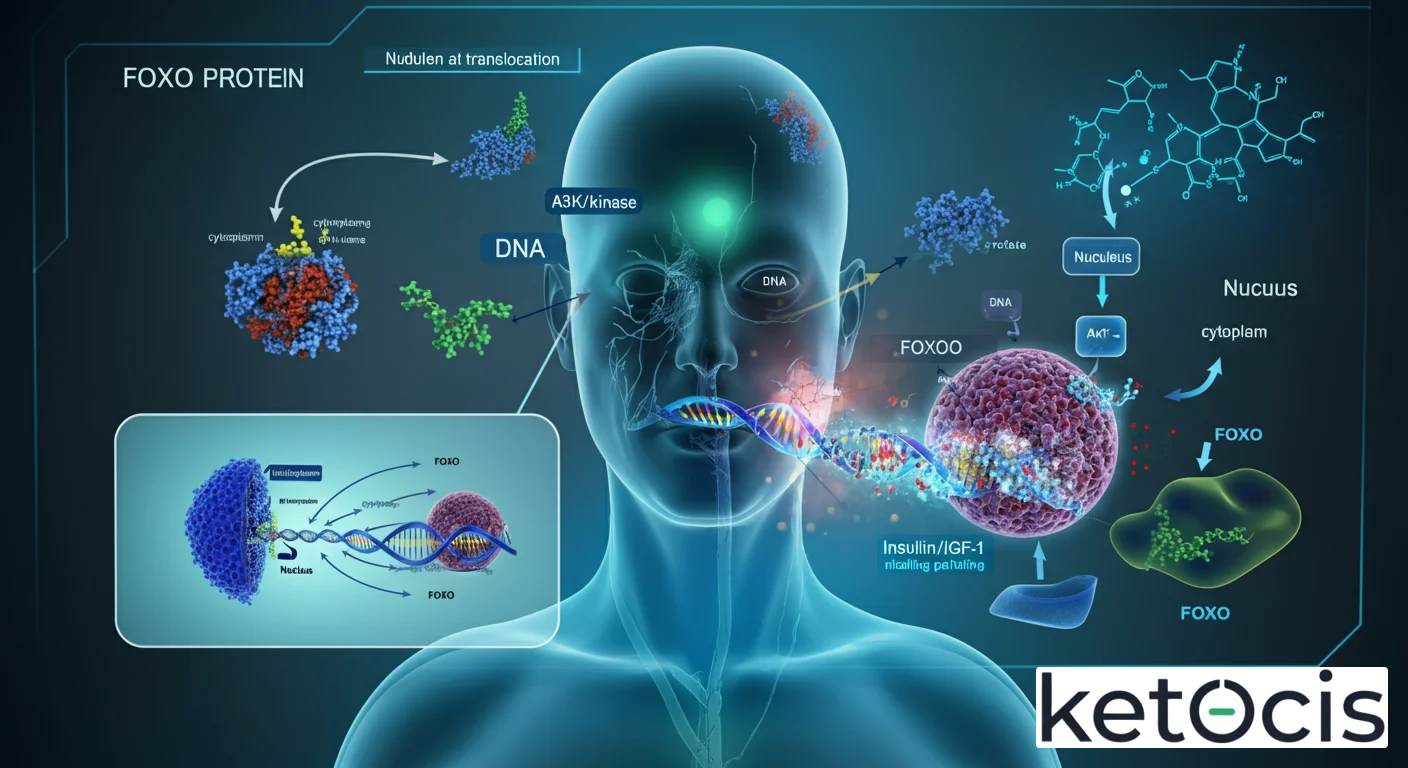
FOXO: El Maestro Genético de la Longevidad y el Metabolismo
Resumen Clínico Rápido
🔬 Clasificación
Factor de Transcripción (Familia Forkhead Box)
⚙️ Función
Regulación de genes de longevidad, estrés, metabolismo, apoptosis, autofagia
📋 Impacto
Central en envejecimiento, cáncer, diabetes, enfermedades neurodegenerativas
¿Qué es el factor de transcripción FOXO? El guardián genético de la longevidad
En el intrincado universo de la biología molecular, donde cada proteína y cada secuencia de ADN orquestan la sinfonía de la vida, existen directores de orquesta que sobresalen por su influencia y versatilidad. Uno de estos directores magistrales es el factor de transcripción FOXO (Forkhead box O), una familia de proteínas que actúa como un centinela genético, regulando una miríada de procesos celulares fundamentales para la supervivencia, la resistencia al estrés y, en última instancia, la longevidad. Comprendido en su esencia, FOXO no es solo una molécula, sino un eje central que conecta las señales del entorno, como la disponibilidad de nutrientes y el estrés oxidativo, con la expresión génica, dictando así el destino de una célula y, por extensión, de un organismo.
Descubierto inicialmente por su papel en la regulación del ciclo celular y la apoptosis, la investigación sobre FOXO ha florecido, revelando su participación crítica en la homeostasis metabólica, la respuesta inmune, la reparación del ADN y la autofagia. Su relevancia se extiende desde organismos unicelulares hasta mamíferos complejos, lo que subraya su importancia evolutiva. En el contexto de dietas cetogénicas, ayuno intermitente y otras intervenciones metabólicas, FOXO emerge como un actor principal, mediando muchos de los beneficios asociados a estas prácticas. Este profundo entendimiento de FOXO no solo desvela los secretos de la biología del envejecimiento, sino que también abre nuevas vías para estrategias terapéuticas y de optimización de la salud.
Resumen Clínico
- Punto clave 1: FOXO es una familia de factores de transcripción clave que regula la expresión de genes implicados en la longevidad, la resistencia al estrés oxidativo, el metabolismo y el ciclo celular.
- Punto clave 2: Su actividad es finamente modulada por vías de señalización cruciales como la de insulina/IGF-1 y se activa bajo condiciones de estrés celular y ayuno, promoviendo la autofagia y la reparación celular.
- Punto clave 3: La disfunción de FOXO está implicada en diversas patologías, incluyendo el cáncer, la diabetes, enfermedades neurodegenerativas y el envejecimiento, convirtiéndolo en un objetivo terapéutico prometedor.
Origen y Nomenclatura del Factor de Transcripción FOXO
La historia de los factores FOXO comienza con el descubrimiento de la familia de proteínas Forkhead box (FOX), caracterizadas por un dominio de unión al ADN conservado, conocido como el dominio forkhead, que se asemeja a una horquilla. Este dominio fue identificado por primera vez en el gen forkhead de Drosophila melanogaster, implicado en el desarrollo embrionario. La subfamilia ‘O’ de FOXO se distingue por su papel específico en la regulación de la longevidad y el metabolismo. En mamíferos, existen cuatro isoformas principales: FOXO1, FOXO3, FOXO4 y FOXO6, cada una con patrones de expresión tisular y funciones ligeramente superpuestas pero también distintivas. Por ejemplo, FOXO1 es abundante en el hígado y el músculo, crucial para la gluconeogénesis y el metabolismo de los lípidos, mientras que FOXO3 está ampliamente expresado y es un regulador clave de la longevidad en muchos organismos.
Desde su identificación, la investigación ha revelado que estos factores de transcripción no son meros interruptores genéticos, sino complejos integradores de señales. Su actividad no es constante, sino que está finamente regulada por una red de vías de señalización intracelular, lo que les permite adaptar la respuesta celular a las cambiantes condiciones fisiológicas y ambientales. Comprender su origen y la diversidad de sus miembros es el primer paso para desentrañar su profunda influencia en la fisiología.
El ayuno es universalmente bueno para todos los aspectos de la salud sin excepción.
Aunque el ayuno ofrece numerosos beneficios mediados por vías como FOXO, su aplicación debe ser individualizada. En ciertos contextos (ej. desnutrición, embarazo, enfermedades crónicas específicas, o dosis excesivas), el ayuno puede ser contraproducente. La respuesta metabólica varía y siempre debe considerarse la supervisión médica.
Mecanismo de Acción: Cómo FOXO Orquesta la Expresión Génica
Los factores FOXO ejercen su función principal como factores de transcripción, lo que significa que se unen a secuencias específicas de ADN en la región promotora de los genes diana para regular su expresión. Esta unión se realiza a través de su dominio forkhead, que reconoce el elemento de respuesta FOXO (FHRE, por sus siglas en inglés). Una vez unidos, los FOXO pueden activar o reprimir la transcripción de genes, dependiendo del contexto celular y de la interacción con otros cofactores.
El mecanismo de acción de FOXO es altamente dinámico y está influenciado por múltiples modificaciones post-traduccionales. La más estudiada es la fosforilación. La vía de señalización de la insulina/IGF-1 (Factor de Crecimiento similar a la Insulina 1) es el principal regulador negativo de la actividad de FOXO. Cuando los niveles de insulina o IGF-1 son altos (indicando abundancia de nutrientes), la proteína quinasa B (Akt) se activa y fosforila a FOXO. Esta fosforilación provoca la exclusión de FOXO del núcleo celular, reteniéndolo en el citoplasma. En el citoplasma, FOXO es a menudo ubiquitilado y dirigido a la degradación proteasomal, lo que reduce su capacidad para regular la expresión génica.
Por el contrario, bajo condiciones de baja insulina/IGF-1, como durante el ayuno o la restricción calórica, Akt se inactiva, y FOXO permanece desfosforilado. Esto le permite translocarse al núcleo, donde se une al ADN y activa la transcripción de genes clave. Entre los genes diana regulados por FOXO se incluyen:
- Genes de resistencia al estrés: Catalasas, superóxido dismutasas (SOD), que combaten el estrés oxidativo.
- Genes de metabolismo: Enzimas de la gluconeogénesis (G6Pasa, PEPCK), que aumentan la producción de glucosa en el hígado.
- Genes de autofagia: Atg genes (Autophagy-related genes), que promueven la degradación y reciclaje de componentes celulares dañados.
- Genes de ciclo celular y apoptosis: p21, p27, Bim, FasL, que detienen el ciclo celular o inducen la muerte celular programada en células dañadas.
- Genes de reparación del ADN: GADD45, que facilitan la reparación genómica.
Esta compleja red de regulación permite a FOXO actuar como un sensor metabólico y de estrés, adaptando la respuesta celular para mantener la homeostasis y promover la supervivencia en condiciones adversas. Su capacidad para activar programas de mantenimiento y reparación celular lo posiciona como un actor central en los procesos antienvejecimiento.
Regulación de FOXO: Más Allá de la Fosforilación
Aunque la fosforilación por Akt es el mecanismo regulador más prominente, la actividad de FOXO está sujeta a una orquestación aún más compleja. Otras quinasas, como las quinasas del estrés (JNK y p38 MAPK), pueden fosforilar FOXO en diferentes sitios, promoviendo su actividad nuclear en respuesta al estrés. Por otro lado, la acetilación, la metilación y la ubiquitilación también desempeñan roles cruciales.
Las sirtuinas, en particular SIRT1, son desacetilasas que interactúan con FOXO. La desacetilación de FOXO por SIRT1 generalmente aumenta su actividad transcripcional, especialmente en la activación de genes relacionados con la resistencia al estrés y la longevidad. Esta interacción es un punto clave en la mediación de los efectos de la restricción calórica, ya que SIRT1 se activa en estas condiciones. La ubiquitilación, por su parte, marca a FOXO para su degradación por el proteasoma, sirviendo como un mecanismo para disminuir rápidamente sus niveles cuando su actividad ya no es necesaria.
Además, la interacción de FOXO con otras proteínas coactivadoras o correpresoras dentro del núcleo también modula su especificidad de unión al ADN y su potencia transcripcional. Esta intrincada red de modificaciones post-traduccionales y asociaciones proteicas permite una respuesta celular altamente contextualizada y adaptable, asegurando que FOXO actúe de manera óptima para preservar la integridad celular.
FOXO en el Contexto de la Cetosis y el Ayuno
La relación entre FOXO y las intervenciones metabólicas como la dieta cetogénica y el ayuno intermitente es uno de los campos de investigación más fascinantes. Ambas estrategias dietéticas se caracterizan por una reducción en los niveles de glucosa e insulina, y un aumento en los cuerpos cetónicos. Esta disminución de la señalización de insulina/IGF-1 es un potente activador de FOXO. Durante el ayuno, la reducción de insulina conduce a una menor actividad de Akt, permitiendo que FOXO se desfosforile y se transloque al núcleo.
Una vez en el núcleo, FOXO activa programas genéticos que son fundamentales para la adaptación al ayuno y la promoción de la salud:
- Gluconeogénesis: En el hígado, FOXO1 es un inductor clave de las enzimas gluconeogénicas, asegurando un suministro constante de glucosa para los tejidos dependientes de glucosa, como el cerebro, cuando los carbohidratos dietéticos son escasos.
- Autofagia: La activación de FOXO promueve la autofagia, un proceso de limpieza celular esencial que elimina orgánulos dañados y proteínas agregadas. Esto es crucial para el mantenimiento celular y la prevención del envejecimiento.
- Resistencia al estrés oxidativo: Al activar genes antioxidantes, FOXO protege a las células del daño causado por los radicales libres, un beneficio clave del ayuno.
- Mantenimiento de células madre: FOXO contribuye al mantenimiento de la quiescencia y la funcionalidad de las células madre en varios tejidos, lo que es vital para la regeneración y reparación.
Así, FOXO actúa como un mediador molecular clave de muchos de los efectos beneficiosos observados con la restricción calórica y el ayuno, desde la mejora de la sensibilidad a la insulina hasta el aumento de la longevidad. Su activación es un pilar fundamental en la capacidad del cuerpo para adaptarse y prosperar en condiciones de escasez de nutrientes, lo que refleja su profundo propósito evolutivo.
Dato de Biohacking: Potenciando tu FOXO
¿Sabías que ciertos compuestos naturales pueden activar directamente la vía FOXO, incluso sin un ayuno prolongado? La resveratrol, un polifenol que se encuentra en el vino tinto y las bayas, y la curcumina, el componente activo de la cúrcuma, han demostrado en estudios preclínicos la capacidad de inducir la activación de FOXO, imitando algunos de los efectos de la restricción calórica. Esto ocurre a menudo a través de la activación de SIRT1, que a su vez desacetila y activa FOXO. ¡Considera estos superalimentos como aliados en la optimización de tu resiliencia celular!
Implicaciones Clínicas y Vías Terapéuticas
La ubicuidad de FOXO en la regulación de procesos celulares fundamentales lo convierte en un actor central en la salud y la enfermedad. Su disfunción está implicada en una amplia gama de patologías crónicas:
- Cáncer: En muchos tipos de cáncer, la actividad de FOXO se suprime, a menudo debido a la hiperactivación de la vía PI3K/Akt. Esta supresión permite que las células cancerosas evadan la apoptosis, proliferen sin control y resistan las terapias. Restaurar la actividad de FOXO se considera una estrategia prometedora en la terapia contra el cáncer.
- Diabetes Tipo 2: FOXO1 es crucial para la homeostasis de la glucosa. Su hiperactivación en el hígado puede contribuir a la resistencia a la insulina y la hiperglucemia al aumentar la gluconeogénesis. Sin embargo, en las células beta del páncreas, FOXO1 protege contra el estrés oxidativo y la apoptosis, manteniendo la función de las células beta. Su papel es, por tanto, contextual y complejo.
- Enfermedades Neurodegenerativas: En patologías como el Alzheimer y el Parkinson, FOXO desempeña un papel protector al promover la autofagia y la resistencia al estrés oxidativo en las neuronas. La reducción de la actividad de FOXO se ha asociado con una mayor susceptibilidad al daño neuronal.
- Enfermedades Cardiovasculares: FOXO contribuye a la salud cardiovascular al regular la homeostasis vascular, la respuesta al estrés y la autofagia en las células cardíacas y endoteliales, protegiendo contra la aterosclerosis y la insuficiencia cardíaca.
- Envejecimiento: La disminución de la actividad de FOXO con la edad contribuye a la acumulación de daño celular, la disfunción metabólica y la senescencia, acelerando el proceso de envejecimiento.
Dada su centralidad, FOXO representa un objetivo terapéutico atractivo. Estrategias que modulan su actividad (activadores o inhibidores selectivos) podrían tener un impacto significativo en el tratamiento de estas enfermedades. Por ejemplo, los fármacos que inhiben la vía PI3K/Akt podrían indirectamente activar FOXO y ser útiles en el cáncer, mientras que los activadores directos de FOXO podrían ser beneficiosos en enfermedades neurodegenerativas.
Alerta Metabólica: El Doble Filo de la Activación de FOXO
Aunque la activación de FOXO es generalmente beneficiosa para la longevidad y la resistencia al estrés, un exceso o una activación desregulada crónica pueden tener efectos adversos. Por ejemplo, una activación excesiva de FOXO1 en el hígado puede contribuir a la resistencia a la insulina y la hiperglucemia al promover una gluconeogénesis hepática incontrolada en ciertas condiciones patológicas. Además, en algunos contextos de cáncer, la activación de FOXO puede no ser siempre protectora, ya que las células tumorales pueden cooptar sus vías para su propia supervivencia. Es crucial entender el contexto celular y la dosis de activación para evitar consecuencias no deseadas; la homeostasis es clave.
Conclusión: FOXO, el Guardián de la Resiliencia Celular
El factor de transcripción FOXO es mucho más que una simple proteína; es un integrador maestro de señales que posiciona a las células y a los organismos para responder de manera adaptativa a los desafíos ambientales y metabólicos. Su papel crucial en la regulación de la longevidad, la resistencia al estrés, el metabolismo, la reparación del ADN y la autofagia lo convierte en una de las moléculas más estudiadas y prometedoras en la biología del envejecimiento y las enfermedades crónicas.
Desde la perspectiva de la optimización de la salud, comprender cómo podemos modular la actividad de FOXO a través de estilos de vida (como el ayuno intermitente y dietas bajas en carbohidratos) y compuestos bioactivos abre un vasto panorama de posibilidades. Sin embargo, como con cualquier sistema biológico complejo, la clave reside en el equilibrio. La investigación futura continuará desentrañando las complejidades de la regulación de FOXO y sus interacciones con otras vías, allanando el camino para intervenciones más precisas y personalizadas que aprovechen el poder de este guardián genético para promover una vida más larga y saludable.
El estudio de FOXO nos recuerda que la salud y la enfermedad son el resultado de una danza molecular finamente coreografiada, y que al entender a los principales bailarines, podemos aprender a influir en el ritmo de la vida misma.
Preguntas Frecuentes Relacionadas
¿Cuánto tiempo tarda el proceso metabólico?
El tiempo varía según el metabolismo individual y la adherencia a la restricción de carbohidratos, pero generalmente toma de 2 a 4 días en condiciones estrictas.
¿Cómo mido mis niveles de forma óptima?
Se recomiendan los medidores de sangre para mayor precisión clínica (miden beta-hidroxibutirato), aunque existen opciones de aliento y tiras de orina para principiantes.
¿Es normal sentir fatiga al inicio?
Sí, durante la fase de adaptación es común experimentar la «gripe keto». Mantener una óptima hidratación y reponer electrolitos (sodio, potasio, magnesio) mitiga drásticamente estos efectos.
Explorar Glosario Médico
Explora Nuestros Centros Temáticos
Tu Panel Metabólico
Sincroniza tus registros y monitorea tu progreso en tiempo real con Ketocis Tracker.
Directorio de Recetas Keto
Explora nuestra base de datos completa de platillos bajos en carbohidratos.